Лекарственные растения, содержащие терпеноиды и масла
Фармакогнозия. Карпук В.В. – 2011
Лекарственные растения и лекарственное растительное сырье, содержащие сесквитерпеноиды
Лекарственные растения и лекарственное растительное сырье, содержащие ароматические соединения
ТЕРПЕНОИДЫ
Название «терпеноиды» происходит от немецкого слова Terpentin— скипидар, который почти целиком состоит из монотерпеноидов. Терпеноиды, или изопреноиды, — углеводороды растительного происхождения, которые в своем составе имеют кратное число фрагментов изопрена. СН2=С (СН3)—СН=СН2, или (С5Н8) — изопрен.
В зависимости от числа таких групп терпеноиды подразделяют на:
- -гемитерпены — С5Н8— газы;
- -монотерпены — С10Н16 — эфирные масла, горечи;
- -сесквитерпены — С15Н24 — эфирные масла, горечи;
- -дитерпены — С20Н32— фитол, витамины К, Е, камеди, смолы;
- -тритерпены — С30Н48— смолы, стерины, сапонины;
- -тетратерпены — С40Н64— каротиноиды;
- -политерпены — (С5Н8)n— каучук, гутта.
Физико-имические свойства
Терпены — углеводороды, не содержащие кислород. Имеются и соединения, содержащие кислород. Их называют терпеноидами. Биосинтез терпеноидов основан на мевалонатном пути биосинтеза вторичных метаболитов и начинается с конденсации двух молекул ацетилкоэнзима А (ацетил-КоА) с образованием мевалоновой кислоты.

Образование мевалоновой кислоты — важнейшая стадия на пути биосинтеза терпеноидных соединений. Эта реакция практически необратима. Следователь но, углерод, вошедший в мевалоновую кислоту, в отличие от углерода предшествующих метаболитов, не возвращается в обменные циклы клетки, а направляется в своих дальнейших превращениях только по пути образования веществ терпеноидной структуры. В этом смысле мевалоновая кислота — первый ключевой специфический предшественник всех без исключения терпеноидных соединений, благодаря чему она может быть определена как их«прародитель», а весь путь био синтеза терпеноидных соединений называют мевалонатным путем. Мевалоновая кислота становится строительным компонентом для создания терпеноидов после трансформации в изопентинилдифосфат. Дальнейшее наращивание углеродной цепи идет путем конденсации молекул изопентинилдифосфата: в геранилдифосфат, фарнезилдифосфат и т. д. Катализируют этот процесс ферменты пренилтрансферазы. Обычно связывание мономеров терпеноидов происходит по типу «голова к хвосту», как, например, при образовании геранил- и фарнезилдифосфатов. Реже конденсация осуществляется по типу «хвост к хвосту», например образование сквалена из молекул фарнезилдифосфата.

Возможен также третий тип — реакции пренилирования: конденсация с переносом пренильного остатка на нетерпеноидный акцептор — при биосинтезе сложных терпеноидов, состоящих из терпеноидной и нетерпеноидной частей. Одним из продуктов метаболизма терпеноидов является циклопентанпергидрофенантрен — структура, лежащая в основе молекул кардиогликозидов, сапонинов, стероидов и стероидных алкалоидов.
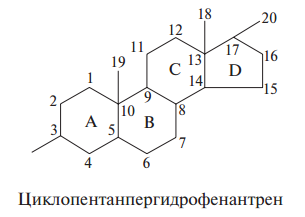
Терпеноиды широко распространены в ЛР. Классификация ЛРС, содержащего терпеноиды, основывается на важнейшихих компонентах, оказывающих терапевтическое действие на организм человека. Прежде всего мы рассмотрим моно-, сескви- и дитерпеноиды, которые входят в состав природных эфирных масел и горечей.
ЭФИРНЫЕ МАСЛА
Эфирные масла (Olea aetherea) — вещества, имеющие запахи масляную консистенцию. В отличие от жирных масел, эфирные масла испаряются, не оставляя после себя жирного пятна. Эфирные масла — это смесь летучих душистых веществ, образующихся в растениях и относящихся главным образом к кислородсодержащим моно-, ди- и сесквитерпеноидам, реже — к алифатическим или ароматическим (фенольным) соединениям. Из эфирных масел выделено более тысячи углеводородов, альдегидов, спиртов, кетонов, фенолов, лактонов, эфиров. Треть этих веществ и производящие их пряно-ароматические растения используются в фармации и здраво охранении, парфюмерной и косметической, пищевой и ликероводочной про мышленности.
Классификация
В основу классификации эфирных масел и продуцирующихих растений положены вещества, обусловливающие их терапевтическое действие:
- -монотерпеноиды,
- -сесквитерпеноиды,
- ароматические соединения.
Эфирные масла, содержащие монотерпеноиды.
Среди них выделяют:
—алифатические, или ациклические, монотерпеноиды— соединения с тремя двойными связями: мирцен (эфирные масла хмеля, мирта), или с двумя двойными связями: гераниол (в цветкахрозы дамасской, содержание примерно 60 %) и линалоол (в плодах кориандра посевного, содержание около 80 %); —

моноциклические монотерпеноиды — соединения, содержащие скелет ментана. Из кислородсодержащих соединений этого типа в ЛР распространены следующие: ментол (в листьях мяты перечной, содержание примерно 70 %), карвон (в плодах тмина обыкновенного, содержание около 60 %), лимонен (в плодах тмина, лимона, содержание около 30 %), цинеол (в листьях эвкалиптов — серого, шарикового, прутовидного, содержание примерно 80 %);

-бициклические монотерпеноиды— соединения с двумя конденсированными неароматическими кольцами и одной двойной этиленовой связью. У терпенов этого класса выделяют четыре ряда: пинена, карена, камфена (фенхена) и туйена. Кислородпроизводные бициклические терпеноиды очень разнообразны, но для нас наибольший интерес представляют борнеол и камфора, широко используемые в фармации.

Эфирные масла, содержащие сесквитерпеноиды.
К сесквитерпеноидам принадлежат соединения с формулой (С5Н8)3: спирты, кетоны, лактоны и другие вещества, которые представлены в составе растительных эфирных масел не меньше, чем монотерпеноиды. Как и монотерпеноиды, сесквитерпеноиды подразделяют на ациклические, моноциклические, бициклические и трициклические со единения. Изациклических, или алифатических, сесквитерпеноидов отметим фарнезол, найденный в цветках липы, ландыша и других ЛР. Фарнезол является предшественником многих других сесквитерпеноидов, в частности моноциклических (на пример, бисаболола), присутствующих в составе эфирных масел ромашки лекарственной, липы, и бициклических типа кадинена, выявленных в эфирном масле перца душистого и других растений.
К бициклическим сесквитерпеноидам относят и производные азулена (например, хамазулен), имеющие пять двойных связей в конденсированных циклопентановом и циклогептановом кольцах).
Трициклические сесквитерпеноиды также часто имеют основной азуленовый бицикл, например у ледола (компонента эфирного масла багульника болотного) и у аромадендрена (в эфирном масле эвкалипта).

Эфирные масла, содержащие ароматические соединения. Из ароматических соединений в эфирных маслах ЛР встречаются, как правило, их кислородсодержащие производные: фенолы (тимол, карвакрол— в цветках и листьях тимьяна обыкновенного, чабреца, душицы), фенольные эфиры (анетол— в плодах аниса, фенхеля), ароматические альдегиды (бензальдегид— в траве тимьяна, плодах аниса). Разные виды растений имеют неодинаковые эфирные масла, даже в одном растении различные органы содержат разные масла.

Распространение эфирных масел в лекарственных растениях
Эфирные масла встречаются в растениях более 90 семейств: в тропиках— в 44 % ЛР от всех эфиромасличных растений, субтропиках— 10 %, в умеренной зоне — 30 %. В мире известно свыше 3000 видов эфиромасличных растений, в странах СНГ произрастает более 1000 видов. Эфирных масел много у растений семейств: Валериановые, Сельдерейные, Астровые, Вересковые, Губоцветные (Яснотковые), Миртовые, Сосновые.
Физиологические условия, оптимальные для образования эфирных масел в растениях
Эти условия изучены недостаточно. На накопление эфирных масел и их качественный состав влияют фаза вегетации, природные условия (количество солнечных дней, баланс температур, географическая широта, высота над уровнем моря, влажность, почвенно-трофические особенности региона). Известно, что образованию эфирных масел способствуют повышение температуры и кислородное голодание. Вместе с тем неясно, почему в эфирном масле в листьях розмарина, образующемся в течение всего года, синтезируются оптические изомеры, которые имеют только правое вращение, а синтезирующиеся за один месяц (апрель — май) — только левое.
Неизвестны и причины изменения химического состава эфирных масел в ЛР в онтогенезе: например, в листьях кориандра (кинза) эфирное масло имеет неприятный запах, а в зрелых плодах— приятный, что сопровождается увеличением плотности эфирного масла. У ЛР отмечаются колебания образования эфирных масел в зависимости от времени суток (например, наибольшее количество эфирных масел у лаванды образуется во второй половине дня, а у розы — в первой, утром).
Образование, накопление и роль эфирных масел
Эти процессы наблюдаются в различных органах растений: лепестках(роза, жасмин), плодах (сочных — кожура цитрусовых; сухих — анис, тмин, фенхель, кориандр, укроп), корневищах(аир, валериана), древесине (сосна и другие хвойные), но чаще всего в листьях(мята, эвкалипт, шалфей, чабрец). Эфирные масла могут быть диффузно распределены в клеточном соке, но чаще скапливаются в особых образованиях— железках, секреторных клетках, канальцах и вместили щах. Содержание эфирных масел в органах растений колеблется от сотых долей до 5 % (25 % — в бутонах гвоздичного дерева). Роль эфирных масел для жизнедеятельности растений не выяснена. Предполагают, что эфирные масла служат для защиты растений от вредителей и возбудителей болезней, действуя как асептические вещества и способствуя заживлению ран. Однако эфиромасличные растения страдают от инфекционных болезней и вредителей практически в такой же мере, как и другие растения.
По-видимому, эфирные масла участвуют в обменных процессах, протекающих в организме и клетках растений и животных. Об этом свидетельствует высокая реакционная способность терпеноидных соединений, являющихся основными компонентами эфирных масел. Высокая реакционная способность терпеноидов обусловливает и широкое фармакологическое и терапевтическое действие эфирных масел. Основными видами их фармакологической активности являются: раздражающая, отхаркивающая, антисептическая (бактерицидная и инсектицидная), защитно-репарацион ная, спазмолитическая, мочегонная.
Физико-химические свойства эфирных масел
Эфирные масла представляют собой прозрачные или желто-бурые (реже голубые, зеленые или розовые) жидкости с характерным для каждого эфирного масла запахом. Они растворимы в органических растворителях (хлороформ, ацетон, спирт, эфир) и практически не растворимы в воде. Эфирные масла (за исключением гвоздичного масла) легче воды. Температура их кипения — 140—260-С — более высокая, чем у воды. Каждое эфирное масло имеет свою температуру застывания. Они оптически активны и имеют определенный коэффициент преломления. Значения рН эфирных масел в основном нейтральные и кислые. При нанесении на бумагу оставляют жирное пятно, которое постепенно исчезает (в отличие от жирных масел). Горят эфирные масла коптящим пламенем. Хорошо перегоняются с водяным паром. Под действием света в присутствии кислорода быстро окисляются, осмоляются, за густевают, изменяют первоначальный цвет и запах. В связи с этим эфирные масла хранят в запаянных стеклянных ампулах в темноте при температуре не выше 15-Си отдельно от других веществ. Те же предосторожности необходимо соблюдать и при хранении эфиромасличного ЛРС, так как сухие ЛР способны передавать свой запах другим растениям и впитывать чужие запахи.
Извлечение эфирных масел из лекарственного растительного сырья Эфирные масла из ЛР можно получить следующими способами:
- перегонка с водяным паром;
- экстракция эфирных масел легколетучими растворителями;
- экстракция эфирных масел жирами путем настаивания ЛРС. Разновидностью этого метода является анфлераж— поглощение эфирных масел из ЛРС сорбентами (твердыми жирами, активированным углем). Из насыщенного жира эфирные масла извлекаются спиртом: спирт вымораживают, осадочные примеси в эфирном масле отфильтровывают и получают чистые эфирные масла;
- механическое прессование сырья.
Количественное определение содержания эфирных масел в ЛРС
Данный процесс основан на способности эфирных масел перегоняться с водяным паром. Согласно закону парциального давления Рауля в смеси компоненты закипают раньше, чем каждый из них достигает своей температуры кипения. Так, смесь скипидара и воды начинает кипеть и перегоняться при температуре 95,5оС (вместо 160оС — температуры кипения пинена, основного компонента скипидара). Другие эфирные масла кипят при температуре ниже 100оС, хотя точка кипения лимонена 177оС, гераниола 229оС, тимола 233оС. В ГФ РБ (т. 1; п. 2.8.12) описаны пять методов перегонки эфирных масел с водяным паром и количественного определения содержания их в ЛРС.
- Первый метод (в ГФ РБ это метод B) связан с применением аппарата Гинзберга;
- второй, третий и четвертый (в ГФ РБ они описаны как методы А, СиD)—аппарата Клевенджера,
- пятый (в ГФ РБ это метод Е) — с модификацией аппарата Клевенджера.
От первого остальные методы отличаются тем, что в ходе выделения прием ник эфирного масла у нихвынесен из колбы парообразователя и, следовательно, эфирные масла не подвергаются длительному воздействию высокой температуры, как в первом методе. Таким образом, второй, третий, четвертый и пятый методы применяются в случае, когда эфирные масла при перегонке претерпевают изменения или имеют плотность, близкую к 1, и бóльшую. В четвертом методе (в ГФ РБ это метод D) против загустения эфирныхмасел (при образовании их комплекса с водой) используют декалин (растворитель).
