Средства, влияющие на тромбообразование
Фармакология. Учебное пособие — под ред. Аляутдина Р.Н.
- Средства, снижающие агрегацию тромбоцитов (антиагреганты)
- Средства, влияющие на свертывание крови
- Средства, понижающие свертывание крови (антикоагулянты)
- Средства, повышающие свертывание крови
- Средства, влияющие на фибринолиз
- Фибринолитические (тромболитические) средства
- Антифибринолитические средства
Глава 27. СРЕДСТВА, ВЛИЯЮЩИЕ НА ТРОМБООБРАЗОВАНИЕ
Образование тромбов является защитной реакцией, которая обеспечивает остановку кровотечения (гемостаз) при повреждении сосудистой стенки. После повреждения сосудистой стенки возникает спазм сосудов. Эта немедленная реакция на травму может остановить кровотечение только при незначительных повреждениях мелких сосудов. В основном гемостаз достигается благодаря образованию тромбов (гемостатических пробок), которые закрывают просвет поврежденного сосуда и таким образом препятствуют кровопотере. Частой причиной образования тромбов могут быть патологические изменения эндотелия, включая его повреждения, связанные с атеросклерозом сосудов.
Тромбообразование происходит при участии двух основных процессов — агрегации тромбоцитов и свертывания крови (гемокоагуляции).
Агрегация тромбоцитов — это объединение тромбоцитов в конгломераты (агрегаты) разной величины и плотности. Этот процесс инициируется при повреждении сосудистой стенки. В месте повреждения тромбоциты связываются с фактором Виллебранда и с коллагеном субэндотелиального слоя, что стимулирует их агрегацию. При этом сами тромбоциты становятся источниками веществ, стимулирующих агрегацию, таких как тромбоксан А2, АДФ, серотонин. Тромбин, который высвобождается из тромбоцитов и образуется локально в процессе свертывания крови, также является индуктором агрегации тромбоцитов. Кроме того, агрегацию индуцируют катехоламины, фактор активации тромбоцитов и некоторые другие эндогенные вещества.
Агрегации тромбоцитов препятствуют простациклин и эндотелиальный релаксирующий фактор, которые образуются клетками эндотелия сосудов и высвобождаются в кровоток. Однако при повреждении эндотелиальных клеток синтез этих веществ снижается и на таком фоне действие веществ, стимулирующих агрегацию, становится доминирующим. В результате тромбоциты объединяются в агрегаты, из которых формируется тромбоцитарный тромб.
Тромбоцитарный тромб становится более прочным благодаря нитям фибрина, который образуется в процессе свертывания крови. Основными участниками этого процесса являются белки плазмы крови, называемые факторами свертывания крови.
Плазменные факторы свертывания синтезируются в печени и циркулируют в крови в неактивной форме. При повреждении сосудистой стенки происходит быстрая активация фактора VII при участии тканевого фактора, который синтезируется эндотелиальными клетками, но в норме не контактирует с кровью. Экспрессия тканевого фактора на поверхности поврежденных эндотелиальных клеток значительно ускоряет активацию фактора VII (образование фактора Vila) в присутствии ионов Са2+. Под действием фактора Vila происходит последовательная активация других факторов свертывания крови (IX и X) в сложной аутокаталитической системе, называемой каскадом свертывания крови. В результате образуется тромбин (фактор Па), который превращает .циркулирующий в крови растворимый белок фибриноген (фактор I) в нерастворимый фибрин. Фибрин заполняет пространство между тромбоцитами и укрепляет тромбоцитарный тромб. Фибриновые нити образуют сеть, которая задерживает циркулирующие в крови эритроциты. Формируется так называемый красный тромб.
Свертыванию крови противодействуют вещества, которые являются естественными ингибиторами факторов свертывания крови. Активации фактора X под действием фактора Vila препятствует ингибитор пути тканевого фактора, синтезируемый эндотелиальными клетками. Ингибитором тромбина и некоторых других факторов свертывания (за исключением фактора VII) является антитромбин III -белок плазмы крови, действующий в комплексе с гепарином. Эти вещества являются компонентами противосвертывающей системы, которая способствует поддержанию крови в жидком состоянии даже при локальном образовании тромбов в месте повреждения сосуда.
Агрегация тромбоцитов и свертывание крови — взаимосвязанные процессы. Преобладание того или иного процесса в механизме тромбообразования зависит от калибра сосуда и скорости кровотока. Агрегация тромбоцитов имеет большее значение для формирования тромбов при высокой скорости кровотока, т.е. в артериях. В венозных сосудах, где скорость кровотока невелика, преобладает процесс свертывания крови.
Последующая судьба образовавшегося тромба зависит от активности фибринолитической системы. Если эта система функционирует нормально, происходит постепенное растворение фибрина (фибринолиз) при участии фермента плазмина (фибринолизина), который образуется из неактивного плазминогена под
влиянием активаторов плазминогена. Действию плазмина препятствуют циркулирующие в крови антиплазмины. Активаторы плазминогена нейтрализуются специфическими ингибиторами.
Нарушение процессов агрегации тромбоцитов и свертывания крови, а также повышение активности фибринолитической системы могут привести к кровоточивости, а чрезмерная активация этих процессов или угнетение фибринолиза — к возникновению тромбов (тромбозу). В результате тромбоза артериальных сосудов уменьшается приток крови к тканям, развивается ишемия тканей. Следствием ишемии является гибель клеток — некроз. Тромбозы могут быть причиной таких тяжелых осложнений, как инфаркт миокарда (тромбоз коронарных артерий), ишемический инсульт (тромбоз сосудов мозга) и т.д. Венозные тромбозы могут быть причиной эмболии легочной артерии.
Для предупреждения тромбозов используют вещества, которые ингибируют агрегацию тромбоцитов и свертывание крови и таким образом препятствуют образованию тромбов. Кроме того, при тромбозах используют вещества, которые вызывают лизис образовавшихся тромбов — тромболитические (фибринолитические) средства.
Для остановки кровотечений в основном применяют средства, повышающие свертывание крови и средства, угнетающие фибринолиз. Выбор тех или иных средств зависит от причины возникновения кровотечения.
Практическое значение имеют следующие группы средств, влияющих на тромбообразование.
Средства, снижающие агрегацию тромбоцитов (антиагреганты).
Средства, влияющие на свертывание крови:
- средства, понижающие свертывание крови (антикоагулянты);
- средства, повышающие свертывание крови (гемостатики). Средства, влияющие на фибринолиз:
- фибринолитические (тромболитические средства);
- антифибринолитические средства (ингибиторы фибринолиза).
27.1. СРЕДСТВА, СНИЖАЮЩИЕ
АГРЕГАЦИЮ ТРОМБОЦИТОВ (АНТИАГРЕГАНТЫ)
Тромбоциты — это небольшие по размеру (в среднем 3,6 мкм в диаметре) форменные элементы крови дисковидной формы, которые образуются как фрагменты мегакариоцитов костного мозга. Тромбоциты циркулируют в крови в течение 6-12 дней, а затем захватываются тканевыми макрофагами. Кроме того, 15-25% тромбоцитов ежесуточно поглощается эндотелиальными клетками. Эндотелий сосудов оказывает влияние на функциональную активность тромбоцитов. Эндотелиальные клетки выделяют в кровоток простациклин (простагландин 12) и эндотелиальный релаксирующий фактор (ЭРФ), который идентифицируют с оксидом азота — N0. Эти вещества препятствуют агрегации тромбоцитов. Кроме того, эндотелиальные клетки секретируют вещества, уменьшающие свертывание крови и способствующие лизису тромба. Все это обеспечивает антитромбогенные свойства неповрежденного эндотелия сосудов.
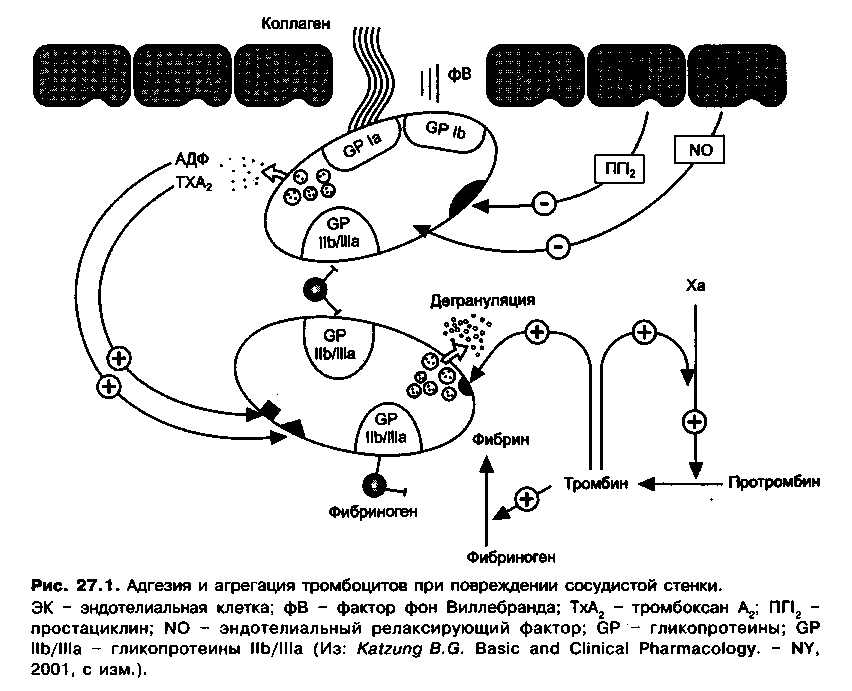
При повреждении эндотелия сосудов, которое может быть вызвано различными факторами (включая механическую травму, инфекции, атеросклеротические изменения сосудистой стенки и др.), антитромбогенные свойства эндотелия снижаются и создаются условия для формирования тромба. В частности, нарушается синтез простациклина и ЭРФ и это облегчает контакт тромбоцитов с поврежденной поверхностью эндотелия. Тромбоциты скапливаются в месте повреждения и начинают взаимодействовать с субэндотелием сосудов: связываются с белками субэндотелия — фактором Виллебранда и коллагеном при участии специфических гликопротеинов, локализованных в мембране тромбоцитов. Этот процесс носит название адгезии. Фактор Виллебранда связывается с гликопротеином lb, а коллаген — с гликопротеином 1а тромбоцитарной мембраны (рис. 27.1).
Воздействие коллагена (а также тромбина, который в небольших количествах образуется локально уже на начальном этапе тромбообразования) на тромбоциты вызывает изменение их состояния, которое называют активацией. Тромбоциты меняют свою форму — из дисковидных они становятся распластанными с множеством отростков (псевдоподий) и таким образом покрывают поврежденную поверхность сосуда. При активации из тромбоцитов высвобождаются различные биологически активные вещества. Эти вещества в неактивированных тромбоцитах находятся в гранулах (альфа-гранулы, плотные гранулы). Плотные гранулы являются хранилищем веществ, стимулирующих агрегацию тромбоцитов — АДФ и серотонина. Высвобождение этих веществ из тромбоцитарных гранул происходит в результате повышения внутриклеточной концентрации Са2+ при действии на тромбоциты коллагена, тромбина и других индукторов агрегаций, в том числе и самого АДФ. Высвобождаемый в кровоток АДФ стимулирует специфические -(пуринергические) рецепторы, локализованные в мембране тромбоцитов. Через рецепторы, связанные с Gj-белками, АДФ вызывает угнетение аденилатциклазы и снижение уровня цАМФ, что приводит к повышению уровня Са2+ в цитоплазме тромбоцитов.
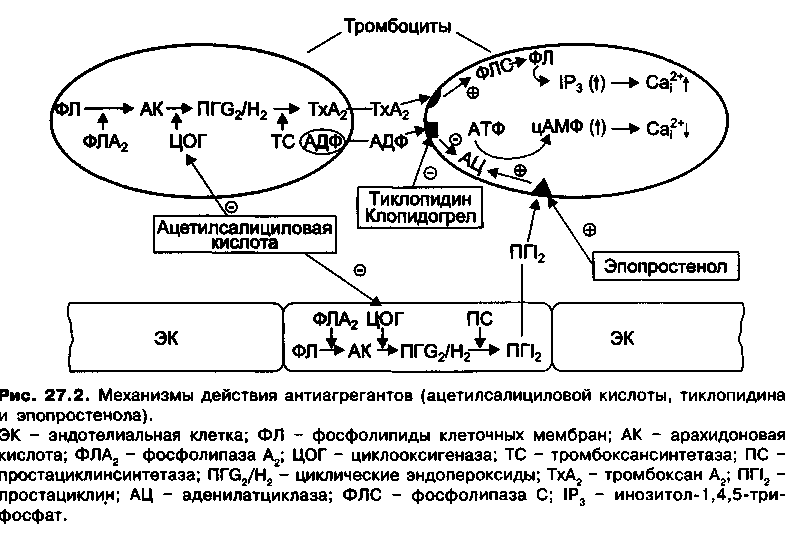
При активации тромбоцитов повышается активность фосфолипазы А2 тромбоцитарных мембран — фермента, который участвует в образовании арахидоновой кислоты из мембранных фосфолипидов. В тромбоцитах из арахидоновой кислоты под влиянием циклооксигеназы сначала синтезируются циклические эндопероксиды (простагландины G2/H2), а из них при участии тромбоксансинтетазы образуется тромбоксан А — активный стимулятор агрегации тромбоцитов и вазоконстриктор. После высвобождения в кровоток тромбоксан А2 стимулирует тромбоксановые рецепторы в мембране тромбоцитов. В результате через связанные с этими рецепторами Q-белки активируется фосфолипаза С и увеличивается образование инозитол-1,4,5-трифосфата (1Р3), который способствует высвобождению Са2+ из кальциевого депо тромбоцитов (роль кальциевого депо в тромбоцитах выполняет система плотных трубочек).
Это приводит к увеличению цитоплазматической концентрации Са2+ (рис. 27.2). Тромбоксан А2 также вызывает повышение концентрации Са2+ в гладкомышечных клетках сосудов, что является причиной вазоконстрикции.
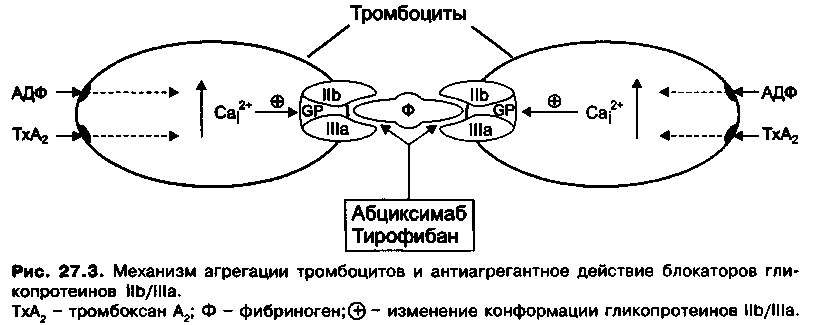
Таким образом, АДФ и тромбоксан А2 повышают уровень Са2+ в цитоплазме тромбоцитов. Цитоплазматический Са2+ вызывает изменение конформации гликопротеинов IIb/IIIа в мембране тромбоцитов, в результате чего они приобретают способность связывать фибриноген. Одна молекула фибриногена имеет два участка связывания для гликопротеинов IIb/IIIа и таким образом может объединить между собой два тромбоцита (рис. 27.3). Объединение многих тромбоцитов фибриногеновыми мостиками приводит к образованию тромбоцитарных агрегатов.
Противоположным образом на агрегацию тромбоцитов влияет простациклин (простагландин I2). Так же, как и тромбоксан, простациклин образуется из циклических эндопероксидов. В отличие от тромбоксана для превращения циклических эндопероксидов в простациклин необходима простациклинсинтетаза. Простациклин синтезируется эндотелиальными клетками и высвобождается в кровоток, где стимулирует простациклиновые рецепторы в мембране тромбоцитов и связанную с ними через выбелок аденилатциклазу.
В результате в тромбоцитах повышается уровень цАМФ и снижается концентрация цитоплазматического Са2+ (см. рис. 27.2). Это препятствует изменению конформации гликопротеинов IIb/IIIа и они утрачивают способность связывать фибриноген. Таким образом, простациклин предупреждает агрегацию тромбоцитов. Под действием простациклина также снижается концентрация Са2+ в гладкомышечных клетках сосудов, что приводит к расширению сосудов.
Можно упрощенно выделить следующую последовательность основных событий, которые приводят к агрегации тромбоцитов (см. схему 27.1).

Основная направленность действия антиагрегантов, которые в настоящее время применяют в клинической практике, в основном связана с устранением действия тромбоксана А^ и АДФ, а также с блокадой гликопротеинов ПЬ/Ша мембран тромбоцитов. Используют также вещества, которые действуют другим образом, в частности, повышают концентрацию цАМФ в тромбоцитах и, следовательно, снижают в них концентрацию Са2+. Могут быть выделены следующие группы средств, уменьшающих агрегацию тромбоцитов.
Средства, ингибирующие синтез тромбоксана А2
а) ингибиторы циклооксигеназы
Ацетилсалициловая кислота
б) ингибиторы циклооксигеназы и тромбоксансинтетазы
Индобуфен
Средства, стимулирующие простациклиновые рецепторы
Эпопростенол
Средства, препятствующие действию АДФ на тромбоциты
Тиклопидин, Клопидогрел
Средства, ингибирующие фосфодиэстеразу тромбоцитов
Дипиридамол
Средства, блокирующие гликопротеины Ilb/IIIa мембран тромбоцитов
а) моноклональные антитела
Абциксимаб
б) синтетические блокаторы гликопротеинов ПЬ/Ша
Эптифибатид, Тирофибан
Ацетилсалициловая кислота (Аспирин) — известное противовоспалительное, анальгетическое и жаропонижающее средство — в настоящее время широко применяется в качестве антиагреганта. Антиагрегантное действие ацетилсалициловой кислоты связывают с ее ингибирующим влиянием на синтез тромбоксана А2 в тромбоцитах.

Ацетилсалициловая кислота необратимо ингибирует циклооксигеназу (вызывает необратимое ацетилирование фермента), и таким образом нарушает образование из арахидоновой кислоты циклических эндопероксидов, предшественников тромбоксана А2 (см. рис. 27.2), при этом уменьшается не только синтез тромбоксана А2 в тромбоцитах, но и синтез простациклина в эндотелиальных клетках сосудов. Однако путем подбора соответствующих доз и режима дозирования можно добиться преимущественного действия ацетилсалициловой кислоты на синтез тромбоксана А2. Это связано с существенными различиями между тромбоцитами и эндотелиальными клетками.
Тромбоциты — безъядерные клетки — не имеют системы ресинтеза белка и, следовательно, не способны синтезировать циклооксигеназу. Поэтому при необратимом ингибировании циклооксигеназы нарушение синтеза тромбоксана А2 сохраняется на протяжении всей жизни тромбоцита — в течение 7-10 дней. Однако вследствие образования новых тромбоцитов антиагрегантное действие ацетилсалициловой кислоты продолжается меньший период времени и для достижения стабильного эффекта препарата его рекомендуют назначать 1 раз в сутки.
В клетках эндотелия происходит ресинтез циклооксигеназы, вследствие чего ее активность восстанавливается уже через несколько часов после необратимого ингибирования ацетилсалициловой кислотой. Поэтому при назначении препарата 1 раз в сутки не происходит существенного снижения синтеза простациклина.
Кроме того, ацетилсалициловая кислота приблизительно на 30% подвергается пресистемному метаболизму в печени, вследствие чего ее концентрация в системном кровотоке ниже, чем в портальной крови. В результате на тромбоциты, циркулирующие в портальном кровотоке, ацетилсалициловая кислота действует в более высоких концентрациях, чем на эндотелиальные клетки системных сосудов. Поэтому для подавления синтеза тромбоксана \ в тромбоцитах необходимы меньшие дозы ацетилсалициловой кислоты, чем для подавления синтеза простациклина в клетках эндотелия. При увеличении дозы ацетилсалициловой кислоты ее угнетающее действие на синтез простациклина становится более выраженным, что может привести к уменьшению антиагрегантного эффекта препарата. В связи с указанными особенностями ацетилсалициловую кислоту в качестве антиагреганта рекомендуют назначать в небольших дозах (обычно 100 мг) 1 раз в сутки.
Как антиагрегант ацетилсалициловая кислота используется для профилактики инфаркта миокарда, при нестабильной стенокардии, для профилактики ишемического инсульта и тромбозов периферических сосудов, при аортокоронарном шунтировании и коронарной ангиопластике. Ацетилсалициловую кислоту назначают внутрь в дозах 75—325 мг 1 раз в сутки на протяжении длительного времени. В настоящее время в распоряжении врачей имеются препараты ацетилсалициловой кислоты, предназначенные для профилактики тромбозов, которые содержат 50—325 мг действующего вещества — Аспирин кардио, Буферин, Новандол, Тромбо АСС и др.
Основные побочные эффекты ацетилсалициловой кислоты связаны с угнетением циклооксигеназы. При этом нарушается образование простагландинов Е2 и 12 (простациклина), которые оказывают гастропротекторное действие. В результате даже при непродолжительном применении ацетилсалициловая кислота может вызвать повреждение эпителия желудка и двенадцатиперстной кишки (ульцерогенный эффект). При применении ацетилсалициловой кислоты возможны желудочно-кишечные кровотечения и другие геморрагические осложнения. Избирательное ингибирование циклооксигеназы приводит к активации липоксигеназного пути превращения арахидоновой кислоты и образованию лейкотриенов, обладающих бронхоконстрикторными свойствами. У больных бронхиальной астмой ацетилсалициловая кислота может провоцировать начало приступа («аспириновая астма»). Возможны аллергические реакции.
Индобуфен (Ибустрин) уменьшает синтез тромбоксана А2 вследствие одновременного ингибирования циклооксигеназы и тромбоксансинтетазы. В отличие от ацетилсалициловой кислоты индобуфен вызывает обратимое ингибирование циклооксигеназы. При приеме этого препарата наблюдается относительное увеличение количества простациклина (увеличивается соотношение простациклин/тромбоксан А2). Индобуфен подавляет адгезию и агрегацию тромбоцитов. Показания к применению и побочные эффекты такие же, как у ацетилсалициловой кислоты.
Еще один путь уменьшения агрегации тромбоцитов — стимуляция простациклиновых рецепторов. С этой целью используют препарат простациклина Эпопростенол. Действие простациклина противоположно действию тромбоксана А2 не только на тромбциты, но и на тонус сосудов. Он вызывает вазодилатацию и снижение артериального давления. Этот эффект простациклина используется при легочной гипертензии. Так как простациклин быстро разрушается в крови (t около 2 мин) и поэтому действует непродолжительно, препарат вводят инфузионно. Из-за короткого действия эпопростенол не нашел широкого применения в качестве антиагреганта. Возможная область использования антиагрегантного действия эпопростенола — профилактика агрегации тромбоцитов при экстракорпоральном кровообращении.
Тиклопидин (Тиклид) — производное тиенопиридина, ингибирует агрегацию тромбоцитов, вызываемую АДФ. Антиагрегантный эффект тиклопидина связан с образованием активного метаболита, который необратимо и селективно нарушает взаимодействие АДФ с рецепторами в мембране тромбоцитов. Это приводит к устранению стимулирующего действия АДФ на тромбоциты и снижению в них концентрации цитоплазматического Са2+ (см. рис. 27.2). В результате не изменяется конформация гликопротеинов НЬ/Ша в мембране тромбоцитов и нарушается их связывание с фибриногеном.

Максимальный эффект при постоянном приеме тиклопидина достигается через 3-7 дней (время, необходимое для действия активного метаболита) и после отмены препарата сохраняется весь период жизни тромбоцитов (7-10 дней). Тиклопидин назначают при нестабильной стенокардии, для профилактики инфаркта миокарда и ишемического инсульта, для предупреждения тромбоза при аортокоронарном шунтировании, ангиопластике, атеросклерозе периферических артерий. Препарат эффективен при приеме внутрь, назначают 2 раза в сутки во время еды.
Применение тиклопидина ограничивается его побочными эффектами. Возможны снижение аппетита, тошнота, рвота, диарея (20%), боли в животе, кожные высыпания (11—14%). Отмечается повышение в плазме крови уровня атерогенных липопротеинов. Кровоточивость является общим осложнением при применении антиагрегантов. Опасным осложнением является нейтропения, которая встречается по разным данным у 1—2,4% больных, получавших тиклопидин в течение первых трех месяцев лечения. Возможны тромбоцитопения, агранулоцитоз, очень редко — апластическая анемия. В связи с этим при применении тиклопидина необходим систематический контроль крови.
Клопидогрел (Плавике) сходен с тиклопидином по химической структуре, основным эффектам и механизму действия. Так же, как тиклопидин, является пролекарством и метаболизируется в печени с образованием активного метаболита. Значимое ингибирование агрегации тромбоцитов отмечается со второго дня лечения, максимальный эффект достигается через 4-7 дней. После отмены препарата действие его сохраняется в течение 7-10 дней. Клопидогрел превосходит тиклопидин по активности — в суточной дозе 75 мг он вызывает такое же снижение агрегации тромбоцитов и удлинение времени кровотечения, что и тиклопидин в суточной дозе 500 мг. Применяется клопидогрел в основном по тем же показаниям, что тиклопидин и ацетилсалициловая кислота, принимают внутрь 1 раз в день независимо от приема пищи. По сравнению с тиклопидином побочные эффекты клопидогрела выражены в меньшей степени (диарея — 4,5%, сыпь -6%). Применение клопидогрела сопряжено с меньшим риском возникновения такого серьезного осложнения, как нейтропения (0,1%).
Дипиридамол (Курантил, Персантин) вначале был предложен как коронарорасширяющее средство. Позже была выявлена его способность угнетать агрегацию тромбоцитов. В настоящее время дипиридамол применяется в основном в качестве антиагреганта для профилактики тромбозов. Антиагрегантное действие

тате чего в них снижается концентрация цитоплазматического Са2+. Происходит это по нескольким причинам. В частности, дипиридамол ингибирует фосфодиэстеразу, которая инактивирует цАМФ. Кроме того, дипиридамол угнетает захват аденозина эндотелиальными клетками и эритроцитами и его метаболизм (угнетает фермент аденозиндезаминазу) и тем самым повышает уровень аденозина в крови (рис. 27.4). Аденозин стимулирует А2-рецепторы тромбоцитов и повышает активность связанной с этими рецепторами аденилатциклазы, в результате в тромбоцитах увеличивается образование цАМФ и снижается уровень цитоплазматического Са2+. Дипиридамол также повышает уровень цАМФ в гладкомышечных клетках сосудов, вследствие чего вызывает вазорелаксацию.
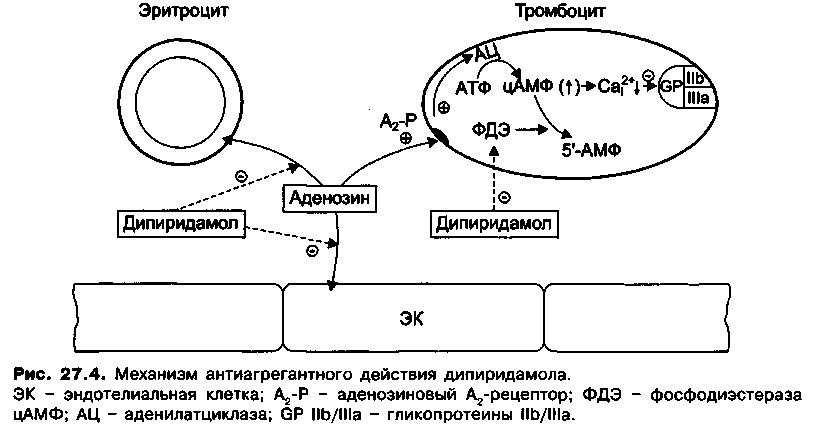
Применяют дипиридамол для профилактики инфаркта миокарда и ишемического инсульта, а также при заболеваниях периферических артерий. Назначают внутрь 3—4 раза в день за 1 ч до приема пищи. При применении дипиридамола возможны головная боль, головокружение, артериальная гипотензия, диспептические явления, кожные сыпи. Опасность кровотечений меньше, чем при применении ацетилсалициловой кислоты. Дипиридамол противопоказан при стенокардии напряжения (возможен «синдром обкрадывания»).
Пентоксифиллин (Агапурин, Трентал) так же, как дипиридамол, ингибирует фосфодиэстеразу и повышает уровень цАМФ. В результате в тромбоцитах снижается уровень цитоплазматического Са2+. Это приводит к уменьшению агрегации тромбоцитов. Пентоксифиллин обладает и другими свойствами — повышает деформируемость эритроцитов, снижает вязкость крови, оказывает сосудорасширяющее действие и таким образом улучшает микроциркуляцию.
Пентоксифиллин применяют при нарушениях мозгового кровообращения, расстройствах периферического кровообращения различного генеза, сосудистой патологии глаз (см. гл. 23). В качестве побочных эффектов отмечают диспептические явления, головокружение, покраснение лица. Возможны понижение артериального давления, тахикардия, аллергические реакции, кровотечения. Так же, как дипиридамол, может провоцировать приступы при стенокардии напряжения.
Относительно недавно появилась принципиально новая группа антиагрегантов, которые непосредственно взаимодействуют с гликопротеинами ПЬ/Ша мембран тромбоцитов, нарушая их связывание с фибриногеном.
Первый препарат из этой группы — абциксимаб (РеоПро) представляет собой «химерные» мышиные/человеческие моноклональные антитела (Fab-фрагмент мышиных антител к гликопротеинам ПЬ/Ша, соединенный с Fc-фрагментом иммуноглобулина человека). Абциксимаб неконкурентно ингибирует связывание фибриногена с гликопротеинами Hb/IIIa в мембране тромбоцитов и таким образом нарушает их агрегацию (см. рис. 27.3).Агрегация тромбоцитов нормализуется через 48 ч после однократного введения. Препарат вводят внутривенно (в виде инфузии)
для профилактики тромбоза при ангиопластике коронарных артерий, в ряде случаев при нестабильной стенокардии для профилактики инфаркта. При применении препарата могут возникнуть кровотечения, в том числе внутренние (желудочно-кишечные, внутричерепные, в мочеполовых путях), тошнота, рвота, гипотензия, брадикардия, аллергические реакции вплоть до анафилактического шока, тромбоцитопения.
Поиски препаратов с таким же механизмом действия, но с менее выраженными аллергенными свойствами привели к созданию синтетических блокаторов гликопротеинов IIb/IIIa. На основе барборина (пептид, выделенный из яда карликовой гремучей змеи) был получен препарат эптифибатид (Интегрилин), который конкурентно вытесняет фибриноген из связи с рецепторами и таким образом нарушает агрегацию тромбоцитов. Препарат вводят внутривенно в виде инфузии; антиагрегантный эффект наступает в течение 5 мин и исчезает через 4-6 ч после прекращения инфузии. Препарат рекомендован для профилактики инфаркта миокарда, при нестабильной стенокардии, при чрескожной коронарной ангиопластике. Опасным осложнением при применении эптифибатид а являются кровотечения, возможна тромбоцитопения.
Тирофибан (Аграстат) — непептидный блокатор гликопротеинов ПЬ/Ша. Как и эптифибатид, тирофибан блокирует гликопротеиновые ПЬ/Ша рецепторы конкурентно. Вводят препарат внутривенно (инфузионно). Скорость наступления эффекта, продолжительность действия и показания к применению такие же, как у эптифибатида. Побочные эффекты — кровотечения, тромбоцитопения.
Чтобы расширить возможности применения препаратов этой группы, были созданы блокаторы гликопротеинов ПЬ/Ша, эффективные при введении внутрь -ксемилофибдн, сибрафибан и др. Сибрафибан представляет собой пролекарство и превращается в активное вещество в результате двух ферментативных реакций. В настоящее время эти препараты проходят клинические испытания.
27.3. СРЕДСТВА, ВЛИЯЮЩИЕ НА ФИБРИНОЛИЗ
При образовании тромбов происходит активация фибринолитической системы, которая обеспечивает растворение (лизис) фибрина и разрушение тромба. Это приводит к восстановлению нормального кровотока.
В процессе фибринолиза происходит превращение неактивного плазминогена в плазмин (фибринолизин) при участии активаторов плазминогена. Плазмин гидролизует фибрин с образованием растворимых пептидов. Плазмин не обладает специфичностью и вызывает также разрушение фибриногена и некоторых других факторов свертывания крови. Это повышает риск развития кровотечений. Плазмин, циркулирующий в крови, быстро инактивируется а2-антиплазмином и другими ингибиторами и поэтому в норме не оказывает системного фибринолитического действия. Однако при определенных патологических состояниях или применении фибринолитических средств возможна чрезмерная активация системного фибринолиза, что может стать причиной кровотечений.
27.3.1. Фибринолитические (тромболитические) средства
Фибринолитические средства применяют для растворения образовавшихся тромбов при коронарном тромбозе (остром инфаркте миокарда), тромбозе глубоких вен, остром тромбозе периферических артерий, тромбоэмболии легочной артерии.
В качестве фибринолитических средств применяют препараты, которые активируют плазминоген: препараты стрептокиназы, препарат тканевого активатора плазминогена, препараты урокиназы.
Препараты стрептокиназы
Стрептокиназа (Целиаза, Авелизин, Стрептаза, Кабикиназа) — высокоочищенный белковый препарат, получаемый из культуры б-гемолитического стрептококка. Стрептокиназа приобретает протеолитическую активность только в комплексе с плазминогеном. При введении стрептокиназы образуется эквимолярный комплекс стрептокиназа — плазминоген, который превращает плазминоген в плазмин. Действие стрептокиназы на плазминоген проявляется как в тромбе, так и в плазме крови.
Стрептокиназу вводят внутривенно капельно при остром инфаркте миокарда, вызванном тромбозом коронарных сосудов (наиболее эффективна первые 3—6 ч), при тромбозе глубоких вен, тромбоэмболии легочной артерии, тромбозах сосудов сетчатки. Дозируют стрептокиназу в ME (международных единицах).
Частым осложнением при применении стрептокиназы являются кровотечения, которые могут быть связаны как с активацией плазминогена, циркулирующего в крови (образующийся плазмин разрушает фибриноген — в результате снижается агрегация тромбоцитов), так и с растворением физиологических тромбов. Возможны тошнота, рвота, артериальная гипотензия. Вследствие антигенных свойств стрептокиназа может вызвать аллергические реакции, включая анафилактический шок. Опасность их возрастает при повторном введении препарата. Циркулирующие в крови антитела могут инактивировать стрептокиназу и снижать эффективность терапии.
Существует препарат стрептокиназы пролонгированного действия — стрептодеказа. Продолжительность фибринолитического действия стрептодеказы составляет 48-72 ч.
Анистреплаза (Эминаза) представляет собой комплекс стрептокиназы с ацилированным лизин-плазминогеном. Ацильная группа в молекуле плазминогена закрывает его каталитический центр, что препятствует активации плазминогена. Препарат является пролекарством и после отщепления ацильной группы приобретает способность превращать плазминоген в плазмин. Скорость деацилирования и, следовательно, скорость образования активного препарата зависит от характера ацильной группы и может составлять от 40 мин до нескольких часов. Анистреплазу вводят внутривенно. После однократного введения фибринолитический эффект сохраняется 4—6 ч. Показания к применению и побочные эффекты такие же, как у стрептокиназы.
Препараты тканевого активатора плазминогена и урокиназы
Тканевой активатор плазминогена и урокиназа являются основными физиологическими активаторами плазминогена. Тканевой активатор плазминогена продуцируется эндотелиальными клетками и вызывает частичный протеолиз плазминогена, в результате чего превращается в плазмин. Отличительной особенностью тканевого активатора является высокое сродство к фибрину, который в сотни раз ускоряет его действие на плазминоген. В результате тканевой активатор с большей скоростью активирует те молекулы плазминогена, которые адсорбированы на нитях фибрина. Таким образом, действие тканевого активатора плазминогена ограничивается фибрином тромба. Попадая в кровоток, тканевой активатор связывается со специфическим ингибитором и поэтому мало действует на циркулирующий в крови плазминоген, а также в меньшей степени снижает уровень фибриногена.
Для клинического использования получен рекомбинантный препарат тканевого активатора плазминогена алтеплаза (Активаза, Актилизе). Препарат вводят внутривенно при остром инфаркте миокарда, вызванном тромбозом коронарных сосудов (эффективен в первые 6—12 ч), при тромбоэмболии легочной артерии. Быстро метаболизируется в печени (t 5—10 мин).
Несмотря на то, что алтеплаза мало действует на циркулирующий в крови плазминоген, при ее применении часто возникают геморрагические осложнения. В отличие от стрептокиназы не обладает антигенными свойствами.
Урокиназа образуется клетками почек, обнаружена в моче. В почках образуется одноцепочечная урокиназа (проурокиназа), которая под действием плазмина превращается в активную форму — двухцепочечную урокиназу. Двухцепочечная урокиназа оказывает прямое активирующее действие на плазминоген (не требуется образования комплекса с плазминогеном). Препарат двухцепочечной урокиназы получают из культуры эмбриональных клеток почек человека. Применяют при остром инфаркте миокарда, венозном и артериальном тромбозах, тромбоэмболии легочной артерии. Вводят внутривенно. Дозируют в ME (международных единицах). В сравнении с тканевым активатором плазминогена урокиназа в большей степени действует на циркулирующий в крови плазминоген, в результате образующийся в крови плазмин вызывает распад фибриногена — снижается агрегация тромбоцитов. Основными побочными эффектами являются кровотечения. Не обладает антигенными свойствами.
Получен рекомбинантный препарат одноцепочечной урокиназы (проурокиназы) саруплаза, проявляющий большую специфичность по отношению к фибрину тромба, чем урокиназа.
27.3.2. Антифибринолитические средства
Антифибринолитические средства применяют для остановки кровотечений, вызванных повышенной активностью фибринолитической системы, при травмах, хирургических вмешательствах, родах, заболеваниях печени, простатитах, меноррагиях, а также при передозировке фибринолитических средств. Для этих целей используют препараты, которые ингибируют активацию плазминогена или являются ингибиторами плазмина.
т’Аминокапроновая кислота связывается с плазминогеном и препятствует его превращению в плазмин. Кроме того, она препятствует действию плазмина на фибрин. Препарат вводят внутрь и внутривенно. Возможны побочные эффекты — артериальная гипотензия, брадикардия, аритмии, головокружение, тошнота, диарея. Сходным действием обладает аминомети л бензойная кислота (Амбен, Памба).
Транексамовая кислота (Циклокапрон) является ингибитором активации плазминогена. Препарат вводят внутрь и внутривенно. По эффективности превосходит аминокапроновую кислоту, действует более продолжительно. Вызывает диспептические явления (анорексия, тошнота, рвота, диарея), головокружение, сонливость. Возможны кожные аллергические реакции.
Апротинин (Горд оке, Контрикал, Трас ил ол, Ингитрил) ингибирует плазмин и другие протеолитические ферменты. Препарат вводят внутривенно. Побочные эффекты — артериальная гипотензия, тахикардия, тошнота, рвота, аллергические реакции.
Основные препараты
| Международное непатентованное название | Патентованные
(торговые) названия |
Формы выпуска | Информация для пациента |
| Ацетилсалициловая кислота (Acidum acetyl-salicylicum) | Аспирин кардио, Буферин, Новандол, Тромбо АСС | Таблетки по 0,05, 0,1, 0,325 и 0,5 г | 0,1-0,325 г внутрь 1 раз в день, предпочтительно в виде таблеток с кишечнорастворимым покрытием |
| Тиклопидин (Ticlopidinum) | Тиклид | Таблетки по 0,25 г | 0,25 г внутрь 2 раза в день во время еды. С осторожностью применять при нарушениях функции печени или почек, необходим анализ крови в течение первых 3 мес лечения |
| Клопидогрел | Плавике | Таблетки, покрытые оболочкой, по 0,075 г | Внутрь по 1 таблетке 1 раз в день независимо от приема пищи. Избегать приема в течение 1 нед после ишемического инсульта |
| Дипиридамол (Dipyridamolum) | Курантил Персантин | Таблетки, покрытые оболочкой, и драже по 0,025, 0,05 и 0,075 г | 0,025-0,1 г внутрь 3-4 раза в день за 1 ч до еды. У больных стенокардией напряжения возможен приступ стенокардии из-за синдрома обкрадывания. Следует избегать приема производных ксантина, в том числе содержащихся в чае или кофе |
| Эноксапарин-
натрий (Enoxaparinum) |
Клексан | Ампулы по 0,2, 0,4, 0,6, 0,8 мл и 1 мл 10% раствора | 20 мг (0,02) под кожу 1-2 раза в день |
| Гепарин (Heparinum) | Флаконы по 5 мл (в 1 мл — 5000, 10 000 и 20 000 ЕД) | 5000-20 000 ЕД в вену и подкожно | |
| Аценокумарол (Acenocumaro-lum) | Синкумар | Таблетки по 0,002 и 0,004 г | 0,001-0,006 г внутрь 1 раз в день. Следует соблюдать особую осторожность при заболеваниях печени или почек, после недавнего хирургического вмешательства. Препарат противопоказан при беременности и кормлении грудью |
| Стрептокиназа (Streptokinasum) | Целиаза Авелизин Стрептаза Кабикиназа | Ампулы по 250 000-500 000 ЕД (растворяют перед употреблением в 5 мл воды для инъекций и разводят в 500 мл 5% раствора глюкозы) | 250 000-500 000 ЕД внутривенно (капельно) |
| Аминокапро-новая кислота (Acidum amino-capronicum) | Порошок; флаконы по 100 мл 5% раствора | 2,0-3,0 внутрь 3-5 раз в день; 5,0 в вену (капельно) |
