СПЕКТРОСКОПИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Аналитическая химия. Васюкова А., Веденяпина М.– 2019
- 6.1. Основные принципы спектроскопических методов анализа
- 6.2. Методы получения спектров
- 6.3. УФ- и видимая спектроскопия
- ИК-спектроскопия. Поляриметрия. Масс-спектрометрия. Ядерно-магнитный резонанс
6.1. Основные принципы спектроскопических методов анализа
Спектроскопические и другие оптические методы анализа — это большая группа методов, основанных на взаимодействии электромагнитного излучения с веществом. Аналитический сигнал можно получать в различных областях спектрального диапазона (рис. 6.1).
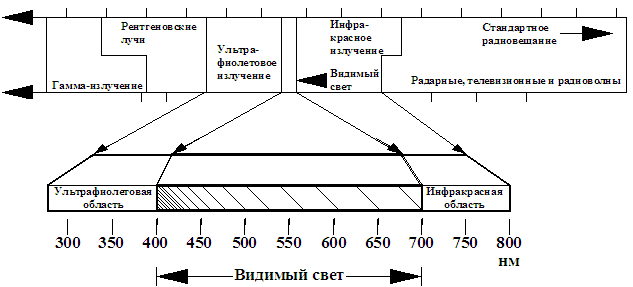
Рис. 6.1. Области спектрального исследования веществ
В зависимости от этого различают следующие виды спектроскопии рентгеновская и оптическая. Оптическая спектроскопия в зависимости от области спектрального диапазона подразделяется на ультрафиолетовую, видимую и инфракрасную. Вещество поглощает энергию излучения и испускает электромагнитное излучение (ЭМИ) только на определенных частотах. Но при получении дополнительной энергии, например при нагревании, ЭМИ может воздействовать на ядра, электроны, атомы или молекулы, вызывая переходы между соответствующими энергетическими уровнями. Спектром называется зависимость степени поглощения или испускания ЭМИ от частоты или от длины волны.
ЭМИ обладает двоякой природой — волновой и корпускулярной. Его можно рассматривать как волну и как частицу (квант). Явления отражения и рассеяния описываются волновой теорией, а поглощение — корпускулярной. Частота ν (Гц) и длина волны λ (нм) связаны между собой соотношением:
ν = c/λ, где с — скорость света.
Используют также величину 1/ λ, называемую волновым числом. В спектрах ультрафиолетовой (УФ) и видимой (vis) областях используют длину волны λ, а в инфракрасной (ИК) — частоту ν или волновое число.
В зависимости от типа взаимодействия излучения с веществом различают спектры испускания и спектры поглощения. Спектры испускания обусловлены переходами частиц с разных энергетических уровней Ei / Ej.
Виды спектров испускания:
- эмиссионные спектры — испускаются термически возбужденными частицами;
- спектры люминесценции — испускаются нетермически возбужденными частицами (под действием энергии электромагнитного излучения, электрического поля, энергии химической реакции).
Спектры поглощения (абсорбционные спектры) обусловлены переходами, при которых Et / Ej. Для анализа наиболее часто используют атомные эмиссионные и молекулярные абсорбционные спектры.
6.2. Методы получения спектров
Атомная спектроскопия. Методы атомной спектроскопии позволяют определить элементный состав исследуемой пробы по спектрам поглощения или испускания излучений возбужденными атомами в оптическом или рентгеновском диапазоне. Например, если раствор поваренной соли внести в пламя газовой горелки, появляется ярко-желтое окрашивание (атомы натрия). Соли лития и рубидия дают ярко-красное окрашивание.
Атомные спектры (рис. 6.2) возникают в результате переходов электронов с одного энергетического уровня на другие. Для каждого элемента характерен свой вид спектра. Спектры атома и иона различаются, так как у них разное электронное строение.

Рис. 6.2. Атомный эмиссионный спектр водорода
Атомные эмиссионные спектры можно получить только при спонтанных (самопроизвольных) электронных переходах в термически возбужденных атомах. Если атомной системе сообщить энергию, то электроны атомов переходят в возбужденное состояние. Через 10 –8с они спонтанно возвращаются в основное состояние. Для получения атомного эмиссионного спектра необходимо:
- атомизировать вещество (перевести его в атомарное состояние) NaCl ↔ Na + Cl;
- возбудить полученные атомы, например Na↔Na.
Энергия, затраченная на возбуждение, должна быть меньше потенциала ионизации, иначе получится спектр иона. Если условия атомизации и возбуждения постоянные, то число возбужденных атомов прямо пропорционально концентрации вещества.
Метод эмиссионной фотометрии пламени. Метод основан на измерении интенсивности света, излучаемого возбужденными частицами (атомами или молекулами) при введении вещества в пламя горелки. Аналитические возможности метода — определение щелочных и щелочноземельных металлов. Они ограничены возможностями источника возбуждения — пламени. Оно обладает меньшей энергией возбуждения, чем другие источники (дуга, искра), поэтому в пламени возбуждаются только элементы с низким потенциалом возбуждения. Пламя — это низкотемпературная равновесная плазма. Основными его характеристиками являются состав и рабочая температура. В состав пламени всегда входят два газа:
- горючий газ — природный газ, метан, пропан, ацетилен;
- газ-окислитель — воздух, кислород, озон, фтор.
Рабочая температура пламени находится в диапазоне 1700–3000 С, зависит от состава горючей смеси и их количественного соотношения. Например, часто используется пламя, имеющее состав природный газ — воздух. Это самая низкотемпературная смесь 1700–1800С.
Анализируемый раствор распыляют в виде аэрозоля в пламя горелки. Возникающее излучение определяемого элемента отделяется от постороннего с помощью светофильтра, попадает на фотоэлемент, вызывает фототок, который измеряется с помощью микроамперметра.
Атомно-эмиссионный спектральный анализ. Этим методом можно определить более 80 элементов. Метод очень чувствителен. Пробу исследуемого вещества нагревают плазмой, электрической дугой или разрядом, что приводит к диссоциации на атомы, которые частично переходят в возбужденное состояние. Время жизни этого состояния 10–7 –10-8 с, затем атомы самопроизвольно возвращаются в нормальное состояние, испуская кванты света, дающие дискретный спектр испускания (эмиссии). Количественный анализ основан на пропорциональной зависимости между интенсивностью излучения и концентрацией элемента. Необходима предварительная калибровка. Источником возбуждения может быть электрическая искра, дуга, аргоновая плазма или пламя. Температура электрической дуги 3000–7000 ºС, искры — 6000–12000 ºС, плазмы — 6000–10000 ºС.
Атомно-абсорбционный эмиссионный анализ. Анализ основан на измерении коэффициента поглощения. Атомы поглощают излучаемые кванты на тех же частотах, на которых испускают. Используется источник излучения с линейчатым спектром — лампа с полым катодом, на который нанесен определяемый элемент. Поэтому спектр излучения источника содержит его линии.
Исследуемое вещество обычно в виде раствора вводится в пламя горелки, где при температуре 2000–3000С происходит диссоциация молекул на атомы. Коэффициент поглощения газообразными атомами подчиняется экспоненциальному закону убывания интенсивности в зависимости от толщины поглощающего слоя и концентрации. Чувствительность атомной абсорбционной спектроскопии превышает чувствительность эмиссионной. Она применяется для анализа многих элементов в различных объектах. Молекулярные спектры, в отличие от атомных, обусловлены:
- электронными переходами;
- колебаниями атомов в молекуле;
- вращением молекулы как целого.
В зависимости от этого различают электронные, колебательные и вращательные молекулярные спектры. Энергия молекулы (Е) складывается из энергии движения электронов (Еэл), энергии колебания атомов (Е кол) в молекуле и энергии вращения молекулы как целого (Евр):
![]()
Электронные спектры наблюдаются в более высокоэнергетических областях спектрального диапазона, а колебательные и вращательные спектры — в области более низких энергий внешнего излучения (табл. 6.1).
Таблица 6.1 Виды молекулярных спектров поглощения

Основной закон светопоглощения (закон Бугера — Ламберта — Бера). Если на слой раствора толщиной l (рис. 6.3) падает световой поток интенсивностью I0, и в результате поглощения света веществом интенсивность прошедшего светового потока I уменьшается, то
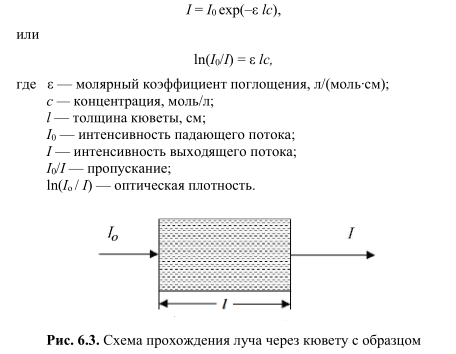
По закону Бугера — Ламберта — Бера оптическая плотность (А) равна A = ε l·с. Коэффициент поглощения (погашения, экстинкции) ε характеризует способность вещества поглощать свет. Величина ε зависит от длины волны падающего света и природы вещества. Условия применимости закона Бугера — Ламберта — Бера:
- раствор должен быть разбавленным (с 0,01 мольл);
- свет должен быть монохроматическим и параллельным;
- не должно протекать побочных химических реакций с участием поглощающих частиц;
- показатель преломления растворов должен быть постоянным;
- температура должна быть постоянной. В зависимости от области оптического диапазона, способа измерения и монохроматичности используемого света существуют различные методы молекулярного абсорбционного анализа.
Фотометрические методы основаны на поглощении света веществом в УФ и видимой областях. Они подразделяются:
- на фотоколориметрию — измерение интенсивности света, прошедшего через окрашенный раствор, фотоэлектрическим способом;
- спектрофотометрию — измерение интенсивности строго монохроматического света, прошедшего через раствор, фотоэлектрическим способом. Наиболее часто используемыми методами анализа являются УФ- и видимая спектроскопия, а также ИК-спектроскопия.
