Заболевания с гепатоцеллюлярными повреждениями
Глава 7. Желтуха и нарушение функции печени
- Вирусные гепатиты
- Гемохроматоз
- Болезнь Вильсона
- Дефицит а1-антитрипсина
- Аутоиммунный хронический активный гепатит
- Алкогольный гепатит
- Повреждение печени лекарственными препаратами
Вирусные гепатиты
Вирусные гепатиты — это общий термин, который имеет отношение к воспалительным процессам в печени, вызванным различными вирусами. Эти вирусы включают вирус гепатита A (HAV), вирус гепатита В (HBV), вирус гепатита С (HCV), вирус гепатита дельта (HDV) и вирус гепатита Е (HEV) (табл. 7.6). Клинические проявления вирусного гепатита весьма вариабельны: от асимптомного течения до ярко выраженной печеночной недостаточности (фульминантная форма). В наиболее легкой форме гепатит протекает либо бессимптомно, либо с грип-позоподобными симптомами, а заболевание идентифицируется только оценкой уровня трансаминаз. Желтуха при вирусном гепатите обычно следует за продромальным периодом, который длится от нескольких дней до нескольких недель, а больные в этом периоде обычно жалуются на слабость, анорексию, тошноту, головные боли, дискомфорт в правом подреберье, субфебрильную температуру. В желтушном периоде пальпируется гладкий, плотный край печени.
Гепатит А — как правило, легко протекающая, самоизлечивающаяся фульминантная форма заболевания, при которой печеночная недостаточность развивается редко, а перехода в хроническую форму не бывает. Передается фекально-оральным путем и имеет инкубационный период до 30 дней. Серологическая идентификация гепатита А включает определение вирус-специфичных антител, представленных IgM (анти-HAV IgM), что способствует диагностике острой или затяжной инфицированности вирусом гепатита А. Больной становится серопозитивным с появлением клинической симптоматики и всегда серопозитивен при наличии желтухи (рис. 7.11). Этот маркер обнаруживается в крови до 120 дней на протяжении всего периода болезни. Вирус-специфичные антитела IgG к гепатиту А не имеют диагностического значения, т. к. появляются на поздних стадиях болезни и определяются в крови в течение нескольких лет после выздоровления.
Гепатит В может быть как острым, так и хроническим заболеванием. Заражение происходит парентеральным путем: при внутривенном введении лекарств, переливании крови, через предметы личной гигиены, а также половым путем. Средний инкубационный период составляет 10 нед. Примерно у 2 % заболевших развивается острая печеночная недостаточность, у 5—10 % заболевание прогрессирует до хронического гепатита. Хронизация гепатита определяется при обнаружении в крови поверхностного антигена (HBsAg) продолжительностью более 6 мес (рис. 7.12). Хронизация гепатита В зависит от возраста больного ко времени инфицирования и состояния его иммунной системы. Хронический гепатит является основным фактором риска для развития гепатоцеллюлярной карциномы. Существует ряд серологических маркеров, помогающих обосновывать диагноз инфицированности вирусом гепатита В, при этом HBsAg сыворотки крови является основным маркером. Появление HBsAg в крови предшествует повышению уровня трансаминаз, а персистенция антигена сохраняется в течение 1 —3 мес при острой инфекции гепатита (рис. 7.13), но примерно у 10 % больных вообще не определяется. Антитела к ядерному антигену (НВсАb) появляются через 2—4 нед вслед за появлением HBsAg.
Между исчезновением HBsAg и появлением специфичных антител к HBsAg (HBsAb) проходит от 3 до 5 мес при острой, самостоятельно купирующейся инфекции, но только НВсАb являются серологическими маркерами, доказывающими перенесенную недавнюю острую инфекцию HBV. ДНК вируса гепатита В (HBV-DNA) и антиген вируса HBcAg могут быть обнаружены в сыворотке при остром гепатите В. Однако эти маркеры используются в оценке хронической инфекции, когда требуются сопоставления с течением репликации и активности вируса.
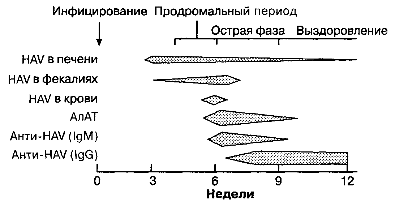
Рис. 7.11. Схема наблюдаемых вариантов сероиммунологических показателей в периоды течения типичной вирусной инфекции гепатита А. В ряде случаев антитела анти-HAV класса IgM могут долго персистировать. Выделение с калом HAV может определяться кратковременно.
Таблица 7.6. Основы дифференциального диагноза вирусных гепатитов
| Признаки | Гепатит А | Гепатит В | Гепатит С | Гепатит D | Гепатит Е |
| Характеристики вирусов | |||||
| Размер | 28 нм | 42 нм | 38-50 нм | 43 нм | 32 нм |
| Нуклеиновая кислота | РНК | ДНК | РНК | РНК | РНК |
| Серологические особенности | |||||
| Маркеры гепатита А | Да | нет | нет | нет | нет |
| Маркеры гепатита В | нет | да | нет | да | нет |
| Маркеры гепатита С | нет | нет | да | нет | нет |
| Маркеры гепатита D | нет | нет | нет | да | нет |
| Маркеры гепатита Е | нет | нет | нет | нет | да |
| РНК вирусная | да | да | да | ||
| Инкубационный период | |||||
| Средний | 30 сут | 75 сут | 50 сут | 75 сут | 40 сут |
| Максимальный | 15-45 сут | 30-180 сут | 15-160 сут | 30-180 сут | 14-60 сут |
| Способ передачи | |||||
| Фекально-оральный | Да | нет | нет | нет | да |
| Парентеральный | редко | Да | Да | да | нет |
| Половой | нет | да | возможно | Да | нет |
| Клиническая картина | |||||
| Пик повышения АлАТ при остром процессе | 800-1000 | 1000-2000 | 300-800 | 1000-1500 | 800-1000 |
| Молниеносная печеночная недостаточность | -0.1 % | -2% | -0.1 % | -5 % при коинфекции -70-90 % при суперинфекции | -2%-20 % при беременности |
| Хронический гепатит | нет | -5-10% -90 % у новорожденных | -50-80 % | -2-5 % при коинфекции -70-90 % при суперинфекции | нет |
| Печеночно-клеточная карцинома | нет | Да | Да | да | нет |
Частицы дельта (HDV) представляют собой неполноценный, ДНК-содержащий вирус, который для своей репликации требует помощи HBV. Поэтому дельта-гепатит имеет место в каждом случае только как сопутствующий острой (коинфекция) или хронической (суперинфекция) инфицированности HBV. Коинфекция и HBV обычно излечимы. Суперинфекция HDV при хроническом гепатите В ассоциируется с увеличением частоты хронического гепатита D с ускоренным развитием на этом фоне цирроза печени. HDV-инфицированность может быть диагностирована серологическим методом путем выявления антител к вирусу гепатита D (анти-HD) у HBsAg-позитивных больных.
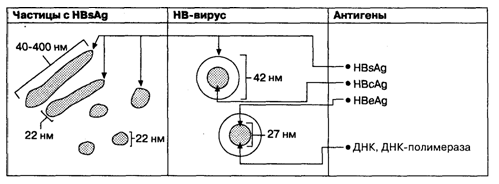
Рис. 7.12. Диаграмма, отражающая соотношения трех морфологических форм HBV-частиц и антигенов HBV. Показана локализация ДНК и ДНК-полимеразы в ядре HBV-частицы величиной 42 нм.

Рис. 7.13. Схема последовательности сероиммунологических изменений, наблюдаемых при типичном гепатите В. *Антитела анти-HBs могут образовываться в раннем периоде гепатита, но часто не идентифицируются как свободно циркулирующие антитела.
Вирус гепатита С (HCV) ранее описывали как «ни А, ни В»-гепатит, он составляет до 90 % всех посттрансфузионных гепатитов. Факторы риска включают переливание крови и/или компонентов крови, но у значительной части больных факторы риска не выявляются. У большинства больных с HCV развивается хронический гепатит, а примерно у 25 % — цирроз печени. К серологическим тестам для выявления антител к вирусным гепатитам HCV относят иммуносорбентный метод исследования ферментных связей или метод рекомбинантного иммунного пятна. Антитела к HCV могут сохраняться более 6 мес после инфицирования. Наиболее чувствительным методом диагностики гепатита С является определение РНК вируса гепатита С при помощи цепной полимеразной реакции.
Гепатит Е (HEV) ранее называли эпидемическим «ни А, ни B»-гепатитом. Заболеваемость этим гепатитом имеет место только в развивающихся странах. Он редко встречается в США, а отдельные случаи заболевания обычно связаны с посещением эндемических регионов. Передача инфекции происходит фекально-оральным путем (аналогично гепатиту А). Эпидемии гепатита Е характеризуются высоким уровнем смертности, особенно беременных женщин. Но как и гепатит А, гепатит Е не приводит к развитию хронических заболеваний печени.
Гемохроматоз
Гемохроматоз представляет собой наследственное заболевание, передаваемое по аутосомно-рецессивному типу, характеризующееся нарушением кишечной абсорбции железа с накоплением его в клетках паренхиматозных органов (табл. 7.7). Так как печень является основным органом депонирования железа в организме, поражение печени, проявляющееся микронодулярным циррозом, является общим и ранним признаком наследственного гемохроматоза (рис. 7.14). Может развиваться застойная сердечная недостаточность, вторично ведущая к дилатационной кардиомиопатии со склонностью к накоплению железа в мышце сердца. Эндокринные признаки наследственного гемохроматоза характеризуются гипогонадизмом, часто в комбинации с частичной дисфункцией переднего гипофиза, первичной тестикулярной недостаточностью, сахарным диабетом. Также характерны артропатии и патологическая пигментация кожи.
Таблица 7.7. Сравнение маркеров при первичном гемохроматозе и алкогольном заболевании печени
| Нормальный уровень | Алкогольное заболевание печени | Гемохроматоз | |
| Насыщение трансферрина железом (%) | 20-50 | 50-60 | >62 |
| Ферритин плазмы (нг/мл) | 15-300 | 300-100 | 500-6000 |
| Концентрация железа в печени (мкг/г сухого вещества) | 300-1800 | 1800-5000 | 10000-30000 |
| Индекс железа (мкмоль Fe/ г сухого вещества/возраст) | < 1.1 | <1.6 | >1.8 |

Рис. 7.14. Биопсия печени при гемохроматозе. Избыточное отложение железа выявляется окраской Пруссидом голубым
Тесты скрининг-диагностики наследственного гемохроматоза включают определение содержания железа в сыворотке, уровня насыщения трансферрина (концентрация железа в сыворотке зависит от общей железосвязывающей способности), содержание сывороточного ферритина. Наконец, диагноз уточняется путем определения железа в гистологическом препарате биоптата печени.
Вторичный гемохроматоз может быть результатом:
- (1) накопления в печени железа при некоторых анемиях (талассемия, сидеробластная анемия);
- (2) пролонгированного применения парентеральных препаратов железа или избыточного употребления железа с пищей;
- (3) болезней печени (алкогольный цирроз, поздняя кожная порфирия, портокавальное шунтирование).
Болезнь Вильсона
Болезнь Вильсона (гепатолентикулярная дегенерация) — это аутосомно-рецессивное заболевание, характеризующееся нарушением связывания меди, что приводит к циррозу печени, дегенерации базальных ганглиев, зеленовато-коричневой пигментации на роговице (кольца Кайзера-Флейшера) (рис. 7.15). У большинства больных симптомы обнаруживаются в возрасте от 5 до 30 лет.
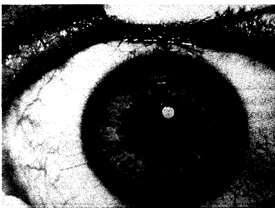
Рис. 7.15. Кольца Кайзера-Флейшера
Поражение печени может проявляться одним из четырех вариантов: острый гепатит, фульминантный (злокачественный) гепатит, хронический активный гепатит или ранний цирроз печени. Быстрое высвобождение меди из печени при злокачественном гепатите вызывает возникновение характерной для данной патологии гемолитической анемии. Двигательные нарушения типичны и характеризуют поражение нервной системы при болезни Вильсона. Напротив, психические нарушения многообразны и проявляются асоциальным поведением, шизофренией, неврозами, деменцией. При проведении лабораторных тестов определяется снижение уровня церулоплазмина в крови, повышение суточной экскреции меди, повышение содержания меди в печени при биопсии (табл. 7.8). Лечение заключается в связывании избытка меди D-пеницилламином, либо триэтилентетраминдигидрохлоридом (триентин). При злокачественном течении заболевания может быть произведена ортотопическая пересадка печени.
Дефицит а1-антитрипсина
Белок а1-антитрипсин синтезируется в печени и, в меньшей степени, макрофагами и моноцитами и действует как ингибитор эластазы лейкоцитов. Этот гликопротеин мигрирует с агглобулиновой фракцией при электрофорезе белков и составляет 80—90 % этой фракции. У людей, относящихся к гомозиготному генотипу, активность а1-антитрипсина мала, они предрасположены к переходу гепатита в хроническую форму на ранней стадии заболевания и развитию криптогенного цирроза печени. Дефицит а1-антитрипсина можно предположить у больных с признаками гепатолентикулярного поражения, у которых отсутствует пик а1-глобулина при электрофорезе. При диагностике используют определение уровня а1-антитрипсина и генетический анализ. При биопсии печени выявляют Шифф-положительные гранулы в перипортальных гепатоцитах, свидетельствующие о неспособности последних синтезировать и секретировать Z-белок (рис. 7.16).
Аутоиммунный хронический активный гепатит
Это заболевание обусловлено нарушениями иммунорегуляции и характеризуется высокими титрами антинуклеарных антител у гомозигот с гипергаммаглобулинемией. Особенностями, позволяющими предполагать это заболевание, являются: отсутствие серологических маркеров вирусного гепатита или метаболических расстройств печени, отсутствие в анамнезе воздействия гепатотоксических веществ и алкоголя, наличие сопутствующих аутоиммунных заболеваний и ответной реакции на терапию кортикостероидами. В некоторых случаях вместо антинуклеарных антител могут обнаруживаться антитела к микросомам гепатоцитов и почек или антитела к гладкомышечным клеткам.
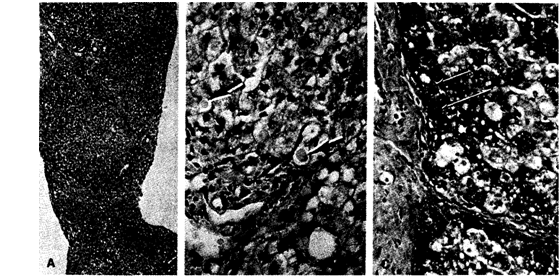
Рис. 7.16. Дефицит а1-антитрипсина. (А) — биопсия печени больного в период первого года цирроза печени при малом увеличении светового микроскопа. (В) — округлые эозинофильные гиалиновые тельца, напоминающие эритроциты, но крупнее их и без двояковогнутой формы, встречающейся у перипортальных гепатоцитов с высокой функциональной активностью (отмечено стрелкой). (С) — окраска перйодной кислотой по Шиффу выявляет диастазорезистеитные глыбки по соседству с соединительной тканью портальных трактов.
Таблица 7.8. Содержание меди в организме больных болезнью вильсона и у обследуемых из контрольных групп
| Радиоактивная медь (64Сu)64Сu — % внутривенной дозы, выводимой с мочой за период | ||||||||
| Группы | Церулоплазмин в плазме(мг/л ± SE) | Содержание Сu в плазме(мкг/л) | Выведение Сu с мочой(мкг/сут) | Содержание Сu в печени (мкг/г веса) | Относительное содержание в плазме 64Сu* | 0-8 ч(М ± SE) | 8-24ч(М ± SE) | 24-30ч после приема пеницилламина (M±SE) |
| Болезнь Вильсона | ||||||||
| бессимптомное течение | 63 ±10 | <600 | >50 | >50 | <0,4 | 0,92 ±0,12 | 0,17 ±0,04 | 0,84 ±0,11 |
| манифестная форма | 63 ±10 | <600 | >50 | >50 | <0,4 | 1,22 ±0,21 | 0,70±0,16 | 3,45 ±0,45 |
| гетерозиготы | 254 ± 11 | >б00 | <50 | <50 | >0,4 | 0,10 ±0,01 | 0,05 ±0,01 | 1,20±0,12 |
| Болезнь печени** | 380 ± 29 | >1000 | <50 | <50 | >0,6 | 0,20 | 0,17 | 1,94 |
| Контроль, мужчины | 333 ±7 | >800 | <30 | <10 | >0,8 | 0,14±0,02 | 0,07 ±0,01 | 2,36 ±0,33 |
| Контроль, женщины | 366±10 | >800 | <30 | <10 | >0,8 | 0,14±0,02 | 0,07 ±0,01 | 2,36 ±0,33 |
* Отношение концентрации в плазме радиоактивной меди (64Сu) через 24 ч к концентрации в плазме радиоактивной меди через 2 ч после внутривенного введения препарата (64Сu).
**Исключая данные пациентов с первичным билиарным циррозом, у которых содержание меди в печени и моче может быть таким же, как и при болезни Вильсона.
Алкогольный гепатит
Основными симптомами алкогольного гепатита являются анорексия, тошнота, рвота, боль в животе, желтуха, лихорадка. Причем, течение заболевания может варьировать от безжелтушного и бессимптомного до тяжелого с асцитом и печеночной энцефалопатией. Таким образом, симптоматика алкогольного гепатита часто похожа на проявления других гепатобилиарных заболеваний. При этом необходимо учитывать, что алкоголики могут страдать и другими болезнями печени. Уровень АсАТ повышается непропорционально больше, чем уровень АлАТ, хотя если они менее 300 ME, то это считается нормой. Гистологически определяются гепатоцеллюлярный некроз в перицентральных зонах с отложением алкогольного гиалина (тельца Маллори) и инфильтрация полиморфноядерными лейкоцитами (рис. 7.17).
Повреждение печени лекарственными препаратами
Повреждение печени лекарственными препаратами может проявляться в виде гепатоцеллюлярных некрозов, холестатического синдрома или иметь сочетанный характер. Токсическое действие лекарств на гепатоциты клинически напоминает повреждения при ишемическом и вирусном гепатитах и значительно варьирует по тяжести течения. Это заболевание можно предполагать при наличии данных о приеме потенциально гепатотоксических препаратов в последние три месяца. Поэтому необходим тщательный сбор анамнеза, в котором помимо лекарственной терапии важно учитывать наличие профессиональной вредности. Определение у больного эозинофилии, сыпи, лихорадки также может свидетельствовать о наличии гепатотоксического действия лекарственных препаратов, но эти симптомы часто неспецифичны или отсутствуют.
Наиболее часто встречается повреждение печени ацетаминофеном. Оно связано с действием его метаболита — N-ацетил-р-бензохинонимина, взаимодействующего с макромолекулами гепатоцита и приводящего к гибели клетки (рис. 7.18). Прием ацетаминофена в дозе от 10—15 г может стать причиной некроза гепатоцитов. Хроническое употребление алкоголя усиливает токсическое действие ацетаминофена, поскольку алкоголь индуцирует цитохром Р450. При этом прием даже 3—4 г лекарства в сутки может вызвать значительный гепатотоксический эффект.

Рис. 7.17. Биопсия печени при алкогольном гепатите. В центре рисунка представлены перинуклеарные тельца Маллори внутри гепатоцитов
