СЕРДЕЧНЫЕ ГЛИКОЗИДЫ
Глава 8. Анализ производных терпенов и циклопентанпергидрофенантрена
Гликозиды — эго группа физиологически активных веществ природного происхождения, оказывающих специфическое действие на сердечную мышцу, при этом их действие проявляется в весьма малых дозах.
Препараты сердечных гликозидов находят применение для компенсации недостаточности сердечной деятельности, многие из них оказывают и диуретический эффект.
Большинство гликозидов сердечного действия относятся к списку А.
По своему строению гликозиды являются эфирами циклических форм сахаров (циклические ацетали), где сахарная часть и несахарная (агликон) соединены через полуацетальный гидроксил сахарной части. Циклические формы сахаров, как известно, носят название полуацетальных форм, гак как они действительно представляют собой внутренние полуацетали, образовавшиеся в результате реакции альдегидной и спиртовой групп в пределах одной и той же молекулы.

Образовавшийся из альдегидной или кетонной группы гидроксил отличается большой реакционной способностью.
Несахарная часть гликозидов называется агликоном; агликоны стероидной природы (в сердечных гликозидах) носят также название генины.
Сахарная часть может быть моносахаридом, дисахаридом, трисахаридом и т.д.
Гликозиды как циклические ацетали под действием кислот и ферментов легко расщепляются на составные части.
Ферменты (или энзимы) действуют избирательно и позволяют осуществлять ступенчатое отщепление сахаров. Ферменты часто находятся в тех же объектах, что и сами гликозиды, поэтому необходимо соблюдать осторожность при выделении гликозидов из сырья.
Сырье сушат при 40—60 °С или помещают в сосуд с парами спирта, хлороформа — это способствует инактивации ферментов, а гликозиды остаются нерасщепленными.
В отличие от сахаров, гликозиды (за некоторым исключением) не обладают восстановительной активностью, поскольку полуацетальный гидроксил блокирован. Исключение составляют гликозиды с восстановительными группами (альдегидная группа). После разложения можно доказать восстановительные свойства сахаров, например с реактивом Фелинга (свободный сахар).
Строение сердечных гликозидов
Различают естественные гликозиды (первичные, генинные) и вторичные, образовавшиеся из первичных и содержащие на 1 или 2 молекулы сахара меньше, чем первичные.
Установление строения сердечных гликозидов карденолидов сводилось к установлению строения агликона.
Агликоны сердечных гликозидов содержат 23 или 24 углеродных атома и различаются между собой по степени окисленности. Они содержат не менее 2 гидроксильных групп, некоторые — альдегидную труппу. Все агликоны содержат ненасыщенное лактонное кольцо.
Некоторые гликозиды содержат в 10-м положении не метильную ангулярную группу, а альдегидную (гликозиды строфанта, ландыша).
Исходя из многочисленных исследований было установлено, что в основе строения всех сердечных гликозидов лежит ядро циклопентанпергидрофенантрена, к которому в 17-м положении присоединяется ненасыщенное лактонное кольцо с двойной связью с β, α — положении, а в 3~м положении через атом кислорода — остаток сахара:

Обязательными элементами проявления кардиотонической активности является, кроме β, α -ненасыщенного ϒ-лактонного кольца при С17, наличие третичной β-ориентированной ОН-труппы при С14 и углеводного фрагмента при С3, а также (в отличие от других природных стероидов), цис-сочленение колец С и D. Агликоны различаются конфигурацией и количеством заместителей. Пространственная конфигурация определяется сочленением колец А,В,С,D, а также расположением заместителей при С10, С12, С13, С14.
Кроме упомянутого для кардиостероидов цис-сочленения колец С и Г), для них характерно цис- или транс-сочленение колец А и В и транс-сочленение колец В и С.
Сердечные гликозиды по характеру заместителя в 10-м положении можно разделить на 2 группы:
1) подгруппа наперстянки — в положении С10 содержит –СН3 группу;
2) подгруппа строфанта — в положении С10 содержит альдегидную группу.

Вторичные гликозиды наперстянок состоят из агликонов и сахарной части одинаковой у всех 3 вторичных гликозидов.

На основе данных табл. 29 и 30, а также сведений о химическом составе агликонов можно вывести формулы первичных и вторичных гликозидов наперстянок.
Формула дигитоксина:

Формула дигиланида С (целанида).

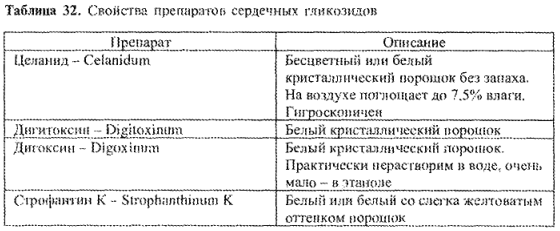
Первичный гликозид наперстянки шерстистой — дигиланид С под названием целанид (Celanidum) и вторичный гликозид наперстянки пурпурной — дигитоксин (Digitoxinum) включены в ГФ.
В ГФ включен также препарат строфантин К (Strophanthinum К). Его получают из семян строфанта Комбе. Препарат содержит в основном 2 гликозида, состав которых приведен в табл. 31.

К-строфантин-β можно рассматривать как вторичный гликозид К.-строфатозида. Последний, теряя молекулу глюкозы, превращается в К-строфантин-β. Формула К-строфантозида:

Сахарная часть гликозидов
Как отмечалось ранее, сахарный компонент может быть моно- и ди-, и три-сахаридом и т.д. У сахаров различают α и β-формы; D- и L-ряды и оптическую активность (+ или -). D-ряд — это моносахариды, у которых конфигурация атомных групп у последнего ассиметрического атома углерода такая же, как у правовращающего — глицеринового альдегида, L-ряд — соответственно как у L-глицеринового альдегида.
α-Форма — это форма сахара, у которого полуацетальный гидроксил направлен в ту же сторону, что и гидроксил у последнего ассиметрического атома углерода; в β-форме — они направлены в прогивоположные стороны.
Оптическая активность сахаров зависит от конфигурации атомных групп у всех ассиметрических атомов углерода.
Сердечные гликозиды могут содержать:

Дигитоксоза, цимароза и олеандроза являются 2,6-дезоксисахарами. Агликоны сердечных гликозидов практически нерастворимы в воде. Сахарный компонент сам по себе неактивный, способствует улучшению растворимости сердечного гликозида, повышает его проницаемость через клеточные мембраны, тем самым усиливая действие агликона.
Методы выделения сердечных гликозидов из растительного сырья
Сердечные гликозиды находятся в растениях в небольших количествах — от 0,001 до 0,2 %.
Растительное сырье экстрагируют эфиром для удаления жиров и смол, а затем — спиртом или смесью спирта и хлороформа. При этом происходит инактивация энзимов, так как они представляют собой вещества белковой природы.
Полученный экстракт выпаривают в вакууме до густой консистенции и экстрагируют теплой водой. Сапонины, которые часто сопровождают сердечные гликозиды, осаждают ацетатом свинца, а избыток ацетата свинца удаляют добавлением серной кислоты; при этом образуется нерастворимый сульфат свинца.
При стоянии из водного раствора выпадает смесь неочищенных гликозидов. Для очистки суммы гликозидов, а также выделения каждого из них отдельно применяют методы фракционной кристаллизации. В последнее время широко используются адсорбционные методы на различных носителях (силикагеле, кизельгеле и др.).
Физические свойства сердечных гликозидов
Сердечные гликозиды — это твердые вещества, кристаллические, плохо растворимы в воде, оптически активные.
Методы идентификации сердечных гликозидов
- Анализ сахаров
Сахара, входящие в состав сердечных гликозидов, дают все цветные реакции, свойственные углеводам: восстанавливают реактив Фелинга, аммиачный раствор нитрата серебра (после гидролиза), образуют окрашенные соединения с ксантгидролом, n-диметиламино-бензальдегидом. Специфическими сахарами сердечных гликозидов являются 2,6-дезоксисахара, для обнаружения которых применяют тест Келлера—Киллиани. Наиболее распространенным реактивом для открытия сердечных гликозидов по углеводному фрагменту является ксантгидрол (реакция Пезеца).
При нагревании смеси ксантгидрола (дибензо-ϒ-пиранола) с испытуемым гликозидом в присутствии ледяной СН3СООН и последующем прибавлении нескольких капель серной или фосфорной кислоты появляется красное окрашивание.
Аналогичную цветную реакцию дает антрон. Методика основана на образовании фурфурола или его производных из сахарных компонентов под действием концентрированной Н2SО4. Фурфурол с антроном затем дает продукт конденсации, окрашенный в зеленый или сине-зеленый цвет:

- Анализ стероидного цикла
Реакции стероидного цикла основаны на цветных реакциях, проводящих при взаимодействии с реактивами, вызывающими дегидратацию гидроксильных групп (особенно при С5 и С10) стероидного скелета с образованием ангидропроизводных. Обычно эти реакции осуществляются в среде концентрированных кислот или под влиянием катализаторов Фриделя—Крафтса. При нагревании до 100°С раствора гликозиды в уксусном ангидриде с 20-25 % раствором треххлористой сурьмы появляется лиловое окрашивание.
Тест Либермана—Бурхарда. Раствор испытуемого вещества в уксусной кислоте смешивают с 2 мл смеси, состоящей из 50 частей уксусного ангидрида и 1 части концентрированной Н2SО4; при этом развивается розовое окрашивание, постепенно переходящее в зеленое или синее. Окраска определяется строением генина: строфантин и его гликозиды в этих условиях окрашиваются в оливковозеленый цвет, переходящий в желтый.
Для сердечных гликозидов характерно явление галохромии: образование окрашенных соединений с концентрированными минеральными кислотами; наибольшее распространение получили цветные реакции с серной кислотой.
Тест Рейхштейна. Несколько кристаллов гликозида смачивают 2 каплями 84 % Н2SО4 и отмечают изменение окраски во времени. Лабильность окраски специфична и используется для первичной идентификации сердечных гликозидов. Для идентификации карденолидов также используется их способность флюоресцировать в УФ- свете в виде пятен различной окраски при взаимодействии, например с фосфорной кислотой.
- Реакции на β,α-ненасыщенное лактонное кольцо
К этой группе относятся реакции, в результате которых при взаимодействии сердечного гликозида с некоторыми полинитропроизводными в щелочной среде образуется окрашивание.
- Сердечные гликозиды в присутствии щелочи дают с пикриновой кислотой (тринитрофенолом) оранжевую окраску (реакция Балье):

- Пятичленный лактонный цикл можно также обнаружить по образованию окрашенных в красно-фиолетовый цвет продуктов взаимодействия в щелочной среде с м-динитробензолом (реакция Раймонда).
Несовместимость сердечных гликозидов
- Карденолиды несовместимы с кислотами и соединениями, которые дают кислую реакцию среды. В данном случае происходит гидролиз по гликозидной связи (отщепление сахаров). Реакция проходит без видимых внешних изменений (с аскорбиновой кислотой и другими витаминами кислой реакции среды).
- Сердечные гликозиды несовместимы со щелочами и соединениями, которые дают щелочную реакцию среды NaНСО3, барбитал-натрия и др.).
В щелочной среде не происходит гидролиза гликозидной связи, а идет алломеризация с образованием неактивного гликозила (расщепляется лактонное кольцо).
На 1-й стадии происходит расщепление β,α-ненасыщенного лактонного кольца с образованием соответствующей оксикислоты:

Затем происходит образование полуацеталя:

Далее γ-кислота способна образовывать внутренний сложный эфир (лактон), что приводит к созданию новой циклической системы (лактонизация). Образовавшийся неактивный изоагликон имеет УФ- спектр, который резко отличается от такового нативного гликозида (возможность оценки чистоты методом УФ-спектрометрии).

- Соли тяжелых металлов осаждают сердечные гликозиды из растворов.
- Гликозиды несовместимы с дубильными веществами (отвар толокнянки и др.), препаратами валерианы (уменьшение фармакологической активности сердечных гликозидов), производными барбитуровой кислоты (уменьшение амплитуды сердечных сокращений), с диуретиками (усиление действия сердечных гликозидов, гипокалиемия).
- Карденолиды разлагаются при нагревании.
Методы количественного определения кардиоактивных стероидов
Кардиоактивные стероиды являются терапевтически важной группой веществ. Для понимания роли этих соединений в жизни растений проводились исследования их метаболизма в живом организме. Результаты данных исследований позволили успешно применять указанные стероиды в медицине (налажен промышленный выпуск сердечных гликозидов). Однако для безопасного использования этих веществ необходимо проводить стандартизацию не только самих ЛС, но и природных источников всевозможными методами количественного oпределения.
До настоящего времени количественная оценка кардиоактивных стероидов проводится в основном с помощью биологических тестов на животных. Биологические методы трудоемки, длительны, плохо воспроизводимы, малодостоверны (ошибки в пределах 10— 20%).Результаты биологического анализа зависят от индивидуальных особенностей животных и не позволяют получить объективную качественную и количественную информацию о действующем веществе.
Стандартизация сердечных гликозидов с помощью биологического метода основана на способности карденолидов вызывать в токсических дозах остановку сердца животных в стадию систолы. Их активность оценивают по сравнению с активностью стандартных препаратов и выражают в единицах действия (ЕД) — кошачих (КЕД), лягушачих (ЛЕД), голубиных (ГЕД).
Известно значительное число методов, в основе которых лежит титриметрическое, фотометрическое, флюориметрическое и полярографическое определение кардиостероидов.
Химические методы
Кислотно-основное титрование в неводной среде (подгруппа строфанта).
И.А. Казаринов и Н.П, Дзюба предложили объемный метод, основанный на способности альдегидной группы при С10 (агликон строфант идина) образовывать оксим при взаимодействии с гидроксиламином в среде диэтиламина. Диэтиламин связывает соляную кислоту, образующуюся при оксимировании; избыток оттитровывают хлорной кислотой. Ошибка метода составляет 0,7—2,6%. Несмотря на то, что метод быстр в исполнении, он не получил распространения, так как пригоден только для анализа стандартных образцов и требует тщательной очистки реактивов от соединений, содержащих карбонильные группы.
Физико-химические методы
- УФ-спектрофотометрический (используется при анализе сырья и стандартного вещества при 217—219 нм).
- Фотометрический метод:
- целанид — с ксантгидроловым реактивом;
- реактив Татье — 2,4-дииитрофенилсульфон — рекомендуется для анализа сырья, лекарственных веществ и лекарственных препаратов (ГФ XI) (реакция на пятичленное лактонное кольцо).
- Хроматографические методы (ВЭЖХ, ГЖХ).
- Флюориметрические методы анализа.
Основаны на способности сердечных гликозидов флюоресцировать под действием сильных кислот и окислительных агентов после кратковременного облучения УФ-светом.
Под действием сильных кислот или окислительных агентов происходит дегидратация гликозидов с образованием ангидропроизводных.
Так, при действии на гитоксин фосфорной кислоты образуется диангидрогитоксин, который под влиянием УФ-света флюоресцирует. При этом интенсивность флюоресценции пропорциональна концентрации гликозида, что позволяет проводить количественную оценку. Необходимо сопоставление химических и физико-химических методов с результатами биологических методов.
Испытание на чистоту
Чистота характеризуется различными физико-химическими параметрами (удельное вращение, ПК- и УФ-спектры, Тпл). Кроме того, регламентируется содержание влаги (способствует гидролизу полуацетальной связи), сульфатной золы и тяжелых металлов (факторы, катализирующие окисление препаратов). Для оценки доброкачественности инъекционных растворов дополнительно оценивают их прозрачность и цветность.
Особое внимание обращают на наличие примесей посторонних гликозидов. Это относится прежде всего к ЛС, полученным из растений, содержащих несколько сходных по структуре сердечных гликозидов. Примесь посторонних стероидов обнаруживают с помощью бумажной хроматографии по величине Rf и флюоресценции пятен.
Хранение
Список А. В хорошо укупоренных банках оранжевого стекла, в сухом, защищенном от света месте.
