Производные пурина. Фармацевтический анализ пурина
Глава 16. Анализ лекарственных средств группы пурина
Фармацевтическая химия — Арзамасцев А. П. — 2004
В природе производные пурина имеют большое биологическое значение. Соединения группы пурина содержатся в растениях и тканях животных в свободном виде, а также входят в состав нуклеозидов, нуклеотидов и нуклеиновых кислот.
Кофеин содержится в листьях чая (до 5%) и зернах кофе (до 1,5%). Впервые кофеин выделен и описан Ф. Рунге (1819); строение этого алкалоида доказано Э. Фишером в 1882 г. В листьях чая содержится также теофиллин, а в бобах какао — теобромин.
Нуклеиновые кислоты присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению и передаче генетической информации.
К производным пурина относится большая труппа лекарственных веществ, обладающих рахтичной фармакологической активностью — бронхолитической, диуретической, кардиотонической, противоопухолевой, действием на ЦНС.
В основе химической структуры указанных лекарств лежит бициклическая система пурина, существующая в виде 2 изомеров:
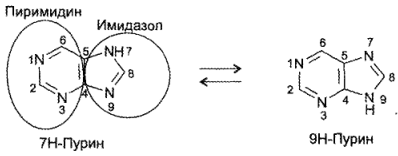
ЛС — производные пурина по химическому строению разделяются на следующие группы:
- производные ксантина;
- нуклеозиды и нуклеотиды пурина (рибоксин, АТФ, динатриевая соль аденозинтрифосфорной кислоты);
- синтетические производные пурина и близкие по строению (табл. 67).
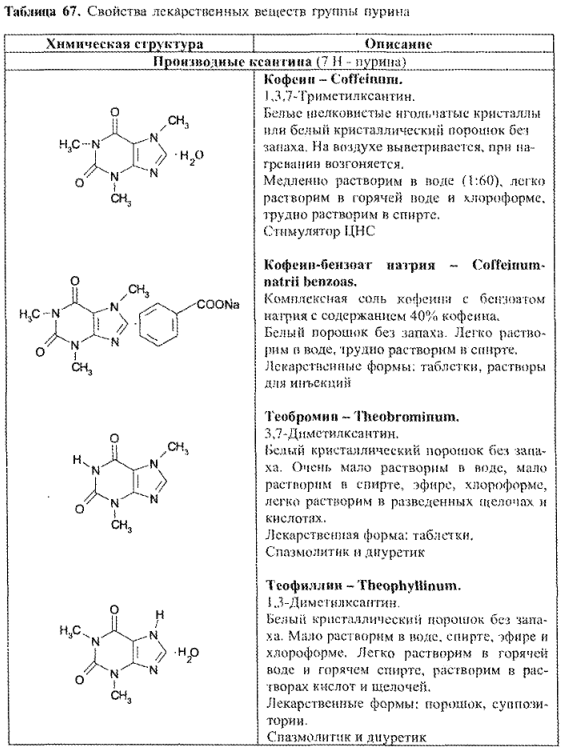
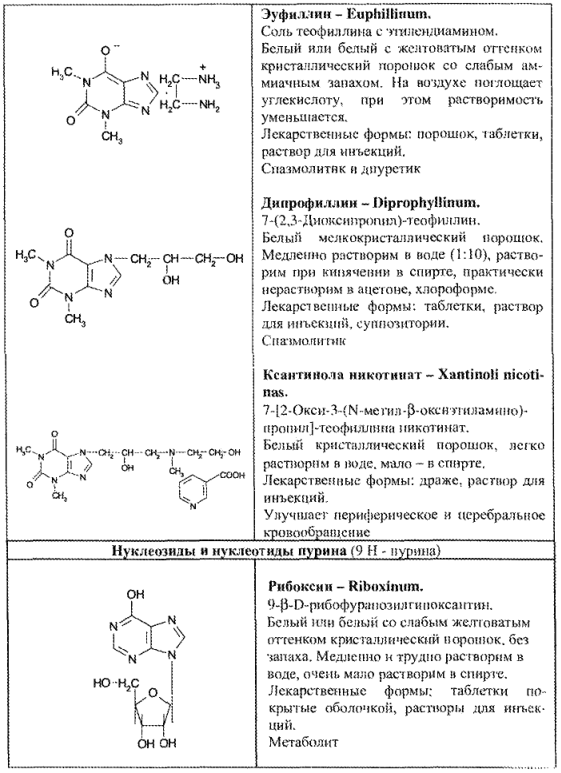
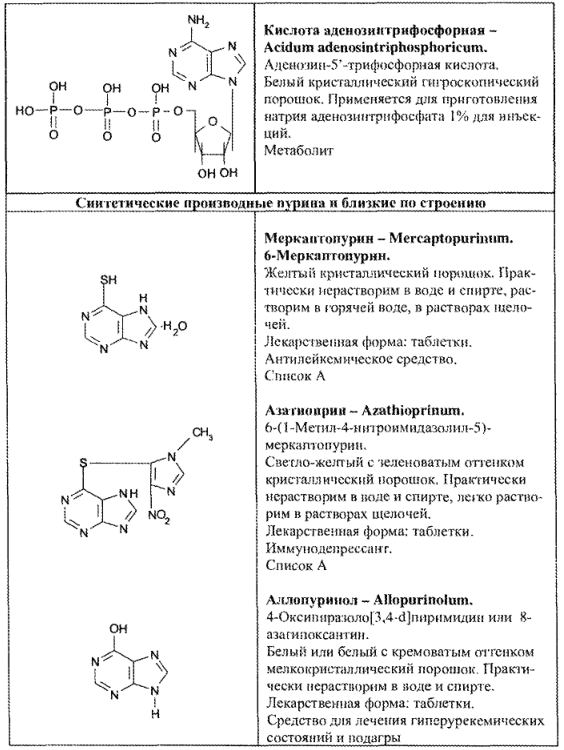

ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА И АНАЛИЗ КАЧЕСТВА
Физические свойства
Все соединения группы пурина — кристаллические порошки белого цвета с характерными Тпл и спектрами поглощения в УФ- и ИК-областях.
Способы получения
Вещества группы пурина можно получать из природных источников и синтетически. Пуриновые алкалоиды (кофеин, теофиллин, теобромин) — растительного происхождения.
С конца XIX в. успешно развиваются различные методы синтеза пурина и его производных. Впервые пурин был синтезирован Э. Фишером в 1899 г. при восстановлении 2,6,8-трихлорпурина. В настоящее время наибольшее практическое значение имеют 4 способа синтеза пуринов:
- Конденсация 4,5-диаминопиримидинов с карбоновыми кислотами (синтез Траубе, 1910). Этот способ в дальнейшем многократно модифицировался и до сих пор не утратил своего значения:
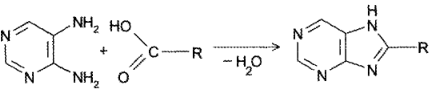
- Конденсация 4,5-диоксипиримидинов с. мочевиной (Беренд, Розен, 1888):
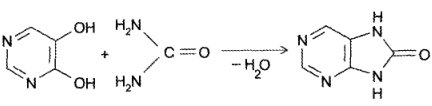
- Присоединение цианатов или изотиоцианатов к 5-амино-2,4,6- гриоксиоксипиримидину с последующей циклизацией образующегося карбамида пои нагревании в кислой среде (Э. Фишер, Аш, 1895):
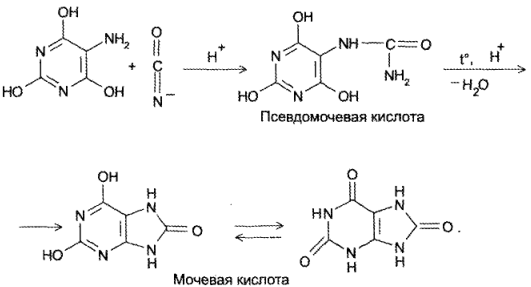
- Конденсация амида 5-амино-1-метилимидазол-4-карбоновой кислоты с муравьиной кислотой:
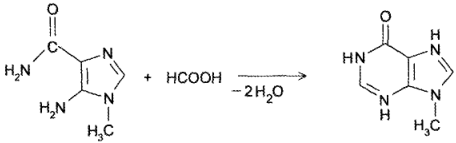
Кислотно-основные свойства
Пурин — ароматическая система с сильной делокализацией тг-электронов, которые играют большую роль в образовании различных молекулярных комплексов. Он обладает электронодонорными свойствами и представляет собой растворимое в воде слабое основание (рКа = 2,4), образующее с кислотами непрочные соли. В то же время благодаря наличию подвижного атома водорода в NН- группе пурин проявляет слабые кислотные свойства (рКа — 8,9) и образует соли с металлами.
Лекарственные вещества группы пурина — слабые основания, образующие с кислотами неустойчивые соли при протонировании гетероатома азота в 9-м положении.
Как правило, производные ксантина с трудом растворяются в воде (лучше — в горячей). Для получения хорошо растворимых лекарственных препаратов используется их способность к комплексообразованию. Данные о растворимости различных веществ группы пурина представлены в табл. 68:
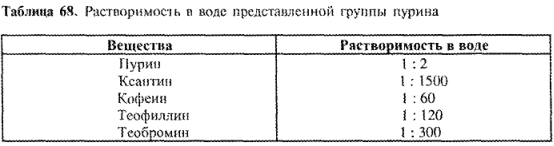
Хорошая растворимость пурина объясняется тем, что он образует водородные мостики с молекулами воды. Особенно мала растворимость ксантина. При метилировании атомов азота она значительно улучшается, как видно на примере кофеина, теофиллина, теобромина. Различия в растворимости объясняются разной межмолекулярной ассоциацией.
У кофеина 3 гетероатома азота метилированы. Вещество является мономером (не образует ассоциатов через водородные мостики), что объясняет его лучшую растворимость и низкую Тпл. Растворимость кофеина увеличивается в горячей воде, а также в присутствии солей органических кислот (за счет образования комплексов).
В теофиллине имеется одна свободная, но мало активная NН- группа, способная образовывать слабые межмолекулярные водородные мостики. Как в твердом состоянии, так и в растворе предполагается димеризация. Это подтверждается меньшей, чем у кофеина, растворимостью и более высокой Тпл.
Теобромин в твердом состоянии образует еще большие межмолекулярные агрегаты, основанные на активной NН-группе и выгодных в пространственном отношении карбонильных группах. Плохую растворимость и высокую Тпл можно также объяснить этой стабильной ассоциацией, что доказано ПК-спектроскопией.
Тенденция ксантинов к «самокомплексообразованию» противостоит их предрасположенности к образованию комплексов с солями органических кислот (бензойной, салициловой, 4~аминобензойной, ацетилсалициловой и др.).
Кофеин — слабое органическое основание (рКa. = 0,61). Растворим в минеральных кислотах, но устойчивых солей не образует. Взаимодействует с общеалкалоидными осадительными реактивами. Но с раствором йода реагирует только при подкислении (что характерно для такого слабого основания) с образованием осадка перйодида (Соff*Cl*14 ). С танином кофеин образует осадок, растворимый в избытке реактива. В отличие от многих других оснований кофеин не осаждается реактивом Майера, что используется при определении чистоты препарата.
Теобромин и теофиллин являются амфотерными соединениями. Их основные свойства обусловлены наличием неподеленной пары электронов атома азота в 9-м положении. Кислотные свойства теобромина (рКа= 9,9) связаны с подвижностью атома водорода имидной группы, а теофиллина (рК,~ 8,8) — с подвижностью атома водорода при гетероатоме азота в 7-м положении. Кислотные свойства у теофиллина выражены сильнее, чем у теобромина. Это связано с тем, что теобромин в растворах щелочей образует только лактимную форму, а теофиллин — мезомерно стабилизированный анион:
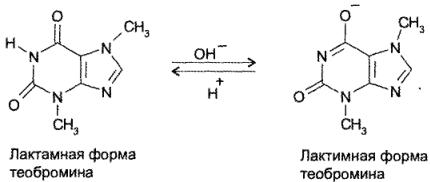
Обладая более выраженными, чем у теобромина, кислотными свойствами, теофиллин растворяется не только в щелочах, но и в растворе аммиака:
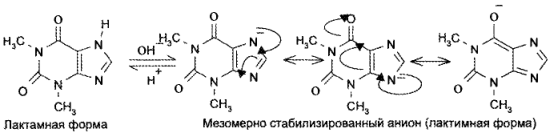
За счет кислотных свойств теофиллин и теобромин образуют растворимые соли не только со щелочами, но и с органическими основаниями. С солями тяжелых металлов (Аg+, Со2+, Сu2+) получаются нерастворимые соединения.
Мурексидная проба (общегрупповая реакция)
Реакция основана на окислительно-гидролитическом разложении веществ группы ксантина до производных пиримидина, в которых 1 или 2 аминогруппы конденсируются друг с другом до образования пурпурной кислоты, имеющей в виде аммонийной соли красно фиолетовое окрашивание. Для проведения реакции препарат нагревают на водяной бане до полного упаривания с окислителем (Н2О2, Вr2, НNО3) в кислой среде. Затем добавляют раствор аммиака; появляется пурпурно-красное окрашивание.
Химизм (на примере мочевой кислоты):
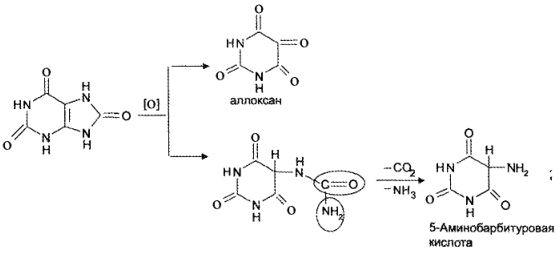
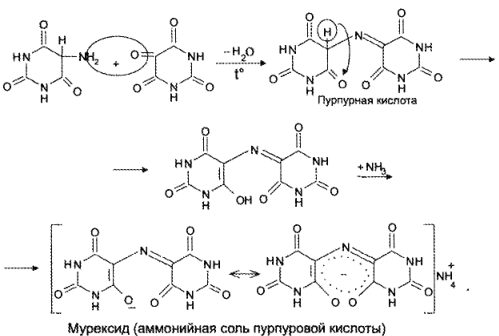
Для мочевой кислоты нагревание производят с кислотой азотной концентрированной, которая окислительно разлагает вещество до аллоксана и 5-аминобарбитуровой кислоты. Затем продукт окисления (как карбонильное соединение) конденсируется с продуктом гидролиза до пурпурной кислоты, которая в присутствии аммиака переходит в мезостабилизированный анион, назывемый мурексидом.
В случае метилированных производных ксантина вместо азотной кислоты применяют раствор пероксида водорода в солянокислой среде и затем добавляют аммиак (в случае, если он не образуется при гидролизе препарата).
Реакции электрофильного замещения после щелочного гидролиза
Кофеин, обладающий слабоосновными свойствами, неустойчив в щелочной среде. При pH > 9 происходит разложение кофеина до кофеидинкарбоновой кислоты, которая разлагается с образованием кофеидина и соответствующего карбоната. Причем кофеидия является антагонистом кофеина по фармакологическому действию, что может привести к нежелательным последствиям при применении разложившегося препарата.
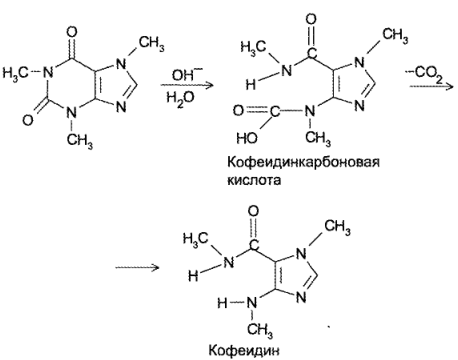
В сернокислой среде кофеин может разложиться до муравьиной кислоты. Аналогично разлагается теофиллин до теофиллидина, который далее может быть идентифицирован по реакции азосочетания с солью диазония с образованием азокрасителя:
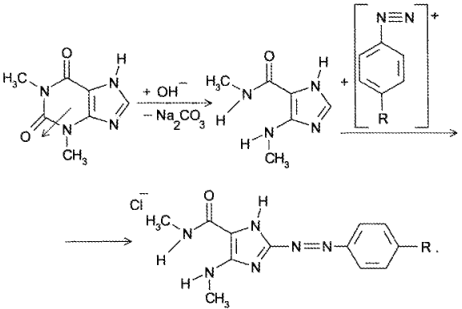
Другие реакции
Теофиллин образует с 2,6-дихлорхинонхлоримидом в боратном буферном растворе (pH 8,5) мероцианиновый краситель интенсивно-голубого цвета:
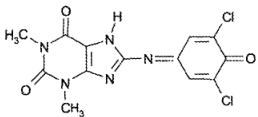
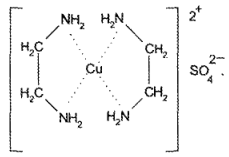
Эуфиллин реагирует с раствором сульфата меди с образованием комплексного соединения красно-фиолетового цвета (реакция на остаток этилендиамина):
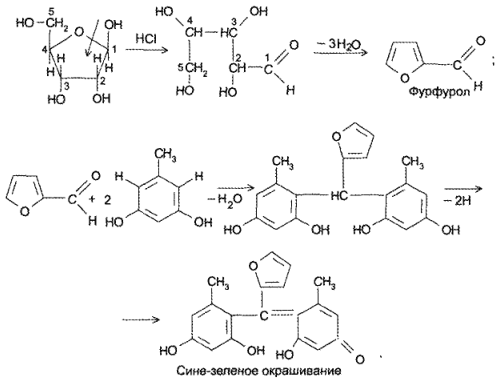
Аденозинтрифосфорная кислота (и натриевая соль) за счет остатка рибозы взаимодействует с орцином в присутствии небольшого количества хлорида железа (III) с образованием продукта конденсации сине-зеленого цвета:
В азатиоприне нитро-группу восстанавливают до первичной ароматической амино-группы и далее проводят диазотирование и азосочетание с фенолом (образование азокрасителя).
Остаток бензойной кислоты в кофеин-бензоате натрия открывают качественной реакцией с хлоридом железа (III) — образуется осадок телесного цвета.
Методы количественного определения
- Кислотно-основное титрование в неводной среде. Препараты-основания и соли оснований определяют в среде уксусного ангидрида (кофеин) или смеси ледяной уксусной кислоты и уксусного ангидрида (ксантинола никотинат). Титрант — 0,1М раствор хлорной кислоты.
Обладающие кислотными центрами теобромин, теофиллин растворяют в протофильных растворителях (диметилформамид, пиридин, бутил амин) и титруют растворами метилатов натрия или калия.
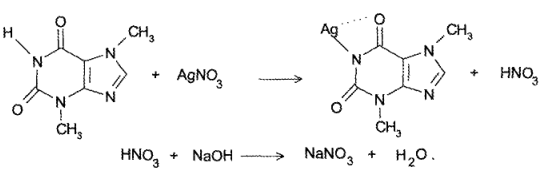
- Косвенный метод нейтрализации. При взаимодействии теобромина и теофиллина с раствором нитрата серебра образуется эквивалентное препаратам количество азотной кислоты, которую титруют стандартным раствором гидроксида натрия:
- Кислотно-основное титрование в водной среде. Кофеин-бензонат натрия определяют по остатку бензоата натрия титрованием стандартным раствором хлороводородной кислоты в присутствии эфира.
Эуфиллин за счет остатка этилендиамина количественно определяют титрованием стандартным раствором хлороводородной кислоты.
- Аргентометрия (обратный способ). К раствору теофиллина или теобромина добавляют аммиак и фиксированный избыток титрованного раствора нитрата серебра; образуется нерастворимая серебряная соль. Осадок отфильтровывают и в фильтрате определяют избыток нитрата серебра титрованием со стандартным раствором роданида аммония (индикатор — железоаммониевые квасцы).
- Йодометрия. Применяется для определения кофеина в кофе- ин-бензоате натрия. Метод основан на образовании осадка перйодида кофеина в кислой среде (соff • Нl • 14), который отфильтровывают и в фильтрате определяют избыток йода.
- Метод Кьельдаля (определение азота в органических веществах).
Данным методом определяют дипрофиллин.
- Весовой метод. Метод иногда используют для определения кофеина в лекарственных формах заводского производства (кофеин извлекают из смеси в щелочной среде хлороформом; далее хлороформ отгоняют, остаток высушивают и взвешивают).
- Физико-химические методы (УФ-спектрофотометрия, ГЖХ и ВЭЖХ) применяют для количественного определения препаратов группы пурина в лекарственных формах заводского производства. Метод рефрактометрии применяют для анализа растворов кофеинбензоата натрия в условиях аптеки.
