ПОСЛЕРОДОВЫЕ ЗАБОЛЕВАНИЯ
Клинические лекции по акушерству (учебное пособие)
- Лохиометра
- Послеродовые язвы
- Послеродовая язва промежности
- Послеродовый эндометрит
- Параметрит
- Тромбоэмболические осложнения
- Перитонит и сепсис
- Септический шок
- Мастит
Послеродовые заболевания — это заболевания, возникающие в послеродовом периоде (от момента родов до конца 6-й недели после родов) и связанные с беременностью и родами.
Различают гнойно-воспалительные послеродовые заболевания и заболевания, не обусловленные инфекционным агентом (послеродовый гестоз, кровотечения, психозы).
Основную группу заболеваний в этом периоде составляют ГСИ. Они возникают в результате проникновения микробов через раневые поверхности, образовавшиеся во время родов, или активации условно-патогенной микрофлоры вследствие ослабления защитных сил организма.
Возбудителями послеродовых заболеваний особенно часто становятся энтеробактерии, стафилококки, протеи, неспорообразующие анаэробы и их ассоциации, а в последнее время — условно-патогенная грамотрицательная микрофлора (эшерихии, протей, клебсиеллы). Инфекционные осложнения отмечаются у 1-8% родильниц.
Основные возбудители послеродовых гнойно-септических осложнений
Аэробы
- Стрептококки групп А, В.
- Энтерококки.
Грамотрицательные бактерии:
- Escherichia coli;
- Klebsiella;
- Proteus sp.;
- Staphylococcus aureus;
- Staphylococcus epiderm;
- Gardnerella vaginalis. Анаэробы
- Peptococcus sp.
- Peptostreptococcus sp.
- Bacteroides fragilis
- Prevotella sp.
- Clostridium sp.
- Fusobacterium sp.
- Mobiluncus sp. Другие
- Mycoplasma sp.,
- Chlamydia trachomatis,
- Neisseria gonorroeae.
Послеродовую инфекцию следует заподозрить, если в течение первых 10 сут после родов (за исключением первых 24 ч) температура тела на протяжении 2 сут подряд достигает 38 °С при измерении температуры не менее четырех раз в сутки.
Обследование лихорадящих больных:
- анамнез;
- анализ течения родов;
- клинический анализ крови;
- общий анализ и посев мочи;
- посев отделяемого из полости матки.
Гнойно-воспалительные послеродовые заболевания в зависимости от распространения патологического процесса разделяют на четыре этапа.
- Первый этап — инфекция ограничена областью родовой раны: послеродовая язва на промежности, стенке влагалища и шейке матки, лохиометра.
- Второй этап — инфекция распространяется за пределы раны, но остается локализованной: эндометрит, параметрит, отграниченный тромбофлебит (метротромбофлебит, тазовый тромбофлебит, тромбофлебит вен ног), аднексит, пельвиоперитонит.
- Третий этап — инфекция по клиническим проявлениям сходна с генерализованной: разлитой послеродовый перитонит, прогрессирующий тромбофлебит.
- Четвертый этап — генерализованная инфекция: сепсис без видимых метастазов, сепсис с метастазами, септический шок.
К этой группе послеродовых заболеваний относится также мастит.
ЛОХИОМЕТРА
Лохиометра (lochiometra) — лихорадочное заболевание, развивающееся в результате задержки в матке выделений (лохий).
Это заболевание возникает на 5-9-й день после родов, как правило, с явлениями эндометрита, вследствие закрытия цервикального канала задержавшимися плодными оболочками, сгустками крови или резкого перегиба матки при ее плохой сократительной способности. Начало заболевания острое, сопровождается повышением температуры тела до 39-40 °С, тахикардией, нередко ознобом. Выделения из матки прекращаются. Температура держится 1-2 дня. При бимануальном акушерском исследовании стенки матки неравномерно утолщены за счет чрезмерного растяжения области плацентарной площадки. Диагноз подтверждается также с помощью УЗИ.
Лечение состоит в применении спазмолитиков (но-шпа, папаверин и др.) с последующим введением через 15-20 мин сокращающих матку средств. При отсутствии эффекта от медикаментозной терапии производят инструментальное опорожнение матки кюреткой или вакуум-аспирацию. Параллельно осуществляют дезинтоксикационную терапию. Прогноз благоприятен. При несвоевременном лечении возможно развитие эндометрита. Профилактика состоит в правильном ведении родов и послеродового периода.
ПОСЛЕРОДОВЫЕ ЯЗВЫ
Послеродовая язва промежности
Частота расхождения швов промежности — до 0,5% (Ramin и соавт., 1992).
Послеродовые язвы представляют собой инфицированные раны промежности, слизистой оболочки влагалища, шейки матки. Границы их четкие, слегка отечные, с воспалительной гиперемией и инфильтрацией окружающих тканей. Дно язвы покрыто грязно-серым или серожелтым налетом с участками некроза.
Клиника заболевания определяется в основном местными проявлениями: локальной болезненностью, зудом, связанным с раздражением кожи отделяемым из раны, иногда дизурическими явлениями.
Лечение заключается в назначении антибактериальной терапии, местном применении антисептических и противовоспалительных средств. Рана обрабатывается перекисью водорода, гипертоническим раствором хлорида натрия. Хорошие результаты дает применение ферментов (трипсин, химотрипсин) для удаления некротических и фибринозных налетов и ускорения регенерации и эпителизации.
Протокол предоперационной подготовки к наложению вторичных швов при расхождении швов промежности (Ramin и Gilstrap, 1994)
- Антибактериальная терапия (внутривенно или внутримышечно).
- Удаление швов, полное раскрытие раны.
- Седативная и обезболивающая терапия по показаниям.
- Обработка раны:
- — аппликации на рану 2% геля лидокаина;
- — удаление всех некротизированных тканей;
- — обработка антисептическими растворами (перманганат калия, повидон-йод, гипертонические растворы и др.);
- — мазевые аппликации (левомиколь и др.);
- — протеолитические ферменты.
- Механическая подготовка кишечника перед хирургическим вмешательством, особенно при восстановлении разрывов промежности III степени.
ПОСЛЕРОДОВОЙ ЭНДОМЕТРИТ
Послеродовый эндометрит (метроэндометрит, эндомиометрит) представляет собой воспаление слизистой оболочки матки, к которому обычно присоединяется в той или иной степени воспаление ее мышечного слоя. Частота заболевания составляет от 36,3 до 59,5% всех послеродовых инфекций. Основные возбудители — грамотрицательная микрофлора и анаэробы, которые высеваются почти у 90% больных.
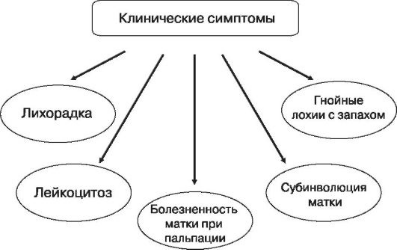
Факторы риска послеродового эндометрита
- Кесарево сечение.
- Длительный безводный промежуток.
- Затяжные роды.
- Частые влагалищные исследования.
- Прямая КТГ.
- Низкий социально-экономический статус.
- Анемия.
- Ожирение.
- Мекониальные воды.
- Многоплодие.
По клиническим проявлениям различают четыре формы эндометрита: классическую, абортивную, стертую и эндометрит после кесарева сечения.
Эндометрит классической, или типичной, формы начинается на 3-5-е сутки после родов, проявляется симптомами общей интоксикации, увеличением размеров матки, чувствительностью ее при пальпации. Выделения из цервикального канала мутные, с характерным зловонным запахом, умеренные или обильные. Заболевание, вызванное анаэробной флорой, отличается ранним началом, тяжелым течением, более выраженными признаками общей интоксикации организма.
Для абортивной формы эндометрита характерно появление симптомов заболевания на 2-4-е сутки послеродового периода. Особенность этой формы — быстрое уменьшение и исчезновение симптомов благодаря интенсивной терапии.
Эндометрит стертой формы начинается сравнительно поздно — на 5-7-е сутки после родов, характеризуется затяжным, без четкой клинической симптоматики течением. Эту форму отличают рецидивирующее течение, запоздалые диагностика и лечение, в последующем возможна генерализация инфекции.
Эндометрит после операции кесарева сечения начинается на 1-5-е сутки. Для него характерны как общие признаки интоксикации, так и местные проявления. При тяжелом течении заболевания реакция со стороны организма и клинические проявления могут соответствовать таковым при перитоните, что обусловлено выраженными нарушениями гомеостаза. Вовремя начатые интенсивная терапия и коррекция предотвращают дальнейшее развитие патологического процесса и генерализацию инфекции.

Поскольку стертые и абортивные формы эндометрита в последнее время превалируют над классической, только комплексное обследование всех органов и систем (дыхание, кровообращение, иммунитет, выделительная функция почек, кислотно-щелочное состояние, водно-электролитный баланс и т.д.) дает необходимую информацию о состоянии больной и позволяет адекватно подобрать необходимые методы и компоненты специфической и общей терапии.
У больных с послеродовым эндометритом в анализах крови наблюдается увеличение СОЭ, повышение количества лейкоцитов со сдвигом формулы влево.
Качественное и количественное бактериологическое исследование содержимого полости матки позволяет подобрать наиболее рациональный антибактериальный препарат.
Большое диагностическое значение имеет срочное гистологическое исследование последа. При наличии в нем воспалительных изменений (базального децидуита) следует учитывать возможность развития эндометрита.
Коагулограмма отражает повышенную готовность организма к возникновению ДВС-синдрома (увеличенное содержание фибриногена — более 5 г/л, снижение фибринолитической активности крови – менее 10%).
При цитохимическом исследовании лейкоцитов крови выявляются повышенные уровни щелочной фосфатазы и увеличенные показатели НСТ-теста (реакция восстановления нитросинего тетразолия).
При допплерографическом исследовании органов малого таза наблюдаются усиление интенсивности кровоснабжения, ускорение кровотока в артериях малого таза, застой и затрудненный отток крови в венах. Температура в полости матки несколько повышена — 37,5 °С и более.
При ультразвуковом исследовании матки определяется нарушение ее сократительной активности, о чем свидетельствует отсутствие разницы при измерении размеров тела и полости матки в динамике послеродового периода. При эндометрите полость матки можно визуализировать в течение 2 нед после родов.
Гистероскопия в послеродовом периоде позволяет видеть непосредственно внутреннюю поверхность матки и практически не имеет противопоказаний для выполнения. При исследовании наблюдаются три вида поражения полости матки: 1) истинный эндометрит — на стенках матки белесоватый налет как следствие воспалительного процесса, причем выраженность этого налета и площадь поражения полости матки зависят от продолжительности и тяжести процесса; 2) эндометрит с некрозом децидуальной ткани — эндометрий в виде структур черного цвета, тяжей и несколько выбухающий над поверхностью стенки матки; 3) эндометрит с задержкой частей плаценты — наблюдается ткань в виде бугристых структур синеватого оттенка с четкими контурами, резко выделяющаяся на фоне матки.
Своевременное и комплексное лечение послеродового эндометрита — основное условие, определяющее предупреждение дальнейшего распространения патологического процесса. Интенсивная терапия заболевания заключается как в общем воздействии на организм, так и в местном лечении. Адекватное местное лечение — важнейший момент, который позволяет ликвидировать очаг инфекции в организме и по возможности сохранить матку. Обязательно удаление из полости матки морфологического субстрата, на котором развивается воспаление. Этим субстратом являются остатки плацентарной ткани либо (в большинстве случаев) децидуальная ткань с различной степенью некроза и лейкоцитарной инфильтрацией. Удаление патологических включений из полости матки производится путем бережного кюретажа или вакуум-аспирации с последующим промыванием дезинфецирущим раствором. После этих манипуляций должны быть созданы условия для свободного оттока отделяемого из полости матки.
Еще один из методов местной терапии послеродового эндометрита — промывное дренирование. В матку вводится катетер, через который производится промывание и орошение ее полости и стенок растворами антисептиков, антибиотиков и т.д. При необходимости применяют аспирационно-промывное дренирование с помощью двухпросветного или двойного катетера. Один из них (приточный) вводится до дна матки, другой (дренажный) — на 6-7 см от внутреннего зева. Через приточный катетер подается охлажденный до температуры 4 °С раствор фурацилина со скоростью 10 мл в минуту.
Кроме местного лечения очага инфекции, необходима интенсивная общая терапия.
Обязательный компонент ее — применение антибактериальных средств, лучше при условии определения возбудителя в содержимом полости матки, а также с учетом чувствительности выделенной микрофлоры к антибиотикам.
Так как в последнее время послеродовый эндометрит вызывается полимикробной аэробной и анаэробной флорой, целесообразно лечение препаратами широкого спектра действия. Необходимо учитывать тот факт, что даже у одной больной в процессе лечения чувствительность возбудителей заболевания к антибиотикам может меняться, поэтому нельзя применять один препарат в течение длительного времени (более 7-8 дней), а при отсутствии положительного эффекта в течение 3-4 дней его также необходимо заменить.
В настоящее время для лечения послеродового эндометрита наиболее часто используют следующие антибиотики:
- ампициллин — по 1 г 4-6 раз в сутки внутримышечно;
- оксациллин — по 0,5-1 г 4-6 раз в сутки внутримышечно (до 6 г в сутки);
- клафоран — по 1 г 2 раза в сутки внутримышечно или внутривенно (до 4 г в сутки);
- кефзол — по 0,5-1 г 3-4 раза (до 6 г в сутки) внутримышечно или внутривенно;
- цефазолин — по 1-2 г 4 раза внутримышечно или внутривенно;
- амикацин — по 0,5 г каждые 8 ч внутримышечно или внутривенно (до 1,5 г в сутки);
- гентамицин — по 80 мг внутримышечно или внутривенно каждые 8-12 ч (до 240 мг в сутки).
Весьма эффективно применение клиндамицина (далацин-С, клеоцин) по 300 мг 2-3 раза в сутки внутримышечно или внутривенно в суточной дозе 600-900 мг, при необходимости дозу можно увеличивать до 2400 мг в сутки.
Кроме антибиотиков, для комплексной антибактериальной терапии необходимы и другие препараты. Хорошей переносимостью и относительно слабой токсичностью обладает метронидазол (метрожил) — по 500 мг 2-3 раза в сутки внутривенно. Перорально можно использовать трихопол (флажил) — по 0,25 г 3 раза в день или тинидазол — в суточной дозе 2 г однократно. Заслуживает внимания лизоцим — фермент, который, кроме антибактериальной активности, обладает способностью стимулировать неспецифические факторы защиты организма. Применяется лизоцим в дозе 100-250 мг внутримышечно дважды в сутки. При непереносимости антибиотиков или при сочетанной мочеполовой инфекции целесообразно назначение препаратов нитрофуранового ряда — фурагина, фурадонина, фуразолидона — по 0,1-0,2 г 3 раза в сутки в таблетках или 300-500 мл 1% раствора фурагина (солафура) внутривенно капельно медленно 1-2 раза в сутки.
При послеродовом эндометрите большое значение имеет также адекватная дезинтоксикационная инфузионная терапия, которую необходимо проводить дифференцированно, с учетом степени нарушения коллоидно-онкотического состояния крови. Объем вводимой жидкости при ненарушенной выделительной функции почек должен составлять 30 мл на 1 кг массы тела в сутки. При повышении температуры тела на один градус необходимо добавлять 5 мл на 1 кг веса в сутки.
Следовательно, общий объем вводимой за сутки жидкости при нормальной функции почек (не менее 60 мл в час) должен составлять 2500-3000 мл. При осложнениях или генерализации процесса количество жидкости может быть увеличено до 5000-6000 мл. Показано введение 5%, 10%, 20% растворов глюкозы объемом 1000-1500 мл с одновременным добавлением инсулина из расчета 1 ЕД на 4 г сухого вещества глюкозы. Введение глюкозы способствует нормализации энергетического баланса организма.
Белковые препараты необходимо назначать из расчета 1-1,5 г нативного белка на 1 кг массы тела больной. Альбумин вводится внутривенно капельно в виде 5%, 10%, 20% раствора по 200-500 мл, плазма крови — по 200-250 мл, аминопептид или интралипид — по 500 мл. При нарастании явлений интоксикации следует проводить коррекцию минерального обмена. Обычно вводится раствор калия, количество которого зависит от содержания его в крови. В качестве инфузионных сред можно использовать физиологический раствор, раствор Рингера, ацесоль, хлосоль. Гемосорбция, лимфосорбция, плазмаферез, форсированный диурез под контролем электролитного баланса с соответствующим восполнением дефицита калия и натрия также способствуют дезинтоксикации.
Так как послеродовые гнойно-септические осложнения развиваются на фоне недостаточности иммунной системы, обязательно применяют стимуляторы защитных сил организма — тималин, тимоген, тактивин, спленин и т.д.
Важный момент в развитии послеродовых заболеваний — нарушение свертывающей системы крови, что в свою очередь составляет одно из основных звеньев в патогенезе ДВС-синдрома. Поэтому для лечения и профилактики коагулопатий в комплекс проводимой терапии необходимо включать гепарин внутривенно путем непрерывной перфузии в суточной дозе 20 000-30 000 ЕД или по 5 000 ЕД с интервалами 4-6 ч. Бывает вполне достаточно подкожного введения минимальных доз гепарина по 2500-3000 ЕД через 4-6 ч под контролем времени свертывания крови, в последнее время используют низкомолекулярный гепарин: фраксипарин, клексан 1 или 2 раза в сутки.
Поскольку при послеродовом эндометрите в крови увеличивается содержание гистамина и гистаминоподобных веществ, рекомендуется применение десенсибилизирующих препаратов — димедрола, супрастина, пипольфена, тавегила, фенкарола.
Гидрокортизон, преднизолон и другие гормональные препараты применяются только по показаниям при генерализации воспалительного процесса.
Один из важных моментов комплексного лечения — использование витаминов А, С, К и группы В. Вначале их вводят парентерально, а затем можно и внутрь. Введению аскорбиновой кислоты должно предшествовать введение унитиола — 5% раствор по 5-10 мл. Аскорбиновая кислота после введения довольно быстро метаболизируется и образует дикетогулоновую и дигидроаскорбиновую кислоты, которые обладают выраженным токсическим свойством. Унитиол способствует пролонгированию действия аскорбиновой кислоты. Кроме того, унитиол связывает тиоловые яды, образуя нетоксичные соединения, выводимые с мочой. Связывание и удаление из организма ядов способствует нормализации метаболических процессов организма и восстановлению его ферментных систем. Своевременное и полноценное комплексное лечение послеродового эндометрита — основа профилактики распространенных генерализованных форм заболеваний у родильниц.
При распространении инфекции за пределы матки (рис. 103) наступает следующий этап в развитии послеродовых гнойновоспалительных заболеваний с появлением местных процессов в малом тазу и образованием инфильтратов и опухолей воспалительного генеза.
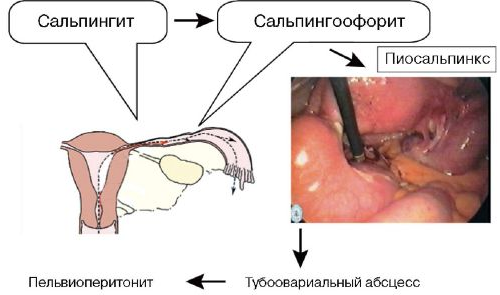
Рис. 103. Распространение инфекционного процесса
В случае распространения инфекции по маточной трубе развивается сальпингит, а при вовлечении в процесс яичника — оофорит. Послеродовые септические сальпингоофориты возникают чаще всего с одной стороны. При запаивании обоих концов маточной трубы патологическое отделяемое может накапливаться в ее просвете с образованием в последующем гидроили пиосальпинкса. Далее могут возникать тубоовариальные абсцессы. При вовлечении в патологический процесс придатков ухудшается общее состояние больной, появляется лихорадка, усиливаются боли в нижних отделах живота, имеют место симптомы раздражения брюшины, особенно при образовании пиосальпинксов.
Иногда в воспалительный процесс вовлекается тазовая брюшина, и тогда развивается послеродовый пельвиоперитонит. При этом выпот в брюшной полости может быть серозным, серозно-фибринозным, но чаще всего он гнойный. При пельвиоперитоните явления общей интоксикации и симптомы раздражения брюшины более выражены.
Для пельвиоперитонита характерна следующая клиническая картина: высокая температура, резкая тахикардия, тошнота и рвота, задержка газов и стула, положительные симптомы раздражения брюшины. Налицо все признаки общего перитонита. Но благодаря строению брюшины процесс постепенно локализуется, образуются спайки, ограничивающие распространение воспаления, уменьшаются явления интоксикации, нормализуется функция кишечника, и при вагинальном исследовании можно установить наличие выпота в брюшной полости.
При распространении воспалительного процесса на околоматочную клетчатку развивается параметрит.
ПАРАМЕТРИТ
Параметрит (parametritis) — воспаление околоматочной клетчатки (параметрия). Возбудители параметрита — кишечная палочка, клебсиелла, протей, меньшую роль играют стрептококки, золотистый стафилококк, неспорообразующие анаэробы (бактероиды, пептококки, пептострептококки), гонококки. Нередко микрофлора носит ассоциированный характер.
В послеродовом периоде инфекция проникает в клетчатку чаще всего из разрывов шейки матки и верхней трети влагалища, редко из плацентарной площадки. Боковые разрывы шейки матки III степени после родов или позднего выкидыша (нераспознанные и неушитые или неправильно ушитые) иногда осложняются гематомой между листками широкой связки матки. Последующее инфицирование такой гематомы вовлекает в патологический процесс околоматочную клетчатку с развитием параметрита. Гнойный параметрит может формироваться при послеродовом тромбофлебите вен параметрия в результате гнойного расплавления инфицированных тромбов. В некоторых случаях параметрит возникает при перфорации матки во время искусственного аборта. Хронический параметрит часто наступает после воздействия на организм неспецифических факторов, например холода. Предрасполагающими к развитию параметрита факторами вне беременности могут быть: расширение канала шейки матки; диагностическое выскабливание; операции на шейке матки; введение внутриматочной спирали, осложненное травматизацией стенок матки; удаление интралигаментарно расположенной опухоли. Микробы могут попадать в параметральную клетчатку различными путями, но чаще всего — по лимфатическим сосудам из матки.
В течении параметрита различают три стадии: инфильтрации, экссудации и уплотнения экссудата. В начальной стадии воспаления отмечаются расширение сосудов, периваскулярный отек и мелкоклеточная инфильтрация клетчатки. В стадии экссудации происходит массивный выход из сосудистого русла лейкоцитов и других форменных элементов крови, инфильтрат доходит до стенок таза. Воспалительный экссудат богат фибриногеном. При превращении фибриногена в фибрин инфильтрат приобретает значительную плотность. Воспалительный процесс может локализоваться в пределах параметрия. Этому способствуют выпадение фибрина и блокада лимфатических путей в очаге воспаления, образование грануляционного вала вокруг него, наличие в клетчатке таза фиброзных образований, разграничивающих ее на отделы. При тяжелой инфекции перечисленных защитных приспособлений оказывается недостаточно, и инфекция распространяется на соседние органы и ткани. Если экссудат нагнаивается, возникает гнойный параметрит, который может сопровождаться прорывом гноя, чаще в прямую кишку или мочевой пузырь.
В зависимости от топографии клетчатки малого таза параметриты делятся на передние, боковые и задние. Наиболее часто встречаются боковые параметриты (70-75%), при которых воспалительный процесс сверху ограничивается верхним отделом широкой связки, снизу — нижним отделом кардинальных связок, сбоку — стенкой малого таза. При переднем параметрите инфильтрат определяется спереди от матки и сглаживает передний свод. Он может распространяться на предпузырную клетчатку и переднюю брюшную стенку. Задний параметрит представляет собой воспаление клетчатки между маткой и прямой кишкой. Инфильтрат плотно окутывает прямую кишку, нередко вызывая сужение ее просвета.
Воспаление всей клетчатки малого таза носит название пельвиоцеллюлита (pelviocellulitis).
По клиническому течению параметрит разделяют на острый, подострый и хронический.
Различают параметрит как отдельную форму заболевания (первичный параметрит) и как реактивное воспаление клетчатки при тромбофлебитах, аднекситах (вторичный параметрит).
Параметрит начинается на 10-12-й день после родов с озноба и повышения температуры до 38-39 °С и более, возможны слабость, головная боль. Внизу живота, в левой или правой подвздошной области (соответственно локализации процесса) возникают постепенно усиливающиеся боли. Они носят постоянный характер и иррадиируют в крестец и поясницу. Иногда боль внизу живота является наиболее ранним симптомом параметрита и предшествует появлению инфильтрата.
Сначала местные симптомы мало выражены, при влагалищном исследовании определяется пастозность в области воспаления. Спустя 2-3 дня отчетливо пальпируется инфильтрат тестоватой, а затем плотной консистенции. Он умеренно болезнен, неподвижен. При боковом параметрите инфильтрат располагается рядом с боковой поверхностью матки и переходит на боковую поверхность стенки таза. При этом происходит сглаживание бокового свода влагалища, и слизистая оболочка под инфильтратом быстро теряет подвижность. Матка отдельно от инфильтрата не пальпируется и смещена при одностороннем параметрите в противоположную сторону, а при двустороннем — кверху и кпереди. Продолжительность данной стадии — 5-10 дней.
Инфильтрат может выходить за пределы параметрия. При распространении кпереди он прощупывается снаружи над пупартовой связкой. Благодаря внебрюшинному расположению инфильтрата верхние пальпаторная и перкуторная границы его совпадают. При перкуссии верхнепередних остей подвздошных костей на стороне поражения отмечается приглушение тона (симптом Гентера). При переходе воспаления на околопузырную клетчатку инфильтрат порой распространяется по задней поверхности брюшной стенки, принимая форму треугольника с вершиной, обращенной к пупку. Из верхнего отдела параметрия инфильтрат порой продвигается позади брюшины вплоть до почечной области. При его локализации на поверхности поясничной мышцы (парапсоит) больная принимает щадящее положение: на спине с отведенной и согнутой ногой.
Течение параметрита различное. Лихорадочный период с небольшими периодами нормализации температуры продолжается 1-2 нед. Инфильтрат постепенно рассасывается, если же нет, то наблюдается его нагноение, и образуется абсцесс (на 3-4-й неделе заболевания). Температура тела поднимается до 39 °С и выше, отмечаются значительные колебания между утренней и вечерней температурой, характерны повторные ознобы, выражены явления интоксикации. При влагалищном исследовании в инфильтрате обнаруживают участки размягчения, свидетельствующие о его нагноении. Образовавшийся абсцесс может самопроизвольно вскрыться во влагалище, прямую кишку или мочевой пузырь, реже в брюшную полость или полость матки. В крови значительно нарастает лейкоцитоз, увеличивается сдвиг нейтрофилов влево, резко повышается СОЭ. При угрожающем прорыве в мочевой пузырь возникают частые позывы к мочеиспусканию, в прямую кишку — тенезмы, поносы. Если гнойник не вскрыт, гной прокладывает себе путь над пупартовой связкой, через седалищное отверстие между сосудами на ягодицу, под пупартовой связкой на бедро, в околопочечную область. На месте угрожающего прорыва гнойника сначала отмечается выпячивание, а затем покраснение кожи и флюктуация. При подостром параметрите клинические проявления менее выражены, чем при остром.
При развитии хронического параметрита у больной возникают жалобы на периодические тупые, ноющие боли внизу живота. При влагалищном исследовании определяют укорочение сводов и неправильное положение матки за счет спаечного процесса. Встречаются стертые формы параметрита, характеризующиеся невыраженностью, а иногда и отсутствием клинических симптомов.
Диагноз ставится на основании жалоб, данных анамнеза, клинической картины и лабораторных исследований. Тщательно выполненные влагалищное и ректальное исследования в большинстве случаев позволяют установить наличие заболевания. Гнойный параметрит диагностируют с помощью пункции заднего свода влагалища; высокорасположенные и недоступные для пункции абсцессы параметрия — путем ультразвукового сканирования.
Нагноение параметрального инфильтрата и прорыв гнойника в мочевой пузырь выявляют на основании исследования мочи и цистоскопии. Прорыв гнойника в прямую кишку устанавливают, обнаружив гной в каловых массах, а также используя ректоскопию.
Дифференциальный диагноз проводят с ретроцервикальным эндометриозом, пельвиоперитонитом, пиосальпинксом и пиоваром, гематомой параметрия, тромбофлебитом вен параметрия. Иногда дифференциальный диагноз труден, так как некоторые из этих заболеваний предшествуют параметриту или сочетаются с ним. Важный дифференциально-диагностическим признак параметрита — притупление перкуторного тона над верхней передней подвздошной остью на стороне поражения.
В ответ на проникновение возбудителей инфекции в начальной стадии болезни наступает расширение кровеносных и лимфатических сосудов. Появляется отек, имеющий тенденцию к нарастанию. В дальнейшем образуется воспалительный инфильтрат, окруженный валом грануляционной ткани, который является преградой для распространения возбудителей инфекции из первичного очага. В последующем возможно полное рассасывание инфильтрата, образование абсцесса, развитие фиброзных и рубцовых изменений.
Лечат острый параметрит с учетом причины и особенностей заболевания, обусловившего его развитие. Основу составляют общеукрепляющие, антибактериальные, десенсибилизирующие, дезинтоксикационные и симптоматические средства, а также физиотерапевтические процедуры. Иногда приходится прибегать к хирургическому вмешательству. Лечение проводится в стационарных условиях. Вначале обычно применяют антибиотики широкого спектра действия, а после определения чувствительности микробной флоры к антибиотикам назначают более эффективные препараты. При недостаточной эффективности терапии или отсутствии результатов через 5-7 дней антибиотик заменяют.
При тяжелом течении процесса и отсутствии результата от использования одного антибиотика прибегают к их сочетанию, что позволяет создать широкий антимикробный спектр действия.
При тяжелых формах заболевания предпочтительнее применять антибактериальные препараты, комплексно влияющие на аэробную и анаэробную инфекцию.
Для предупреждения развития дисбактериоза, кандидоза назначают нистатин (по 250 000 ЕД 4 раза в день) или леворин (по 200 000 ЕД 4 раза в день), дифлюкан 150 мг однократно и др.
Инфузионная терапия при параметрите направлена на коррекцию метаболических нарушений, борьбу с интоксикацией. Для повышения резистентности организма назначают гамма-глобулин, иммуностимуляторы, используют УФО крови и внутрисосудистую гелий-неоновую лазеротерапию.
При параметрите стафилококковой этиологии для повышения специфической иммунологической реактивности используют антистафилококковый гамма-глобулин, антистафилококковую плазму, адсорбированный стафилококковый анатоксин.
Применяют также препараты протеолитических ферментов (трипсин и химотрипсин), супрастин, димедрол, дипразин. При сильных болях показаны анальгезирующие и седативные средства.
При образовании в параметрии абсцесса проводят оперативное лечение. В случае нагноения инфильтрата с целью уточнения характера экссудата делают его пункцию через свод влагалища в месте наиболее низкого расположения гнойника. При появлении гноя его удаляют шприцем, полость промывают антисептическим препаратом или протеолитическим ферментом (химопсин, химотрипсин), а затем вводят антибиотики. При выпячивании заднего свода, а иногда и задней стенки влагалища показано срочное вскрытие свода с введением дренажа. Операцию чаще выполняют трансвагинальным путем, реже трансабдоминальным или прямокишечным. Пункцию абсцесса выполняют толстой длинной иглой на шприце. После получения гноя по ходу иглы (не извлекая ее) скальпелем рассекают стенку влагалища и капсулу абсцесса (задняя кольпотомия). Образовавшееся отверстие расширяют и в полость абсцесса вводят резиновую дренажную трубку с боковыми отверстиями (лучше Т-образную).
Лечение подострого параметрита проводят аналогично. При хроническом параметрите назначают фибринолитическую терапию, свечи с лидазой, ЛФК; показаны лазеротерапия, УФО аутокрови, вибротерапия, акупунктура, ручной массаж, бальнеотерапия. Больным хроническим параметритом рекомендовано санаторно-курортное лечение.
Прогноз при ранней диагностике и своевременном рациональном лечении благоприятный. При развитии хронического параметрита отмечается нарушение локальной гемодинамики и функции органов таза.
Профилактика параметрита заключается в предупреждении инфекционно-воспалительных осложнений после абортов и родов, а также гинекологических заболеваний; в борьбе с внебольничными абортами; в рациональном ведении родов и послеродового периода; в своевременном лечении послеродового и послеабортного эндометрита.
ТРОМОЭМБОЛИЧЕСКИЕ ОСЛОЖНЕНИЯ
Тромбофлебит (thrombophlebitis) — заболевание вен, характеризующееся воспалением венозной стенки и тромбозом. Вначале может возникать воспаление венозной стенки (флебит), а затем тромбоз, либо, наоборот, — тромбоз и вслед за ним воспаление вены (флеботромбоз).
Роль инфекции в развитии тромбофлебита сложная. Некоторые исследователи считают, что возбудитель инфекции влияет непосредственно на стенку вены, попадая в нее либо с током крови, либо из близлежащего воспалительного очага. Другие рассматривают действие инфекции как общетоксическое, поражающее всю сосудистую систему, нарушающее функцию свертывающей и противосвертывающей системы крови. Если в гнойный процесс вовлекаются питающие венозную стенку сосуды (vasa vasorum), может произойти гнойное расплавление вены.
Острый тромбофлебит — одно из наиболее серьезных осложнений послеродового периода. Возникновению его у родильниц способствуют затяжные и осложненные роды, травмы родовых путей, акушерские операции, постгеморрагическая анемия, послеродовый метроэндометрит, гиперкоагуляция, варикозная болезнь, ожирение, гестоз.
В развитии тромбофлебита важное значение имеют изменение внутренней поверхности сосудистой стенки, повышение свертываемости крови, замедление тока крови, а также рефлекторный спазм сосудов, способствующий замедлению кровотока и повреждению сосудистой стенки. После родов предпосылки к тромбозу следующие: повышение свертываемости крови ко времени родов, развитие застойных явлений в обширной сосудистой сети малого таза, замедление тока крови в венах нижних конечностей. Опасность тромбоза возрастает при сердечно-сосудистых заболеваниях, варикозном расширении вен, ожирении, анемии, позднем гестозе, после затяжных родов и оперативных вмешательств.
Патогенез тромбофлебита различен. У большинства больных острый тромбофлебит не есть следствие гнойного воспаления венозной стенки; он возникает из-за воздействия комплекса факторов, среди которых ведущее значение имеет венозный застой в сочетании с тромботическим состоянием системы гемостаза — гиперкоагуляцией, гипофибринолизом и усилением адгезивно-агрегационных свойств форменных элементов крови. Сравнительно редко в клинической практике наблюдаются случаи истинного септического тромбофлебита, формирующегося на фоне гнойного воспаления вены с последующим тромбообразованием или вследствие вторичного инфицирования венозного тромба и гнойного его расплавления.
Флебит — воспаление стенки вены, которое чаще развивается при общей или местной гнойной инфекции. При понижении реактивности организма, замедлении кровотока, повреждении венозной стенки, изменении состава крови и повышении ее свертываемости создаются благоприятные условия для оседания микробов на внутренней поверхности сосуда, что ведет к ее воспалению (эндофлебит). Поражение венозной стенки воспалительным процессом может происходить и другим путем, когда инфекция переходит из расположенного рядом воспалительного очага на наружную стенку вены (перифлебит). В обоих случаях в воспалительный процесс вовлекается вся венозная стенка. Раздражение, вызванное травмой, микробами, циркулирующими в крови, оказывает влияние на нервные окончания, заложенные в стенках сосудов, вследствие чего возникает спазм вен. В свою очередь это приводит к замедлению тока крови и образованию тромба. В таких случаях возникает тромбофлебит. Тромб также раздражает нервные окончания венозной стенки, что способствует спазму основного ствола и коллатералей. Спазм и тромбоз вен влекут за собой повышение венозного давления не только в венах, но и в капиллярах, приводящего к увеличению проницаемости капилляров и к отеку конечности.
Послеродовые тромбофлебиты делятся на тромбофлебиты поверхностных и глубоких вен. Последние в свою очередь подразделяются на: метротромбофлебиты; тромбофлебиты вен таза; тромбофлебиты вен ног (подвздошно-бедренные, бедренные, глубоких вен голени и пр.).
По клиническому течению следует различать острую, подострую и хроническую стадии тромбофлебита, по характеру процесса — гнойный и негнойный тромбофлебит. Кроме того, выделяют первичные и рецидивирующие, распространенные и ограниченные (сегментарные) тромбофлебиты.
Тромбофлебиты чаще всего развиваются на 2-3-й неделе после родов, реже — на 5-6-й день; нередко им предшествует длительный субфебрилитет.
К клиническим предвестникам тромбофлебита (точнее, образования тромба) относятся ступенеобразное учащение пульса («лестничный» пульс), стойкое учащение его, болевые ощущения в нижних конечностях: боли в икроножных мышцах при вставании, ходьбе, при дорсальной флексии стопы, спонтанные боли по ходу вены, боли при надавливании на икроножные мышцы, подошву стопы, по обе стороны ахиллова сухожилия, а также положительная проба с манжеткой. Ценны результаты определения коагулирующих и антикоагулирующих свойств крови (в частности, выявление фибриногена В), а также тромбоэластография. В клинической картине различных форм отграниченного тромбофлебита имеется много общего. Состояние больных обычно удовлетворительное. Температура держится в пределах 37-38,5 °С, пульс учащен (нередко до 100 ударов в минуту и более). В начале заболевания наблюдается однократный озноб. В крови чаще всего обнаруживается незначительный лейкоцитоз, умеренный сдвиг лейкоцитарной формулы влево, сравнительно небольшое повышение СОЭ.
Тромбофлебит поверхностных вен характеризуется яркой клинической симптоматикой и нетруден для диагностики. Как правило, он развивается на почве варикозного расширения вен нижних конечностей. В ряде случаев это заболевание — следствие введения лекарственных средств в вены стопы. При поверхностном тромбофлебите определяется шнуровидный тяж по ходу подкожной вены, в зоне которого видна полоса гиперемии и отмечается резкая болезненность при пальпации. Процесс чаще развивается в большой подкожной вене и очень редко поражает малую подкожную вену. Длительность заболевания — от 2 до 4 нед. Иногда образуется значительный перифокальный инфильтрат вследствие вовлечения в воспалительный процесс окружающей вену подкожной жировой клетчатки. В ряде случаев наблюдается большой отек мягких тканей в области лодыжек. Если отек значительный и распространяется на голень и бедро, то следует заподозрить сопут-ствующий тромбоз глубоких вен.
Прогрессирование эндомиометрита нередко вызывает метротромбофлебит. Диагностика его часто затруднена. Следует обращать внимание на учащение пульса, субинволюцию матки, длительные обильные кровянистые выделения из половых путей. Иногда при бимануальном акушерском исследовании обнаруживается фасетчатая поверхность матки или на ней определяются характерные извитые тяжи.
Тромбофлебит вен таза выявляется обычно через 2 нед после родов. При влагалищном исследовании определяется плохо сократившаяся матка. При поражении вен нижней венозной системы они нередко прощупываются в основании широкой связки и на боковой стенке таза в виде болезненных плотных и извитых тяжей.
При переходе процесса на клетчатку, окружающую вены, образуются небольшие инфильтраты (вторичный параметрит). При поражении вен яичникового сплетения (верхней венозной системы) имеется повышенная опасность эмболии. При влагалищном исследовании в области придатков определяется небольшой инфильтрат, напоминающий воспалительно измененные придатки.
Развитие подвздошно-бедренного (илеофеморального) венозного тромбоза у родильниц имеет свои особенности. Первично вовлекаются в процесс мелкие ветви внутренней подвздошной вены, что на начальных этапах является следствием физиологического тромбоза вен плацентарной площадки. Далее тромбоз постепенно распространяется на ствол внутренней подвздошной вены и через ее устье — в общую подвздошную вену. Этот период наиболее опасен в отношении возникновения тромбоэмболии легочной артерии, так как в общей подвздошной вене, диаметр которой значительно больше, чем внутренней, образуется флотирующий (плавающий) тромб, представляющий собой потенциальный эмбол. Если эмболии не произошло, наступает тромботическая окклюзия общей подвздошной вены с блокадой кровотока в ней, и процесс распространяется на весь подвздошно-бедренный венозный сегмент. Период распространения тромбоза на общую подвздошную вену протекает латентно из-за отсутствия выраженных нарушений кровотока в магистральных венах таза. На этом этапе клиническая симптоматика неспецифична и характеризуется необъяснимой лихорадкой и тахикардией (признак Малера), нередко — выраженными болями в нижних отделах живота и крестцовой области, иногда наблюдаются дизурические явления. Если в послеродовом периоде возникает пневмония (в особенности плевропневмония), то необходимо исключить ее эмболический генез. По мере распространения тромбоза на подвздошнобедренный сегмент появляются боли и болезненность при пальпации по ходу сосудов нижних конечностей, развивается быстро нарастающий отек ноги, который захватывает всю нижнюю конечность от стопы до паховой складки. У некоторых больных отмечается отек ягодицы, наружных половых органов. Кожа на пораженной конечности цианотична. Цианоз может распространяться на ягодичную область, нижние отделы живота, иногда ограничивается областью голени. Усиление рисунка подкожных вен на бедре и особенно в паховой области — очень важный симптом острого илеофеморального венозного тромбоза.
При остром тромбофлебите глубоких вен бедра в первые дни заболевания возникает сильная боль, температура повышается до 39-40 °С, быстро развивается отек конечности. На бедре по ходу сосудистого пучка отмечается резкая болезненность. На голени боли появляются в проекции глубоких вен (в области икроножных мышц). Окружность бедра пораженной конечности больше, чем окружность здоровой конечности, на 8-15 см. Кожа на больной конечности блестящая, чаще с цианотичным мраморным оттенком, при надавливании пальцем на передней поверхности голени остаются ямки. Конечность на ощупь холоднее по сравнению со здоровой. Температура кожи в области стопы и пальцев на 1,5- 2 °С ниже. Пульс на артериях пораженной конечности отсутствует или значительно ослаблен, что объясняется спазмом магистральных артерий. Регионарные лимфатические узлы увеличены. Вследствие нарушения кровообращения развивается коллатеральная венозная сеть в подвздошной, паховой области и на бедре. В некоторых случаях единственный симптом острого тромбоза глубоких вен голени — боль в икроножных мышцах. Иногда отмечается умеренный отек в области лодыжек. Наиболее выраженный признак острого тромбоза глубоких вен голени — симптом Хоманса, выявляемый следующим образом. Больная лежит на спине, ноги полусогнуты в коленных суставах. Производят тыльное сгибание стопы в голеностопном суставе. Боль в икроножных мышцах, которую при этом ощущает больная, свидетельствует о тромбозе глубоких вен голени, имеющем тенденцию к распространению в проксимальном направлении.
Заболевание продолжается от 3 нед до 2,5 мес и более. Если в процесс вовлекаются бедренная вена и подвздошный сегмент, развивается клинический симптомокомплекс илеофеморального тромбоза.
Острый тромбофлебит как глубоких, так и поверхностных вен может перейти в гнойный, при этом возникают множественные абсцессы и флегмоны по ходу пораженных вен. Гнойный тромбофлебит является чаще осложнением гнойного процесса и характеризуется высокой температурой; ознобом; тяжелым общим состоянием; гиперемией кожи, болезненностью и очагами размягчения (флюктуация) по ходу вены. Если не наступает полного излечения, тромбофлебит чаще из острой стадии переходит в подострую или, минуя подострую, — в хроническую стадию.
Подострый тромбофлебит — переходная стадия от острого процесса к хроническому. Течение: боли постепенно утихают, температура снижается до субфебрильной или нормальной, значительно уменьшается отечность конечности. При тромбофлебите глубоких вен по ходу сосудистого пучка пальпаторной болезненности не отмечается. Уплотнения и инфильтраты определяются по ходу вен на небольшом протяжении или совсем не выявляются. При полной нагрузке на больную конечность наблюдается небольшая болезненность. При хождении и стоянии отек может увеличиваться. Длительность процесса в среднем 1,5-2 мес, а иногда — 4-6 мес. Продолжительность тромбофлебита глубоких вен нижних конечностей составляет в среднем 4-6 нед. Лихорадочный период длится от нескольких дней до 2-3 нед. Лихорадка обычно сменяется субфебрилитетом. Развитие тромбофлебита на другой ноге является обострением заболевания, ее поражение чаще происходит через 10-12 дней.
После перенесенного тромбофлебита нередко возникают осложнения (посттромбофлебитический синдром — хроническая венозная недостаточность в 20-40% случаев). Боли в пораженных конечностях обычно появляются вследствие сдавления нервных стволов или распространения на них воспалительного процесса. Одно из наиболее тяжелых осложнений при тромбофлебите крупных вен — эмболия сосудов различных органов, нередко вызывающая инфаркты соответствующей локализации.
После перенесенного тромбофлебита иногда развивается хроническая венозная недостаточность, которая протекает длительно — от нескольких месяцев до 1-2 лет и более. По ходу пораженных вен определяются плотные прерывистые шнуры в виде четок на отдельных участках, безболезненные или несколько болезненные при пальпации. После длительной ходьбы, особенно при поражении глубоких вен, появляются небольшая отечность голени и стопы, напряжение и пастозность мягких тканей. Резкие движения в конечностях вызывают болезненные ощущения. При хронической венозной недостаточности возникают частые обострения тромбофлебита, в основном при варикозном расширении вен, когда наблюдаются трофические расстройства, сухость и шелушение кожных покровов в области голеней, варикозные язвы.
Диагноз ставят на основании анамнеза и тщательного клинического обследования родильницы (осмотр, пальпация, определение пульсации на периферических сосудах, сравнительное измерение окружности конечностей и т.д.). Помимо клинических признаков, большое значение имеют дистальная флебография, антеградная и ретроградная илеокавография, допплерометрическое исследование кровотока, а также исследование с меченым фибриногеном. Косвенная оценка активности тромбообразования может быть произведена путем анализа состояния системы гемостаза. Наиболее информативные тесты — тромбоэластограмма, коагулограмма. Сегментарная окклюзия венозной магистрали на коротком протяжении или флотирующий тромб выявляются только с помощью рентгеноконтрастного метода исследования. При необходимости используют лучевые способы диагностики: флебографию, термографию, радиоизотопное исследование.
Острый тромбофлебит глубоких вен конечностей, сопровождающийся отсутствием или ослаблением пульсации на периферических сосудах, следует дифференцировать с тромбоэмболией и тромбозом артерий — острой артериальной непроходимостью. Закупорка тромбом магистрального венозного ствола приводит к рефлекторному спазму ближайшей артерии, что клинически иногда напоминает артериальную непроходимость. При эмболии артерий явления непроходимости наступают сразу, а при тромбофлебите только к концу 1-х суток появляются отек конечности и цианоз кожи, в то время как при артериальной непроходимости наблюдается бледность кожи. Иногда при тромбофлебите спастические изменения артерии выражены слабо.
Подострый тромбофлебит глубоких вен голени может иметь некоторое сходство с начальной стадией облитерирующего эндартериита. В отличие от тромбофлебита, эндартериит характеризуется перемежающейся хромотой, трофическими расстройствами на стопе. Эндартериит развивается постепенно. Болезнь Рейно также имеет некоторое сходство с тромбофлебитом. Для нее свойственны симметричное поражение кожи, цикличность болевых приступов. Эти симптомы отсутствуют при тромбофлебите.
Тромбофлебит поверхностных вен следует дифференцировать с мигрирующим тромбофлебитом и лимфангитом. При мигрирующем тромбофлебите процесс развивается одновременно на двух конечностях, быстро возникают тромбы, узелки на свежих участках. При лимфангите имеет место гиперемия кожи в виде полосы по ходу лимфатических сосудов, но уплотнений по ходу поверхностных вен, наблюдаемых при тромбофлебите, не отмечается.
Особенности морфогенеза тромбофлебита зависят от взаимоотношения процессов воспаления и тромбоза. Эндофлебит в сочетании с тромбозом называют эндотромбофлебитом. Тромбофлебит, развивающийся на основе перифлебита, именуется перитромбофлебитом.
При эндотромбофлебите стенка вены гиперемирована, отечна, внутренний ее слой умеренно инфильтрирован полиморфно-ядерными лейкоцитами. Эндотелиальный слой стенки отсутствует, к ней прилежат тромботические массы, в ряде случаев внутренние слои стенки расплавлены, ее структурные элементы в этих местах не прослеживаются, непосредственно к некротизированным тканям прилежит тромб, содержащий большое число лейкоцитов.
При перитромбофлебите в первую очередь поражаются наружная оболочка стенки вены и vasa vasorum. Стенка вены утолщена, серо-желтого цвета, с участками кровоизлияний и лейкоцитарной инфильтрации. Стенки vasa vasorum, вокруг которых отмечается наиболее интенсивная инфильтрация, подвергаются некрозу, просвет их тромбируется. Это ведет к развитию дистрофических и некротических изменений стенки вены.
При благоприятном течении острого тромбофлебита происходит резорбция некротических масс, исчезают полиморфно-ядерные лейкоциты, вместо них появляются макрофаги, лимфоциты, плазматические клетки, фибробласты. Развивается рыхлая молодая грануляционная ткань. Затем следуют канализация или организация тромба, созревание грануляционной ткани и превращение ее в грубоволокнистую соединительную ткань.
Исходом тромбофлебита является склероз венозной стенки и тромба. Степень восстановления просвета вены зависит от величины тромба. После завершения организации тромб нередко облитерирует просвет вены. В соединительной ткани, замещающей тромб, обнаруживаются щели и каналы. От их объема в определенной мере зависит степень восстановления просвета.
Перифлебит, развивающийся при тромбофлебите, может быть причиной склероза соединительной ткани, окружающей сосудисто-нервный пучок, что приводит к развитию нейротрофических расстройств.
Лечение тромбофлебитов во всех стадиях — обязательно комплексное. Используют консервативные и хирургические методы. Выбор метода зависит от локализации, характера (эмбологенный, неэмбологенный) и протяженности тромбоза.
Консервативные методы являются основными при лечении острых тромбозов и тромбофлебитов. При сегментарном тромбозе магистральных вен проводят хирургическое лечение. При обнаружении эмбологенной формы тромбоза показано оперативное вмешательство, направленное на профилактику тромбоэмболии легочной артерии (тромбэктомия, перевязка вен, имплантация кавафильтра).
Главный компонент комплексного консервативного лечения — применение антитромботических средств. Активная стадия венозного тромбоза, продолжающаяся в среднем 2-3 нед, характеризуется тромботическим состоянием системы гемостаза: значительной гиперкоагуляцией, выраженным торможением фибринолиза и резким повышением агрегационной способности тромбоцитов. В связи с этим при лечении острого венозного тромбоза необходимо устранить тромботический сдвиг во всех трех основных звеньях гемостаза.
Успех лекарственной терапии тромбозов достигается при сочетанном использовании антикоагулянтных, тромболитических средств и препаратов, изменяющих микроциркуляцию и агрегацию форменных элементов крови.
Рекомендуемые средства профилактики и лечения тромбозов включают:
- антикоагулянты прямого и непрямого действия — дикумарин, фенилин, синкумар, гепарин, фраксипарин, клексан и др.;
- тромболитические средства — трипсин, химотрипсин, стрептокиназа, тромболитин (комплексный препарат трипсина и гепарина), фибринолизин;
- препараты, улучшающие микроциркуляцию и уменьшающие агрегацию форменных элементов крови, — трентал, никотиновая кислота.
Комплексное лечение острого поверхностного тромбофлебита включает: эластическую компрессию нижней конечности, ее возвышенное положение, местное применение холода, троксевазиновой или гепаринсодержащей мази, внутривенное введение троксевазина по 5 мл в течение пяти дней с переходом на пероральный прием этого же препарата (1 капсула 3 раза в день), назначение бутадиона в дозе 5 г 3 раза в день в течение 10 дней. На протяжении всего периода лечения необходим тщательный контроль за динамикой процесса в поверхностных венах.
Если, несмотря на консервативную терапию, тромбофлебит распространяется в проксимальном направлении, следует совместно с хирургом решить вопрос о необходимости оперативного лечения.
При остром тромбофлебите поверхностных и глубоких вен нижних конечностей хороший клинический эффект дает лечение, которое начато в течение первых трех дней от начала заболевания. Если же оно начато в более поздние сроки, отмечается длительное сохранение отека, реканализация затягивается надолго.
Сроки активизации больных тромбофлебитом зависят главным образом от тяжести заболевания. При тромбофлебите поверхностных вен лечебная физкультура показана со 2-3-го дня, при тромбофлебите глубоких вен — с 5-10-го дня, когда уменьшается местная воспалительная реакция, снижается температура тела и прекращаются боли. Занятия проводят 1-2 раза в день, их продолжительность — 7-10 мин. Начинают с упражнений на здоровой ноге, через 1-3 дня вводят упражнения для больной ноги.
Комплексная сочетанная терапия должна осуществляться под контролем коагулограммы, что позволяет дозировать препараты и избежать осложнений.
Методами хирургического лечения являются: перевязка вен, разрезы по ходу вен с раскрытием венозного ложа и иссечением пораженного участка — венэктомия, эмболэктомия, тромбэктомия, пересадка и пластические операции на венах. При гнойном восходящем тромбофлебите перевязка вены производится значительно выше тромба.
При необходимости флебэктомию выполняют спустя 5-10 дней от начала лечения, т.е. после ликвидации воспалительных явлений (перифлебита). Консервативное лечение с применением протеолитических ферментов в этих случаях служит предоперационной подготовкой к радикальному лечению.
Лечение послеродовых тромбофлебитов осуществляют в отделении акушерского стационара, специализирующегося на лечении воспалительных заболеваний у беременных, рожениц и родильниц, а также в гинекологических и хирургических отделениях.
У больных с тромбофлебитом поверхностных вен прогноз обычно благоприятный. Менее благоприятный прогноз у больных с невосстановленным венозным кровотоком. У них развивается хроническая венозная недостаточность с выраженным отечно-болевым синдромом, трофическими язвами, в связи с чем может наступить стойкая утрата трудоспособности.
Прогрессирующий тромбофлебит является формой третьего этапа послеродовой инфекции. При этом процесс не ограничивается воспалением венозной стенки и образованием тромба, а распространяется дальше по протяжению вены. В результате распада тромбов могут возникнуть эмболии и инфаркты легких. При своевременной и адекватной антибактериальной терапии метастатические очаги, как правило, не развиваются.
Клиническая картина эмболии легких определяется механической закупоркой ветвей легочной артерии, резким рефлекторным спазмом ее незатронутых разветвлений, спазмом бронхов и возникшей коронарной недостаточностью.
Эмболия крупных ветвей легочной артерии проявляется резкой слабостью, бледностью, снижением артериального давления, тахикардией, болями в грудной клетке. Острая эмболия главного ствола легочной артерии, как правило, приводит к смерти.
При эмболии небольших ветвей наблюдаются одышка, боли при дыхании (на выдохе), учащение пульса. Нередко в легких развиваются инфаркты, преимущественно в нижних долях. Наиболее постоянные признаки инфаркта — боли при дыхании, притупление перкуторного звука, ослабленное дыхание с бронхиальным оттенком, мелкопузырчатые хрипы по периферии инфарктного очага. Иногда появляется примесь крови в мокроте. Повышается температура, отмечается лейкоцитоз.
Лечение заключается в немедленном внутривенном введении морфина, спазмолитических средств, ингаляции кислорода, в инфузии в легочную артерию стрептокиназы, урокиназы с гепарином или во внутривенном введении стрептодеказы (иммобилизированный фермент — стрептокиназа). Все чаще делаются попытки применять хирургический метод лечения эмболии легочных артерий, но ввиду того, что это осложнение развивается очень быстро, чаще со смертельным исходом, операции в специализированных лечебных учреждениях производят редко.
Прогноз при эмболии крупных ветвей легочной артерии неблагоприятный, а при эмболии мелких и небольших ветвей в случаях правильного и своевременного лечения в большинстве случаев благоприятный.
К мерам общей неспецифической профилактики относятся: своевременная и полноценная коррекция нарушений гемогидробаланса, предупреждение дыхательных расстройств, борьба с метеоризмом, лечебная физкультура и ранняя активизация больных. Женщинам, имеющим факторы риска, в особенности тем, которые в прошлом перенесли острый венозный тромбоз или страдают варикозным расширением вен нижних конечностей, показано применение специальных профилактических мер. Для устранения расстройств венозного оттока рекомендуют постоянную компрессию нижних конечностей с помощью эластических бинтов или чулок, обеспечение возвышенного положения ног в постели. Эффективным средством улучшения периферической гемодинамики является прерывистая пневматическая компрессия или электростимуляция икроножных мышц, имитирующая действие мышечно-венозной «помпы» голени.
Важную роль в профилактике послеродовых тромбофлебитов у больных с повышенным риском развития тромбоза играет использование медикаментозных средств, влияющих на систему гемостаза и реологические свойства крови. Опасность возникновения послеродового тромбофлебита может быть значительно уменьшена подкожным введением препаратов гепарина (5-7 дней). Создаваемая при этом легкая гипокоагуляция не вызывает геморрагических осложнений. Широко применяют с целью профилактики никотиновую кислоту, аспирин.
Профилактика тромбофлебита состоит в правильном и своевременном лечении тех заболеваний, которые могут им осложняться. Следует не допускать обезвоживания организма в предоперационном и послеоперационном периодах, поощрять активные движения больных в послеоперационном периоде, бережно относиться к тканям во время операции, своевременно назначать антикоагулянты и средства, улучшающие функцию сердечно-сосудистой системы.
МАСТИТ
Мастит — воспаление паренхимы и интерстиция молочной железы. Это заболевание — одно из наиболее частых осложнений послеродового периода. Частота возникновения послеродовых маститов составляет 1,5-6% по отношению к числу родов. Две трети различных случаев гнойно-воспалительных процессов в послеродовом периоде приходится на долю мастита. Увеличение частоты возникновения маститов объясняется изменением видового состава возбудителей гнойной инфекции, их антигенных свойств и антибиотикорезистентностью.
Обычно мастит развивается с одной стороны. Двусторонний процесс встречается редко. Из всех случаев маститов 70% приходится на первородящих, 27% — на повторнородящих, 3% — на многорожавших. Возрастание заболеваемости маститом у женщин старше 30 лет обусловлено увеличением количества первых родов в этом возрасте.
Возбудителем мастита чаще всего является стафилококк. У 82% больных при посеве гноя стафилококк выделяется в чистом виде, у 11% — в ассоциациях с E.coli и стрептококком, у 3,4% выявляется E.coli в монокультуре, у 2,4% — стрептококк, редко встречаются протей, грибы. Источник инфекции — носители возбудителей и больные со стертыми формами гнойно-воспалительных заболеваний из числа окружающих лиц, от которых микробы распространяются через предметы ухода, белье и т.д. Важную роль в возникновении мастита играет госпитальная инфекция.
Чаще всего входные ворота для инфекции — трещины сосков. Возможно интраканаликулярное распространение возбудителей при кормлении грудью и сцеживании молока. Реже происходит распространение инфекции гематогенным и лимфогенным путем из эндогенных очагов. Способствовать возникновению и развитию заболевания могут наличие сопутствующей экстрагенитальной патологии, снижение иммунореактивности организма, осложненные роды, особенно первые, различная патология в послеродовом периоде.
Маститу во многих случаях предшествует нарушение оттока молока с развитием лактостаза, что наблюдается при недостаточности млечных протоков у первородящих, аномалиях развития сосков, нарушениях функции молочной железы. При наличии микробов молоко в расширенных молочных ходах сворачивается, стенки протоков отекают, что еще больше способствует застою молока. Все эти моменты являются факторами, способствующими попаданию микробов в ткань молочной железы и обусловливающими начало и развитие мастита
В зависимости от локализации воспалительного процесса выделяют следующие виды мастита: паренхиматозный, характеризующийся преимущественным поражением паренхимы молочной железы; интерстициальный, с преимущественным поражением интерстициальных отделов; галактофорит — воспаление молочных протоков; ареолит — воспаление желез околососкового кружка.
Различают острые и хронические маститы. Для практических целей наиболее приемлема клиническая классификация острых маститов с учетом течения воспалительного процесса: серозный (начинающийся), инфильтративный, гнойный и гангренозный. В свою очередь гнойный мастит может быть инфильтративно-гнойным (диффузный, узловой), абсцедирующим (фурункулез ареолы, абсцесс ареолы, абсцесс в толще железы, абсцесс позади железы — ретромаммарный) и флегмонозным (гнойно-некротический).
В группе хронических маститов различают гнойную и негнойную формы. Хронический гнойный мастит встречается довольно редко, чаще всего он — следствие неправильно леченного острого мастита. Характеризуется образованием мелких абсцессов с выраженной индурацией окружающих тканей. В редких случаях возможно развитие первично-хронического мастита. К негнойной форме хронического мастита относят плазмоклеточный перидуктальный мастит, при котором определяются инфильтраты, имеющие большое число блуждающих плазматических клеток вокруг млечных протоков.
Клиническая картина мастита в различных фазах имеет свои особенности. Для типичной клинической формы серозного мастита характерно острое начало обычно на 2-3-4-й неделе послеродового периода, т. е. после выписки родильницы из стационара. Температура тела быстро повышается до 38-39 °С, сопровождается познабливанием или ознобом. Развиваются общая слабость, разбитость, возникает головная боль, боль в молочной железе. Во время осмотра отмечается едва заметное увеличение молочной железы при полном сохранении ее контуров. Кожа не изменена. При сравнительной пальпации можно отметить несколько большую упругость и диффузную болезненность пораженной молочной железы. В этой фазе особенно опасен застой молока, который приводит к венозному стазу и способствует быстрому переходу серозного мастита во вторую фазу. Острый застой молока часто предшествует воспалительному процессу. Нагрубание молочных желез, протекающее с повышением температуры, следует считать серозной формой мастита.
При неадекватной терапии начинающийся мастит в течение 2-3 дней переходит в острую инфильтративную форму. Появляются ознобы, в железе образуется резко болезненный инфильтрат с неясными границами, вся железа значительно увеличивается, кожа над ней краснеет, СОЭ повышается до 30-40 мм/ч, лейкоцитоз нарастает до 10-20х109/л. Усиливаются чувство напряжения и боль в молочной железе, появляются головная боль, бессонница, слабость, потеря аппетита. Подмышечные лимфатические узлы увеличиваются и становятся болезненными. При пальпации инфильтрата обычно не удается заметить очаги размягчения, флюктуации.
Если общая и местная терапия не останавливает процесс и не способствует его обратному развитию, возникает абсцедирующая форма мастита. Все клинические признаки прогрессируют: СОЭ достигает 50-60 мм/ч, количество лейкоцитов — 15-16х109/л, гемоглобин снижается до 80-90 г/л, усиливается озноб, продолжается лихорадка. Наблюдается гиперемия кожи молочной железы, расширение подкожных вен, появляется лимфаденит. При нагноении инфильтрата определяется флюктуация.
Для флегмонозной формы характерны резкое ухудшение общего состояния, повышение температуры до 38-40 °С, ознобы. Усиливаются симптомы интоксикации. Появляются сухость губ и языка, бессонница, головная боль. Молочная железа увеличена, кожа ее гиперемирована, с участками цианоза. Наблюдаются резкое расширение подкожной венозной сети, лимфангит и лимфаденит. При пальпации железа пастозная, определяется несколько участков флюктуации. Лейкоцитоз достигает 17-18х109/л, содержание гемоглобина падает до 70 г/л, СОЭ нарастает до 60-70 мм/ч. Лейкоцитарная формула — со сдвигом влево, отмечаются эозинофилия, лимфопения.
Гангренозная форма мастита возникает при несвоевременном обращении за медицинской помощью либо при длительном амбулаторном лечении без адекватного контроля за общим состоянием больной и распространением процесса. При гангренозном мастите общее состояние очень тяжелое, температура достигает 40 °С, пульс 110-120 ударов в минуту, слабого наполнения. Кожа бледная, язык и губы сухие. Больная жалуется на слабость, головную боль, бессонницу, отсутствие аппетита. Молочная железа увеличена, болезненна, отечна. Кожа над ней от бледно-зеленого до синюшно-багрового цвета, в некоторых местах с пузырями и участками некроза. Сосок втянутый, молока нет, причем почти всегда и в здоровой железе. Регионарные лимфоузлы увеличены, при пальпации болезненны. Лейкоцитоз составляет 20-25х109/л, в формуле — резкий сдвиг влево, имеет место токсическая зернистость нейтрофилов. Гемоглобин снижается до 40-60 г/л, СОЭ повышается до 70 мм/ч.
В современных условиях для послеродового лактационного мастита характерны следующие особенности:
- более позднее начало, чаще после выписки из родильного стационара (иногда первые признаки заболевания появляются через 4 нед после родов);
- преобладание инфильтративно-гнойных маститов, протекающих в виде диффузных или узловых форм;
- затяжное и длительное течение гнойных форм заболевания;
- увеличение числа стертых субклинических форм мастита, при которых клинические проявления заболевания не соответствуют истинной тяжести процесса.
Диагностика основывается на оценке жалоб больной, особенностях клиники и лабораторных данных. Общий анализ крови характеризуется лейкоцитозом, нейтрофильным сдвигом, ускорением СОЭ, анемией. Бактериологическое исследование молока и гноя производится до антибактериальной терапии, а также в процессе и после окончания курса лечения. Идентифицируется возбудитель, определяется его чувствительность к антибиотикам. При цитологическом исследовании отмечается значительное увеличение числа лейкоцитов в единице объема молока (более 20 в поле зрения).
При УЗИ наблюдается гомогенная масса инфильтрата в определенном участке исследуемой молочной железы. При формировании гнойного мастита появляется очаг разрежения, вокруг которого тень инфильтрата усиливается. В последующем на этом месте визуализируется полость с неровными краями, перемычками.
Дифференциальная диагностика серозной формы мастита и лактостаза проводится на основании клинической картины заболевания. Для лактостаза характерно однократное повышение температуры до 38 °С при общем удовлетворительном состоянии; молочная железа равномерно нагрубает во всех отделах; после сцеживания температура быстро нормализуется; лактация не страдает. Патогномоничным признаком мастита является высевание микроорганизмов из молока. При массивном высевании микробов лактостаз необходимо рассматривать как субклиническую стадию мастита и проводить лечение, как при серозном мастите. В фазе серозного воспаления ткань железы пропитана серозной жидкостью, отмечается скопление лейкоцитов вокруг сосудов. При прогрессировании воспалительного процесса серозное пропитывание сменяется диффузной гнойной инфильтрацией паренхимы молочной железы с мелкими очагами гнойного расплавления, которые в последующем сливаются, образуя абсцессы. Наиболее частая локализация гнойников — интрамаммарная, субареолярная. Иногда при гнойном мастите в результате вовлечения в воспалительный процесс сосудов и тромбирования их наступает некроз отдельных участков железы, развивается гангренозная форма мастита. После опорожнения гнойника и удаления секвестров ткани начинается процесс пролиферации, образуется грануляционная ткань, а затем происходит рубцевание.
В основе хронического гнойного мастита лежит образование мелких абсцессов с выраженной индурацией окружающих тканей. При плазмоклеточном мастите выделяются инфильтраты с большим количеством блуждающих плазматических клеток вокруг млечных протоков.
Особенности гнойного процесса железистых органов — незначительная способность к отграничению и стремительное распространение с вовлечением в воспалительный очаг большого количества железистой ткани. У части больных развивается гнойная инфильтрация паренхимы железы (апостематозный мастит), что быстро приводит к некрозу пораженных участков железы и образованию больших секвестров. Иногда наблюдается гнилостное поражение молочной железы, сопровождающееся септической реакцией.
Лечение проводят с учетом формы мастита. Его следует начинать как можно раньше, с появлением первых признаков заболевания. При отсутствии гнойного воспаления рекомендуется комплексное консервативное лечение, при гнойных маститах — оперативное вмешательство. При появлении признаков застоя молока железе создают состояние покоя, придают возвышенное положение с помощью поддерживающего, но не сдавливающего ее бюстгальтера. Для улучшения опорожнения железы используют молокоотсос, назначают окситоцин 1 мл (5 ЕД). Предварительно за 20-30 мин перед инъекцией окситоцина рекомендуется ввести 1-2 мл 2% раствора но-шпы внутримышечно.
При развитии мастита грудное вскармливание временно прекращают.
Показания к подавлению лактации у больных маститом при его тяжелом течении и резистентности к проводимой терапии следующие:
- быстро прогрессирующий процесс — переход серозной стадии в инфильтративную в течение 1-3 дней на фоне активного комплексного лечения; гнойный мастит с тенденцией образования новых очагов после хирургического вмешательства;
- вялотекущий, резистентный к терапии гнойный мастит (после хирургического лечения);
- флегмонозный и гангренозный мастит;
- мастит на фоне заболеваний других органов и систем.
Для подавления лактации используют препарат, ингибирующий секрецию пролактина, парлодел (бромокриптин). При неустоявшейся лактации его применяют в течение 4-5 дней по 1 таблетке 2 раза в день; при развившейся лактации лечение проводят в течение 7-14 дней.
Основной компонент в комплексной терапии послеродового мастита — антибиотики. При гнойном мастите их назначение сочетается со своевременным хирургическим вмешательством. В таких случаях целесообразно использовать цефалоспорины, сочетание синтетических антибиотиков с метронидазолом.
Упорная резистентность гнойного мастита позволяет предполагать наличие анаэробной микрофлоры и применять метронидазол в сочетании с вышеперечисленными антибиотиками. Повысить эффективность лечения можно сочетанным использованием антибиотиков и поливалентного стафилококкового бактериофага. В комплексной терапии мастита важное место занимают средства, повышающие специфическую иммунологическую реактивность и неспецифическую защиту организма. Эффективен антистафилококковый гамма-глобулин по 5 мл (100 ME) через день внутримышечно, на курс — 3 инъекции. Применяют антистафилококковую плазму (по 100-200 мл внутривенно), адсорбированный стафилококковый анатоксин (по 1 мл с интервалом 3 дня, на курс 3 инъекций).
Инфузионную терапию проводят всем больным при наличии интоксикации. В комплексной терапии используют антигистаминные препараты — супрастин, димедрол, дипразин; анаболические стероидные гормоны — ретаболил, неробол. При резистентных к терапии формах, склонности к гипотонии и угрозе развития септического шока показаны глюкокортикоиды.
Физические методы лечения применяют дифференцированно. При серозном мастите используют микроволновую терапию дециметрового или сантиметрового диапазона, ультразвук, УФО; при инфильтративном мастите — те же физические методы, но с увеличением тепловой нагрузки. После хирургического лечения гнойного мастита назначают внутрисосудистую УФО- и лазеротерапию, электрическое поле УВЧ в слаботепловой дозе.
При гнойном мастите показано оперативное лечение. Операция должна выполняться в операционной в стационарных условиях. Необходимо производить широкое вскрытие гнойного очага с минимальным травмированием молочных протоков. Наиболее часто применяют радиальный разрез — от границы околососкового кружка к периферии, а затем тупым путем разрушают перемычки между пораженными дольками, эвакуируют гной, удаляют некротические ткани, в рану вводят тампон и дренаж. При флегмонозном и гангренозном мастите иссекают и удаляют некротизированные ткани. Прогноз при своевременном адекватном лечении благоприятный.
Профилактика заключается в строгом соблюдении санитарно-гигиенических и санитарно-противоэпидемических мероприятий в акушерском стационаре, в систематической борьбе со стафилококковой инфекцией, в осуществлении целенаправленных мер для предупреждения мастита.
В послеродовом периоде необходимо следующее:
- ежедневный гигиенический душ и смена белья;
- занятия гимнастикой;
- раннее вставание;
- мытье рук и туалет молочных желез перед кормлением;
- прием воздушных ванн в течение 10-15 мин после каждого кормления;
- ношение бюстгальтера, приподнимающего, но не сдавливающего молочные железы;
- проведение профилактических мероприятий против мастита у родильниц группы высокого риска;
- обучение родильниц правилам и технике грудного вскармливания;
- профилактика, своевременное распознавание и рациональное лечение трещин сосков и лактостаза.
Для лечения трещин сосков используют 14% спиртовой раствор бриллиантового зеленого, 1-5% линимент синтомицина, 0,2% фурацилиновую мазь, мазь каланхоэ, 2% раствор хлорофиллипта в масле, цигерол, настойку календулы. Эффективно применение токов Д’Арсонваля, УФО. В процессе лечения на 2-4 дня отлучают ребенка от груди (искусственное вскармливание).
