ОКСОСОЕДИНЕНИЯ: АЛЬДЕГИДЫ И КЕТОНЫ

Физические свойства альдегидов и кетонов
Альдегиды и кетоны – жидкости с характерным запахом.
Молекулы альдегидов и кетонов не образуют ассоциатов, поэтому по сравнению со спиртами они имеют более низкие температуры плавления и кипения.
Способы получения альдегидов и кетонов
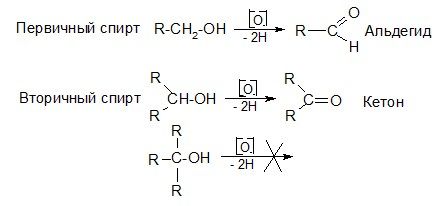
1. Окисление спиртов
При мягком окислении (дегидрировании) первичных и вторичных спиртов образуются соответственно альдегиды и кетоны (см. » Химические свойства спиртов»).
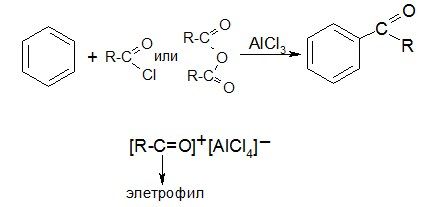
2. Ацилирование ароматических углеводородов
При ацилировании ароматических углеводородов (реакция Фриделя-Крафтса) образуются ароматические кетоны (см. » Химические свойства аренов»).
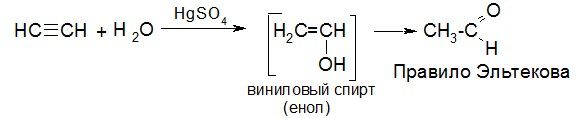
3. Гидратация алкинов
При присоединении воды к тройной связи образуются альдегиды и кетоны (см. » Химические свойства алкинов»).
4. Оксосинтез – промышленный способ
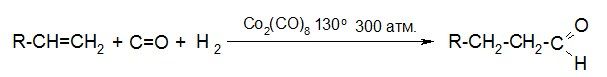
5. Окисление метильных производных бензола
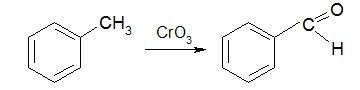
6.Гидролиз геминальных дигалогенопроизводных
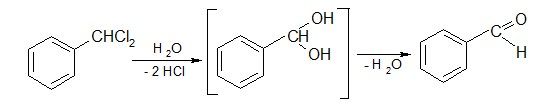
7. Восстановление хлорангидридов кислот
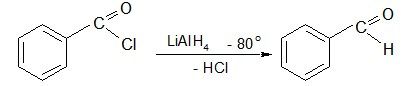
Химические свойства альдегидов и кетонов
Химия альдегидов и кетонов очень разнообразна. Из них можно получить соединения многих других классов.
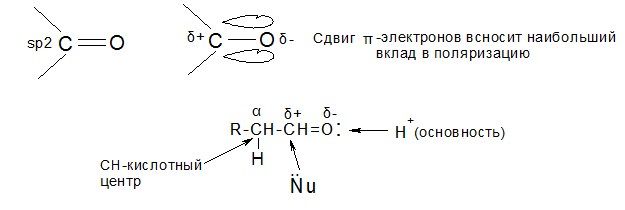
1. Реакции нуклеофильного присоединения к карбонильной группе (AN)
Механизм реакции (Большинство таких реакций обратимы)
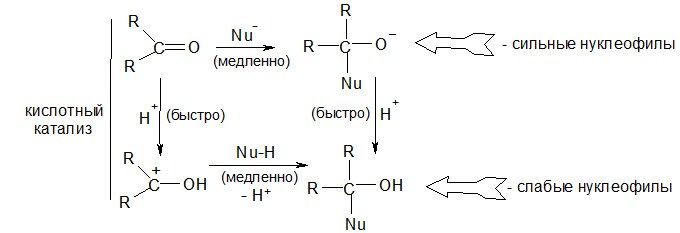
Фактор, определяющий скорость реакции АN – (+)-заряд на карбонильном атоме углерода.
Влияние заместителей на скорость реакци
Электроноакцепторы увеличивают скорость реакции, электронодоноры её уменьшают
Альдегиды более реакционноспособны, чем кетоны: заместитель R — электронодонор).
Ароматические альдегиды менее реакционноспособны, чем алифатические: +М-эффект арильного заместителя больше, чем +I-эффект алкила.
Влияние пространственных факторов на скорость реакции AN:
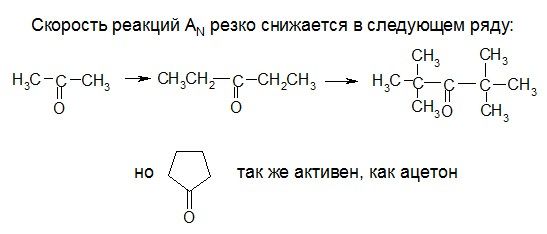
Разновидности реакций AN
а) гидратация
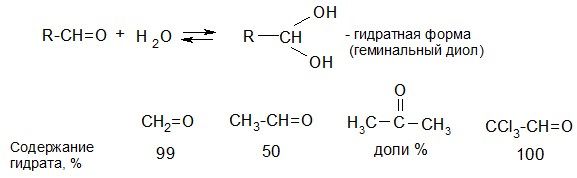
б) реакция со спиртами (образование полуацеталей и ацеталей)
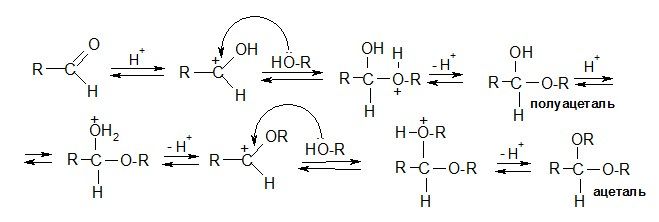
Реакция обратима.
Обратная реакция – это кислотный гидролиз ацеталей.
В щелочной среде ацетали не гидролизуются.
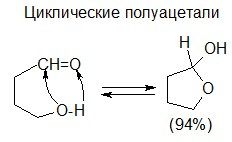
в) реакции с тиолами
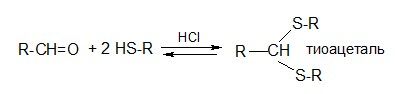
Тиоацетали трудно гидролизуются кислотами, в щелочи они устойчивы.
г) реакции с N-содержащими нуклеофилами
Механизм «присоединение – отщепление»:
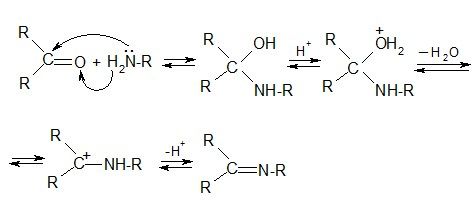
Амины:
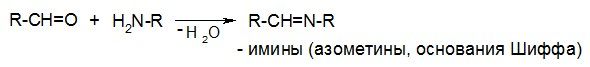
Гидразины:
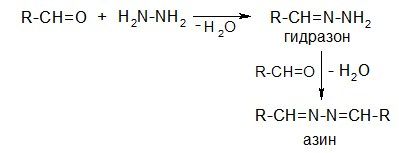
С фенилгидразином и его производными альдегиды и кетоны образуют устойчивые, хорошо кристаллизующиеся вещества, удобные для идентификации исходного соединения. Например:
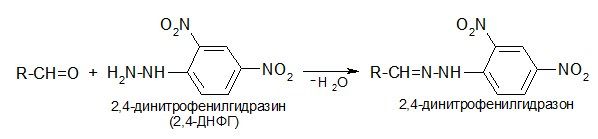
Гидроксиламин:
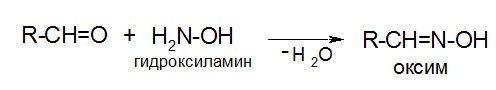
Семикарбазид:
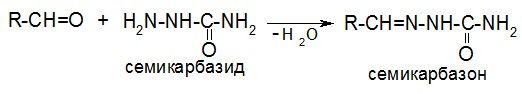
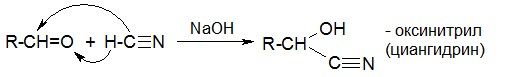
д) реакции с синильной кислотой
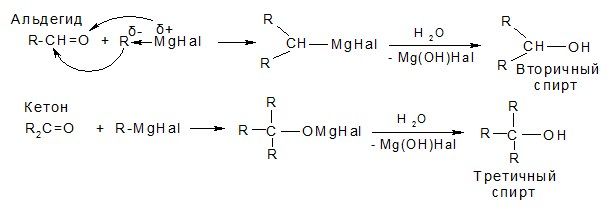
е) реакции с магнийорганическими соединениями (реактивами Гриньяра)
2. Реакции с участием СН-кислотного центра
Галоформные реакции
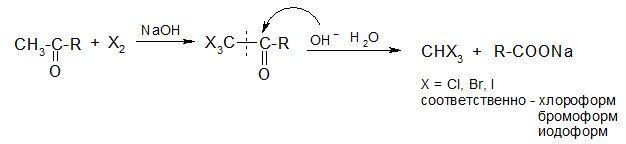
Эти реакции используются для получения галоформов, а также для качественного определения ацетона и других соединений, содержащих в своей структуре фрагменты СН3-С=О или СН3-СНОН.
Альдольная конденсация
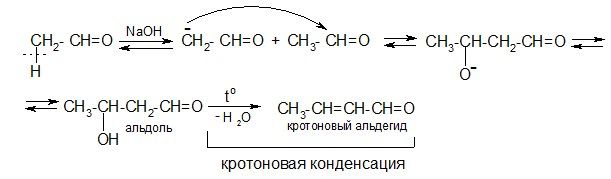
3. Восстановление (гидрирование)

4. Окисление
Альдегиды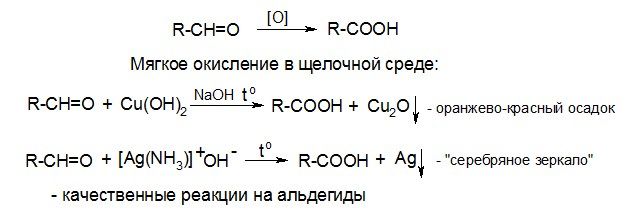
Кетоны
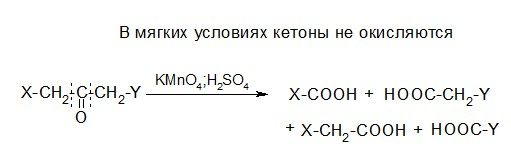
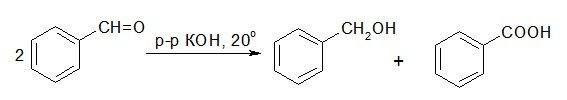
5. Реакции диспропорционирования
Реакция Канницарро — реакция идет с альдегидами, не имеющими Н в α-положении
Реакция Тищенко
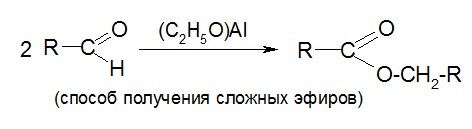
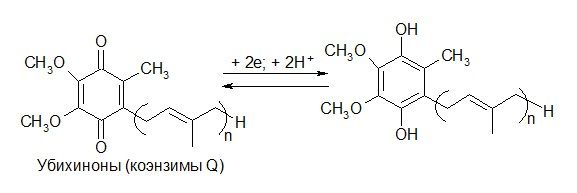
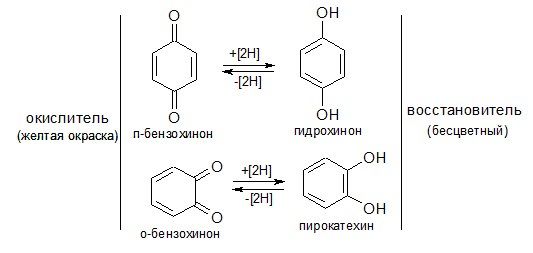
ХИНОНЫ — ненасыщенные циклические кетоны
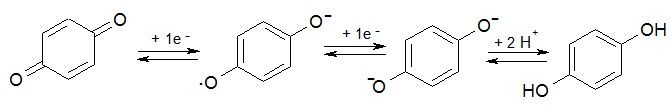
Механизм восстановления – одноэлектронный перенос:
Превращения типа «хинон-гидрохинон» участвуют в процессах биологического окисления: