МОЛЕКУЛЯРНЫЕ МЕХАНИЗМЫ СТАРЕНИЯ
2.1. Роль соматических мутаций в старении
2.2. Метилирование ДНК и старение
2.3. Гликозилирование белков и ДНК
2.4. Репарация ДНК и старение
2.5. Изменения структуры и функции генов при старении
2.6. «Предел Хейфлика», теория маргинотомии, теломеры и теломераза
2.7. Апоптоз и продолжительность жизни
2.8. Свободнорадикальная теория старения
2.1. Роль соматических мутаций в старении
Среди современных теорий старения, основанных на предположении, что ДНК является основной мишенью в клетке, доминирует теория соматических мутаций, согласно которой старение является результатом взаимодействия различных эндогенных и экзогенных повреждающих агентов с генетическим материалом клетки и постепенного накопления случайных мутаций в геноме соматических клеток. Повреждения ядерной и митохондриальной ДНК соматических клеток, такие как точковые мутации, делеции и перестройки приводят к активации или инактивации специфических генов, вовлеченных в такие ключевые клеточные процессы, как регуляция клеточного цикла и контроль роста. Накопление с возрастом таких мутаций в различных органах и тканях является основным фактором, определяющим развитие возрастной патологии, включая рак.
Пpедставляется весьма существенным вывод о неоднозначности возpастной динамики накопления соматических мутаций в pазличных оpганах и тканях. Трансгенные мыши, несущие шаттл-вектор LacZ, являются уникальной моделью для изучения частоты и спектра соматических мутаций при старении. Было установлено, что увеличение частоты мутаций в печени происходит равномерно с рождения до глубокой старости, тогда как в головном мозгу она нарастает только от рождения до 4-6 месяцев жизни, а затем не изменяется. Перестройки генома постепенно накaпливаются в печени до 27-месячного возраста, после чего их число резко увеличивается. В головном мозге геномные перестройки встречаются значительно реже и с возрастом их частота не увеличивается.
Некоторые биологические свойства синтетического аналога тимидина 5-бромо-2′-дезоксиуридина (БДУ) позволяют предполагать, что этот агент может служить адекватным средством для изучения роли избирательного повреждения ДНК в процессах старения. Индукция БДУ точечных мутаций в генетическом аппарате может приводить либо к ускоренному старению клеток и, следовательно, всего организма в целом, либо к скачкообразному увеличению биологического возраста (по типа сдвига). А.И.Потапенко и соавт. установили, что присутствие БДУ в питательной среде для D.melanogaster может укорачивать продолжительность их жизни. При этом БДУ усиливал сокращающее продолжительность жизни насекомых действие облучения в дозах 150 — 500 Гр. На основании анализа кривых выживаемости популяций дрозофил авторы сделали вывод о развитии у них при облучении синдрома преждевремннного старения и его усилении постоянным введением БДУ в питательную среду.
В наших исследованиях также было изучено влияние неонатального введения БДУ на продолжительность жизни крыс. В опыте, в котором в общей сложности было использовано более 400 крыс, было установлено, что БДУ достоверно уменьшает среднюю продолжительность жизни самцов и самок крыс, причем этот эффект был пропорционален его дозе. При этом, наблюдалось существенное изменение параметров старения популяции, расчитанных по уровнению Гомпертца: R = Ro (exp t), где R= смертность, Ro= смертность во время (t) = 0, = константа, и свидетельствовавших об ускорении старения в подопытных группах. Изучение у подопытных и контрольных самок крыс их эстральной функции показало, что введение БДУ сопровождается не скачкообразным, а постепенным и более ранним наступлением ее обычных возрастных нарушений (персистирующего эструса и анэструса). В специально проведенных экспериментах было убедительно показано, что эти нарушения определяются развивающимися под влиянием БДУ постепенными и более ранними, чем в контроле, возрастными изменениями центральных звеньев регуляции репродуктивной функции.
2.2. Метилирование ДНК и старение
Молекулярные события, определяющие транскрипцию, имеют решающий интерес для геронтологов, поскольку регуляция экспрессии генов коренным образом влияет на старение и старческие изменения. Хорошими примерами служат гиперэкспрессия амилоидного белка или экспрессия онкогенов. Генетические -облучении мышей разного возраста репаративный синтез увеличивается в 2-3 раза по сравнению с контролем. Авторы установили, что дело не в снижении активности ферментов репарации ДНК, поврежденной радиацией, а в степени доступности для ферментов этих повреждений ДНК в составе хроматина клеток. Об этом же свидетельствует и возрастное снижение релаксируемости нуклеоида ядер печени мышей при сравнении молодых и старых -облученных животных.
Было показано, что радиационная повреждаемость ДНК стволовых клеток кишечного эпителия мышей разных линий и возраста примерно одинакова, однако, скорость репарации этих повреждений с возрастом снижается. Cпособность диплоидных фибробластов человека к репарации индуцированных -излучением однонитевых разрывов ДНК достоверно снижается с увеличением возраста донора. В ряде работ оценивалось влияние возраста донора на интенсивность внепланового синтеза ДНК в клетках человека, подвергнутых in vitro УФ-облучению. B.Lambert и соавт. нашли отрицательную корреляцию между возрастом и величиной ВСД в лейкоцитах периферической крови 58 здоровых субъектов 13-94 лет. Авторы отметили сильные индивидуальные колебания величины ВСД. Было обнаружено также ослабление индуцированного УФ-светом репаративного синтеза в лимфоцитах человека с возрастом и в глубокой старости.
2.5. Изменения структуры и функции генов при старении
При старении может изменяться не только структура генов, но и направление их функционирования. С возрастом в соматических клетках накапливаются не только мутации, но и хромосомные перестройки. Полагают, что изменения хроматина могут играть главную роль в связанных с возрастом изменениях регуляции экспрессии генов. C увеличением возраста не отмечено изменений стехиометрии большинства гистонов однако имеются сообщения об изменениях подвида гистона Н1. Ацетилирование гистонов, которое предположительно изменяет взаимодействие гистон-ДНК и делает ДНК более доступной, снижается по мере старения на 30-70%.
В последние годы десятилетиe было опубликовано несколько обзорных работ,в которых обсуждается влияние возраста на транскрипцию. Установлено, что в целом транскрипционная активность клетки при старении организма снижается. Однако уровень общей РНК остается постоянным за счет снижения скорости обновления РНК. В большинстве исследований была найдена хорошая корреляция между связанными с возрастом изменениями уровней видов мРНК и уровнем белка (или энзиматической активностью), обусловленным различными видами мРНК. Это было показано на печени крыс в отношении альбумина, альфа(2)-глобулина и супероксиддисмутазы и каталазы. Связанное с возрастом уменьшение индукции митогенами мРНК интерлейкина 2 (ИЛ-2) в лимфоцитах грызунов и человека соответствует возрастному снижению биологической активности этих двух интерлейкинов.
2.6. «Предел Хейфлика», теория маргинотомии, теломеры и теломераза
Около 100 лет тому назад в связи с развитием методов поддержания клеток in vitro со всей остротой встал вопрос о том, ограничен ли потенциал клеток многоклеточного организма. A.Каррель культивировал фибробласты сердца куриных эмбрионов в культуре в течение 34 лет, при этом клетки прошли тысячи делений без изменений их морфологического строения или скорости роста. Эти опыты встретили серьезные возражения. В частности, указывалось, что несовершенство методов культивирования приводило к внесению свежих клеток в культуры при каждом их пересеве. С другой стороны, онкологам хорошо известны многочисленные штаммы перевиваемых in vivo и in vitro опухолевых штаммов и линий, которые поддерживаются в течение многих лет, иногда десятков лет, клетки которых являются практически бессмертными (иммортализированными). Наряду с этими опытами, появились наблюдения о том, что в клеточных культурах все же не удается длительно поддерживать клетки, полученные из нормальных, не опухолевых тканей.
В 1961 г. L.Hayflick и P.S.Moorhead представили данные о том, что даже в идеальных условиях культивирования фибробласты эмбриона человека способны делиться только ограниченное число раз (50 +/-10). Было установлено, что при самом тщательном соблюдении всех мер предосторожности при пересевах клетки проходят in vitro ряд вполне морфологически различимых стадий (фаз), после чего их способность к пролиферации исчерпывается и в таком состоянии способны находиться довольно длительное время. В повторных опытах это наблюдение было многократно воспроизведено, последняя фаза жизни клеток в культуре была уподоблена клеточному старению, а сам феномен получил по имени автора название лимита Хейфлика. Более того, оказалось, что с увеличением возраста донора число делений, которые были способны совершить клетки организма, существенно уменьшалось, что привело к представлению о существовании гипотетического счетчика делений, ограничивающего общее их число.
В 1971 г. А.М.Оловников на основании появившихся к тому времени данных о принципах синтеза ДНК в клетках предложил гипотезу маргинотомии, объясняющую механизм работы такого счетчика. Этот механизм заключался, по мнению автора гипотезы, в том, что при матричном синтезе полинуклеотидов ДНК-полимераза не в состоянии полностью воспроизвести линейную матрицу, реплика получается всегда короче в ее начальной части. Таким образом, при каждом делении клетки ее ДНК укорачивается, что, подобно шагреневой коже, ограничивает пролиферативный потенциал клеток и, очевидно, является тем «счетчиком» числа делений и, соответственно, продолжительности жизни клетки в культуре (рис.1). В 1972 г. Ж.Медведев показал, что повторяющиеся копии функциональных генов могут управлять или запускать процесс старения.

Открытие в 1985 году теломеразы — фермента, который достраивал укороченную теломеразу в половых клетках и клетках опухолей, обеспечивая их бессмертие [213], вдохнуло новую жизнь в гипотезу Оловникова. Было выполнено огромное количество работ, в которых были установлены следующие основные факты:
1. Концы линейных хромосом с 3′-конца ДНК заканчиваются повторяющимися последовательностями нуклеотидов, получившими название теломер, которые синтезируются специальным рибонуклеиновым ферментом теломеразой.
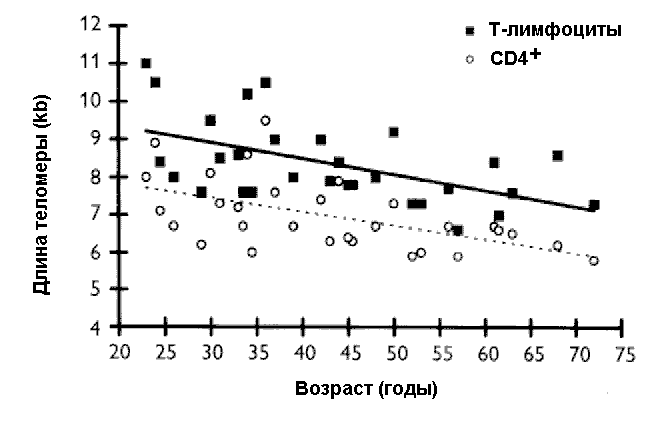
2. Соматические клетки эукариотов, имеющие линейные хромосомы, лишены теломеразной активности. Их теломеры укорачиваются как в процессе онтогенеза и старения in vivo (рис. 2), так и при культивировании in vitro.
3. Половые клетки и клетки иммортализированных линий, а также опухолей имеют высокоактивную теломеразу, которая достраивает 3′-конец ДНК, на котором реплицируется комплементарная цепь при делении.
4. Структуры теломер сильно различаются среди простейших, однако у всех позвоночных они одинаковы (TTAGGG)n.
5. Имеются существенные межвидовые различия в длине теломер, причем у мыши общая их длина в несколько раз превышает таковую у человека (до 150 тысяч пар нуклеотидов у некоторых линий мышей и 7-15 т.п.н. у человека).
6. Репрессия теломеразы определяет клеточное старение в культуре (лимит Хейфлика).
7. Клетки больных синдромом преждевременного старения Хатчинсона-Гилфорда и синдромом Дауна имеют укороченные теломеры.
Недавно было установлено, что при введении гена теломеразы в клетки фибробластов человека, которые в норме делятся лишь 75-80 раз, они способны поделиться 280 раз и без каких либо признаков старения и патологии. Тщательное исследование показало отсутствие в этих клетках таких признаков малигнизации, как нестабильность хромосом, независимый от добавления натуральной сыворотки рост, отсутствие контактного торможения и потеря контроля клеточного цикла. В другой работе также было показано, что иммортализованные теломеразой фибробласты, прошедшие по крайней мере в два раза больше удвоений, чем нормальные, не проявляют признаков злокачественного роста in vitro, но, что особенно важно, из них не развиваются опухоли при трансплантации бестимусным мышам. Полученные данные свидетельствуют о том, что экспрессия теломеразы в культуре клеток человека совсем не обязательно вызывает развитие рака, то есть лишена свойств онкогена, которые ей приписывали. Видимо, основным свойством теломеразы является контроль клеточного деления, а для возникновения опухолевого роста необходимы дополнительные мутации и факторы.
Доказательства правомочности такого предположения недавно были представлены T.Kiyono и соавт., которые показали, что введения каталитического компонента теломеразы hTERT или теломеразной активности с помощью онкобелка вируса папилломы человека Е7 в кератиноциты или клетки эпителия человека недостаточно для их полной иммортализации. Она наступает лишь при дополнительном торможении регуляции антионкогена Rb/p16 или при угнетении экспрессии p16 в качестве второй важнейшей ступени этого процесса. Элиминация антионкогена р53 таким свойством не обладала. C другой стороны, протоонкоген c-Myc может активировать экспрессию теломеразы, а введение онкогена v-Ha-RAS дрожжам увеличивает продолжительность их жизни.
Важные данные получены в Институте молекулярной биологии им.В.А.Энгельгардта РАН. С помощью опосредованного микроклетками переноса маркированную геном neo хромосому 20 из стареющих и молодых диплоидных фибробластов человека ввели в молодые фибробласты. Во всех новообразованных клонах наблюдалось уменьшение пролиферативного потенциала на 17-18 удвоений популяции. Авторы склонны рассматривать полученные данные как свидетельство того, что отдельные теломеры способны ограничить пролиферативный потенциал клеток.
Показано, что старение некоторых тканей, например, эпителиальных клеток слизистой полости рта или роговицы глаза человека in vivo, не сопровождается укорочением теломер. Экспрессия белка аденовируса 12 Е1В 54К в нормальных клетках человека сопровождалась существенным увеличением их пролиферативного потенциала (до 100 удвоений). Когда затем деления все же прекратились и клетки перешли в фазу старения, то какого-либо существенного укорочения их теломер выявлено не было. Экспрессию активности теломеразы наблюдали в печени крыс после частичной гепатэктомии, то есть в процессе регенерации. Не удалось наблюдать существенных изменений в продолжительности жизни или развитии мышей с «выключенным» (knockout) геном теломеразы. Однако недавно было показано, что выключение гена теломеразы все же приводит к сокращению продолжительности жизни мышей, уменьшению устойчивости к стрессу и увеличению частоты развития новообразований. Авторы отметили, что в остальном физиологические и биохимические параметры животных не свидетельствовали об ускорении у них старения.
Многое в этой области еще предстоит выяснить. Тем не менее, очевидно, что опыты с теломеразой открывают новые перспективы как в геронтологии, так и в онкологии для диагностики рака и, что особенно важно, для его лечения.
2.7. Апоптоз и продолжительность жизни
Установление роли соматических мутаций и репарации ДНК в механизмах старения ставит вопрос о их непосредственной связи с процессами дифференцировки и программированной клеточной гибели (апоптоз) и злокачественного роста. Если у одноклеточных организмов лишь репарация повреждений ДНК позволяет им выжить при изменении условий окружающей среды, то у Metazoa оптимальная стратегия в отношении клеток, несущих повреждения ДНК, не столь однозначна, поскольку некоторые мутации в генах, регулирующих клеточную пролиферацию, адгезию и апоптоз, могут приводить к развитию злокачественных новообразований, ведущих к гибели организма. Поэтому, для организма в целом, «безопаснее» иметь механизмы элиминации таких генетически поврежденных клеток, чем риск возникновения очагов неконтролируемого автономного роста. Выбор конкретной «стратегии» организма — репарации ДНК, блокады пролиферации или апоптоза, зависит, во-многом, от типа клеток, их локализации, микроокружения, характера повреждающего фактора и степени повреждения. В любом случае, эффективный ответ на повреждение ДНК является ключевым звеном для выживания многоклеточного организма.
В последние годы достигнут значительный прогресс как в изучении самого феномена программированной клеточной гибели (апоптоза), так и в понимании молекулярных механизмов его реализации и регуляции. Установлена ключевая роль антионкогена р53 в этом процессе. Опосредованная р53 остановка пролиферации в стадии G1 или G2 клеточного цикла необратима. Такая клетка хотя и не погибает, но генетически она уже «мертва», поскольку не способна к развитию опухоли. Реализации такого эффекта р53 предшествует индукция циклин-зависимого ингибитора киназы р21. Менее ясна роль р53 в стимуляции собственно апоптоза. Установлено, что мишенями для р53 является несколько специфических генов, таких как антагонист гена Bax ген Bcl2, рецептор инсулиноподобного фактора роста-I (IGF-I), связывающий белок IGF-BP3, компоненты ренин-ангиотензин конвертирующей системы и белки, регулирующие ангиогенез. Более того, в некоторых случаях показано участие в этом процессе трансэкспрессии генов анти-апоптоза и даже некоторых нетранскрипционных механизмов. Выявлено также, что р53 участвует в реакции клетки на воздействия, которые не повреждают непосредственно ДНК, например при метоболической депривации, физических травмах, тепловом шоке, гипоксии и экспрессии таких онкогенов как Myc и E1A.
Выше уже обсуждалась модель клеточного старения Хейфлика и роль теломер и теломеразы в продолжительности жизни клеток in vitro. Использование этой модели оказалось весьма плодотворным для изучения механизмов репликативного старения. Прекращение способности пролиферировать клеток в культуре можно было объяснить потерей экспрессии пострепликативных генов, например, репрессией с-myc, или неспособностью фосфорилироваться белка ретинобластомы (RB), или, напротив, увеличением экспрессии антирепликативных генов, например, ингибитора циклин-зависимой киназы (cdk) р21. Недавно было установлено, что находящиеся в фазе репликативного старения фибробласты человека резистентны к апоптозу. Угнетение экспрессии ключевых генов G1 фазы, удерживающих стареющие фибробласты человека от вступления в фазу S клеточного цикла, по-видимому, является тем механизмом, который запускает процесс клеточной гибели. Уровень антиапоптотического фактора bcl2 постоянно высок в таких клетках, при этом не наблюдается протеолиза терминина от формы 90 kDa до 30kDa. Таким образом, репрессия генов G1 фазы, увеличение экспрессии гена анти-апоптоза bcl2 и отсутствие протеолиза преставляется, по образном выражению E.Wang, крепким «тройным замком», который предотвращает апоптотическую гибель стареющих фибробластов. Весьма существенна в патогенезе апоптоза роль свободных радикалов и ферментов, участвующих в их метаболизме, в частности, цитохрома с.
Закономерен вопрос — имеют ли отношение эти результаты, полученные в опытах in vitro, к реальной ситуации старения in vivo, прежде всего, к старению кожи человека? Недавно было установлено, что в коже пожилых лиц стареющие фибробласты содержатся в большом количестве. Хорошо известна высокая чувствительность кожи пожилых канцерогенному действию ультрафиолета и сниженная способность к заживлению ран. Cледует заметить, что еще в 1985 г. P.Ebbesen выявил существенное повышение чувствительности старых мышей к действию промотора кожного канцерогенеза 12-О-тетрадеканоилфорбол-13-ацетата по сравнению с кожей молодых животных. При подкожном введении старым животным самых разнообразных канцерогенных агентов (полициклических ароматических углеводородов, нитрозосоединений, пластмассовых пленок или вируса Молони) саркомы на месте введения развивались с большей частотой и значительно раньше, чем у молодых. C другой стороны, стимуляция апоптоза в клетках печени ограничением калорийности питания угнетала развитие пренеопластических узелков в печени у старых крыс и мышей. Введение мелатонина стимулировало апоптоз в клетках аденокарцином толстой кишки, индуцируемых 1,2-диметилгидразином, что сопровождалось отчетливым торможением развития опухолей, тогда как в постмитотических клетках головного мозга этот геропротектор угнетал индуцированную оксидативным стрессом клеточную гибель.
Таким образом, накопление в тканях с возрастом резистентных к апоптозу стареющих клеток, возможно, является тем айсбергом, который аккумулирует множественные повреждения, приводящие, в конечном счете, к неоплазии, нейродегенеративным процессам или смерти вследствие инфаркта миокарда.
2.8. Свободнорадикальная теория старения
Одной из наиболее плодотвоpно pазвивающихся в последние годы фундаментальных теоpий является свободноpадикальная теоpия стаpения, практически одновременно выдвинутая D.Harman в 1956 г. и Н.М.Эмануэлем в 1958 г. Эта теория объясняет не только механизм старения, но и широкий круг связанных с ним патологических процессов (сердечно-сосудистые заболевания, возрастные иммунодепрессия и дисфункция мозга, катаракта, рак и некоторые другие). Согласно этой теоpии, пpодуциpуемые главным образом в митохондриях клеток молекулы супеpоксида (О2-.), Н2О2, гидpоксильного pадикала (НО. ) и, возможно, синглетного кислоpода (О2) повpеждают клеточные макpомолекулы (ДНК, белки, липиды). Полагают, что активные формы кислорода вызывают повpеждения мембpан, коллагена, ДНК, хpоматина, стpуктуpных белков, а также участвуют в эпигенетической pегуляции экспрессии ядерных и митохондриальных генов, приводя к метилированию ДНК, влияют на внутpиклеточный уpовень кальция и т.д. Подсчитано, что за 70 лет жизни человека организм производит около одной тонны радикалов кислорода, хотя только 2-5% вдыхаемого с воздухом кислорода превращается в его токсические радикалы. В клетке крысы может возникать до 104 вызыванных активными формами кислорода повреждений ДНК в день и при постоянных условиях до 10% молекул белка могут иметь карбонильные модификации. Подавляющее большинство из них нейтрализуется еще до того, как успеют повредить те или иные компоненты клетки. Так, из каждого миллиона образующихся супероксидных радикалов от ферментной защиты ускользает не более четырех. К основным эндогенным факторам антиоксидантной защиты организма относятся некоторые ферменты и витамины (таблица 3).
Показано, что видовая продолжительность жизни прямо коррелирует с активностью супероксиддисмутазы (СОД), содержанием -каротина, -токоферола и мочевой кислоты в сыворотке крови. Более того, у долгоживущих линий D. melanogaster экспрессия СОД, каталазы, глютатионредуктазы и ксантиндегидрогеназы была достоверно большей, чем у короткоживующих линий мух).
Таблица 3. Факторы, защищающие макромолекулы клеток от повреждения свободными радикалами
| Мишень | Агент | Функция |
| О2 | Супероксиддисмутаза | Превращает О2 в Н2О2 |
| Н2О2 | Глютатион-пероксидаза | Превращает Н2О2 в Н2О и О2 |
| Каталаза | Превращает Н2О2 в Н2О и О2 | |
| Свободные радикалы | -каротин (провитамин А)
|
Связывает жирорастворимые свободные радикалы |
| Витамин Е (-токоферол)
|
« | |
| Витамин С (аскорбиновая кислота) | Связывает водорастворимые свободные радикалы | |
| Мочевая кислота | « | |
| Мелатонин | Связывает жиро- и водорастворимые свободные радикалы | |
| Переходные металлы | Хелатные агенты | Предотвращают катализ свободнорадикальных реакций переходными металлами, железом и медью |
В пользу свободнорадикальной теории старения говорят эксперименты в которых трансгенные линии D. melanogaster с дополнительными копиями генов, обеспечивающих избыточную активностьСОД и каталазы, жили на 20-37% дольше контрольных мух, тогда как мухи с избыточными копиями генов лишь одного из этих ферментов антиокислительной защиты таким эффектом не обладали. Недавно было установлено, что трансгенные дрозофилы с избыточной экспрессией гена SOD1 в мотонейронах жили на 40% дольше и были значительно устойчивее к окислительному стрессу, чем мухи, не имевшие этого гена. Витамин Е, мелатонин, хелатные агенты и некоторые синтетические антиоксиданты увеличивали продолжительность жизни не только дрозофил, но и лабораторных мышей и крыс. Однако, то обстоятельство, что продукты взаимодействия АФК с макромолекулами постоянно обнаруживаются в органах и тканях организма, свидетельствует о том, что системы антиоксидантной защиты недостаточно эффективны и что клетки постоянно подвергаются окислительному стрессу. Противодействие ему может играть существенную роль в механизме геропротекторного действия эндогенных и экзогенных антиоксидантов.


