МЕНСТРУАЛЬНЫЙ ЦИКЛ. ОПЛОДОТВОРЕНИЕ И РАЗВИТИЕ ПЛОДА.
Клинические лекции по акушерству (учебное пособие)
- ОВАРИАЛЬНЫЙ ЦИКЛ
- СТРОЕНИЕ ФОЛЛИКУЛА
- МАТОЧНЫЙ ЦИКЛ
- ОПЛОДОТВОРЕНИЕ
- ВНУТРИУТРОБНЫЙ РОСТ ПЛОДА
Менструальный цикл — циклические изменения в организме женщины, внешним проявлением которых является менструация.
Циклические изменения в яичниках — овариальный цикл — делятся на фолликулярную и лютеиновую фазы, а изменения в эндометрии — маточный цикл — на пролиферативную и секреторную фазы. В результате отторжения функционального слоя эндометрия возникает менструация. Менархе — первая менструация. Обычно она наблюдается в 10-12 лет, при этом регулярный цикл обычно устанавливается через 1-1,5 года. В среднем цикл составляет 28 дней, в норме — от 21 до 35 дней. Первый день менструации соответствует первому дню менструального цикла. Продолжительность менструации — 2-7 дней (в среднем 4-5 дней), кровопотеря — от 50 до 150 мл (в среднем 70-100 мл).
Менструальный цикл детерминируется сопряженной работой пяти звеньев нейрогуморальной цепи (кора мозга, гипоталамус, гипофиз, яичники, матка).
Основные продукты секреции гипоталамуса — гипофизарные рилизинг-факторы. Гонадотропин рилизинг-гормон (ГнРГ) контролирует секрецию гипофизарных гонадотропинов, лютеинизирующих гормонов (ЛГ) и фолликулостимулирующих гормонов (ФСГ) (рис. 4).
ГнРГ — единственный гормон, регулирующий секрецию двух гипофизарных гормонов в пульсирующем режиме. Постоянная инфузия ГнРГ не стимулирует секрецию гонадотропинов. Пульсирующий режим секреции ГнРГ (рис. 5) необходим из-за очень короткого периода пулураспада РГ — около 2-4 мин. В течение менструального цикла частота и амплитуда пульсации ГнРГ меняются: в фолликулярную фазу они высокие, а в лютеиновую происходит их уменьшение.

Рис. 4. Регуляция менструального цикла
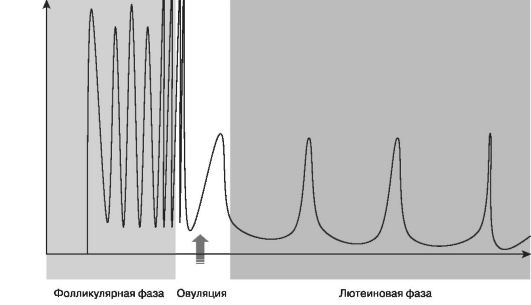
Рис. 5. Схема секреции ГнРГ
Конец каждого менструального цикла и начало следующего характеризуются низким уровнем половых стероидов: прогестерона и эстрогенов.
С прекращением функции желтого тела возрастает продукция ФСГ и ЛГ. Клетки гранулезы взаимодействуют с ФСГ, а клетки внутреннего текального слоя — с ЛГ. Каждый менструальный цикл (рис. 6) от 3 до 30 примордиальных фолликулов под влиянием ФСГ вступают в фазу роста и секретируют эстрогены, уровень которых прогрессивно возрастает в течение 1-й — фолликулярной фазы менструального цикла.

Рис. 6. Менструальный цикл
В процессе роста вторичных фолликулов (к 8-му дню менструального цикла) появляется доминантный фолликул, превращающийся в третичный фолликул (преовуляторный, далее граафов пузырек, до 2-3 см в диаметре).
Синтез эстрогенов обеспечивается двумя путями. Первый путь включает ферментативную ароматизацию гранулезными клетками андрогенов в эстрогены. Второй путь связан с синтезом эстрогенов в текальных клетках на поздних стадиях антральной фазы. Таким образом, в середине фолликулярной фазы нарастает уровень фолликулярных эстрогенов и андрогенов, что сопровождается падением концентрации ФСГ (отрицательная обратная связь).
В то же время эстрогены стимулируют секрецию ЛГ в течение всего фолликулярного периода.
ФСГ стимулирует:
- фазу роста примордиальных фолликулов;
- транспорт жидкости в полость фолликула;
- экспрессию рецепторов к ЛГ и пролактику на клетках гранулезы;
- активность ароматазы. ЛГ стимулирует:
- продукцию фолликулярными клетками низкомолекулярных белков, нейтрализующих фактор, подавляющий мейоз;
- мейотическое деление ооцита и переход в стадию 2-го порядка — гаплоидного набора;
- синтез андрогенов-андростендиона и тестостерона — в клетках theca;
- синтез прогестерона (лютеинизацию) в фолликулярных клетках;
- синтез простагландинов в фолликулярных клетках;
- индукцию овуляции.
В преовуляторной фазе на гранулезных клетках фолликула ФСГ индуцирует развитие рецепторов к ЛГ и пролактину. Таким образом, в конце преовуляторной фазы содержание ФСГ и ЛГ нарастает, а фолликулярные клетки становятся нечувствительными к воздействию эстрогенов и андрогенов. Высокие концентрации эстрогенов стимулируют триггерный выброс ЛГ и разрыв стенки граафова пузырька (третичного фолликула) — т.е. овуляцию, происходящую через 10-12 ч после пика уровня ЛГ. Затем яйцеклетка выходит в брюшную полость, и начинается лютеиновая фаза цикла.
Эстрогены:
- стимулируют пролиферацию фолликулярных клеток;
- стимулируют экспрессию рецепторов ФСГ;
- принимают участие (вместе с ФСГ) в образовании в фолликулярных клетках рецепторов к ЛГ;
- усиливают секрецию ЛГ; при высоком содержании эстрогенов гонадолиберин стимулирует клетки, синтезирующие ЛГ;
- подавлялют секрецию ФСГ; при низком содержании эстрогенов гонадолиберин стимулирует клетки, синтезирующие ФСГ.
Андрогены:
- ингибируют экспрессию рецепторов ФСГ на клетках гранулезы;
- ингибируют активность ароматазы.
В полость фолликула быстро врастают образующиеся капилляры, гранулезные клетки подвергаются лютеинизации под действием ЛГ, что приводит к образованию желтого тела.
Уровень эстрогенов начинает снижаться с конца преовуляторной фазы на фоне высоких концентраций ФСГ и ЛГ, продолжает падать в течение ранней лютеиновой фазы и снова возрастает в результате секреции желтого тела.
Желтое тело (corpus luteum) является транзиторной эндокринной железой, которая функционирует 8-14 дней независимо от продолжительности менструального цикла и синтезирует прогестерон, эстрогены (преимущественно 17b-эстрадиол) и пролактин. Уровень прогестерона постепенно возрастает после овуляции и достигает пика через 8-9 дней после овуляции, что приблизительно соответствует времени имплантации. Термогенный эффект прогестерона приводит к повышению температуры тела как минимум на 0,33 °С (эффект длится до завершения лютеиновой фазы).
Прогестерон:
- подготавливает эндометрий к нидации;
- релаксирует миометральные волокна;
- оказывает натрийуретическое действие, стимулируя секрецию альдостерона;
- плацентарный прогестерон метаболизируется в коре надпочечников и яичках плода в качестве предшественника кортикостероидов и тестостерона соответственно.
Таким образом, лютеиновая фаза характеризуется повышенной концентрацией прогестерона и пролактина и низким уровнем ФСГ и ЛГ.
По мере регресса функции желтого тела происходит снижение концентраций половых стероидов и начинается новый менструальный цикл.
Помимо перечисленных гормонов, желтое тело и в последующем плацента вырабатывают релаксин. Он тормозит сократительную активность миометрия путем активации действия прогестерона и повышения уровня цАМФ как в гладкомышечных клетках миометрия, так и в хондроцитах лонного сочленения, вызывая его размягчение.
Белое тело — соединительнотканный рубец на месте завершившего функцию и дегенерировавшего желтого тела.
ОВАРИАЛЬНЫЙ ЦИКЛ
Число оогониев у эмбриона женского пола к середине внутриутробного развития достигает 5-7 млн, однако значительная часть ооцитов подвергается атрезии (рис. 7), связанной с низкой продукцией гонадотропных гормонов. У новорожденной девочки в яичниках содержится уже 1-2 млн ооцитов; к периоду полового созревания их остается от 100 до 400 тыс. В течение репродуктивного периода 98% примордиальных фолликулов погибают, около 2% достигают стадии первичного и вторичного фолликулов, но овулируют не более 400-500. Все начавшие развитие, но не достигшие стадии овуляции фолликулы подвергаются атрезии.
Таким образом, продолжительность жизни ооцита может достигать 40-50 лет. Именно поэтому риск генных дефектов плода значительно увеличивается с возрастом матери.

Рис. 7. Количество ооцитов в периоды жизни
СТРОЕНИЕ ФОЛЛИКУЛА
Примордиальный фолликул покрыт одним слоем фолликулярных клеток (гранулеза) и окружен базальной мембраной. Окружающие ооцит гранулезные клетки («лучистый венец») секретируют гликопротеиновый субстрат, который образует прозрачную зону — zona pellucida — между ооцитом и гранулезными клетками. На поверхности прозрачной зоны существуют видоспецифические рецепторы взаимодействия только с аллогенными сперматозоидами; пенетрация зоны одним сперматозоидом приводит к развитию «зональной реакции», предотвращающей полиспермию.
Клетки стромы яичника образуют слой веретенообразных клеток — теку. Андрогены, обеспечивающие развитие фолликулов, продуцируются исключительно текальными клетками. Последние в результате пролиферации делятся на два слоя: внутренний, имеющий железистое строение, и наружный — соединительнотканный. Между ними скапливается фолликулярная жидкость, содержащая сывороточный транссудат и мукополисахаридный секрет гранулезных клеток. Накопление жидкости придает фолликулу вид пузырька и такой фолликул называется вторичным или антральным (рис. 8). Находящийся в нем ооцит еще не претерпел второго мейотического деления.
Примордиальный фолликул покрыт одним слоем фолликулярных клеток (гранулеза) и окружен базальной мембраной
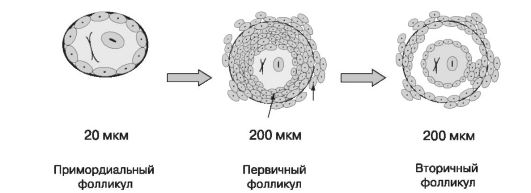
Рис. 8. Рост фолликула
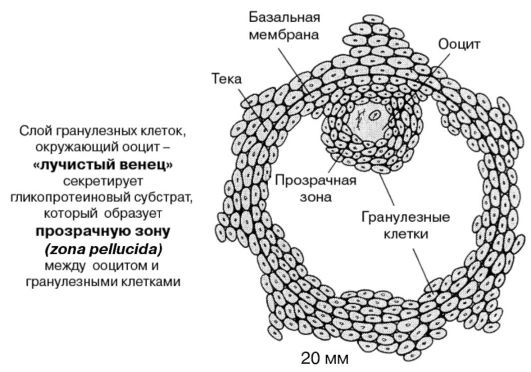
Рис. 9. Третичный фолликул («граафов пузырек»)
Развитие ооцита продолжается вплоть до оплодотворения, а превращение ооцита 1-го порядка в ооцит 2-го порядка, обладающего уже гаплоидным набором хромосом, наступает или непосредственно перед овуляцией, или в фаллопиевой трубе.
Во время каждого овариального цикла в яичниках развивается 15-20 фолликулов. Некоторые из них достигают к середине цикла больших размеров (до 8 мм), но только один фолликул становится зрелым третичным фолликулом с диаметром 2-3 см («граафов пузырек», рис. 9).
МАТОЧНЫЙ ЦИКЛ
Изменения гормонального фона прямо влияют на состояние эндометрия, слизистой оболочки маточных труб, цервикального канала и влагалища. Слизистая оболочка матки подвергается циклическим изменениям (пролиферативная, секреторная и менструальная фазы). В эндометрии различают функциональный (отпадающий при менструации) и базальный (сохраняющийся при менструации) слои.
Пролиферативная фаза — первая половина цикла — длится от первого дня менструации до момента овуляции. Характеризуется регенерацией функционального слоя за счет миграции и пролиферации эпителиальных клеток желез базального слоя на поверхность под влиянием эстрогенов (в основном эстрадиола). В эндометрии происходят формирование новых маточных желез и врастание спиральных артерий из базального слоя. Длительность фазы может варьировать. Базальная температура тела нормальная.
Секреторная фаза — вторая половина — продолжается от овуляции до начала менструации. Эпителиальные клетки прекращают деление и гипертрофируются. Маточные железы расширяются, а железистые клетки активно секретируют гликоген, гликопротеины, липиды и муцин. В поверхностных частях функционального слоя увеличивается количество соединительнотканных клеток, вокруг которых формируются коллагеновые и ретикулярные волокна. Спиральные артерии становятся более извитыми, приближаются к поверхности слизистой оболочки. Если не произошла имплантация плодного яйца, уменьшение содержания стероидных гормонов яичника приводит к скручиванию, склерозированию и уменьшению просвета спиральных артерий, снабжающих верхние две трети функционального слоя эндометрия. В результате происходит ухудшение кровотока в функциональном слое, ишемия и отторжение, т.е. кровотечение.
Менструальная фаза — отторжение функционального слоя эндометрия, продолжается 3-7 дней.
С целью определения времени овуляции используются различные методы функциональной диагностики фаз менструального цикла. Определяются следующие параметры.
1. Базальная температура. Она связана с термогенным действием прогестерона (рис. 10).
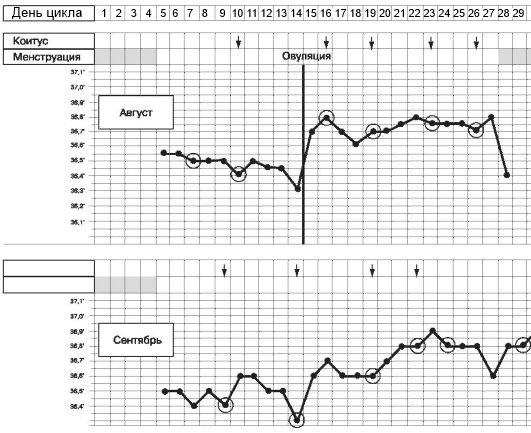
2. Растяжимость шеечной слизи. Под действием эстрогенов значительно увеличивается растяжимость слизи. Максимальных значений достигает во время овуляции (рис. 11)
3. Эффект арборизации шеечной слизи (феномен «папоротника»). Данный феномен максимально выражен в период овуляции за счет высокой концентрации солей натрия, выпадающих в кристаллы (симптом кристаллизации), внешне напоминающие поверхность в виде дерева или папоротника (рис. 12).
4. Кариопикнотический индекс — КПИ (с помощью микроскопического анализа влагалищного мазка).
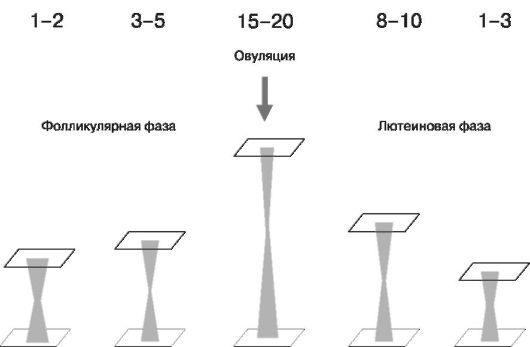
Рис. 11. Степень растяжимости цервикальной слизи

Рис. 12. Феномен «папоротника»
Кариопикнотический индекс является отношением ороговевших клеток с пикнотическими (точечными) ядрами ко всем клеткам влагалищного эпителия в мазке (рис. 13). Наибольшее значение КПИ соответствует периоду овуляции — 70-80%, в остальные дни менструального цикла — до 30-40%.
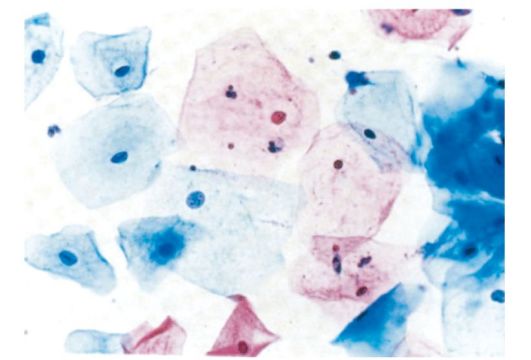
Рис. 13. Кариопикнотический индекс (КПИ)
Эмбриология — наука о зародыше, о закономерностях его развития. Медицинская эмбриология изучает закономерности развития зародыша человека, структурные, метаболические и функциональные особенности плацентарного барьера (система мать-плацента-плод), причины возникновения уродств и других отклонений от нормы, а также механизмы регуляции эмбриогенеза.
В понятие эмбриогенеза включают период от момента оплодотворения до рождения (для живородящих животных), вылупления из яиц (для яйцекладущих), окончания метаморфоза (для животных с личиночной стадией развития).
ОПЛОДОТВОРЕНИЕ
Транспорт гамет. У человека объем эякулята в норме составляет около 3 мл; в нем содержится в среднем 350 млн сперматозоидов. Для обеспечения оплодотворения общее количество сперматозоидов должно быть не менее 150 млн, а концентрация их в 1 мл — не менее 60 млн. Благодаря высокой подвижности сперматозоиды при оптимальных условиях могут через 30 мин — 1 ч достигать полости матки, а через 1,5-2 ч находиться в дистальной (ампулярной) части маточной трубы, где происходит оплодотворение. Спермии сохраняют оплодотворяющую способность до 2 сут.
Вышедший из яичника при овуляции ооцит 1-го порядка имеет диаметр около 130 мкм и окружен плотной блестящей зоной, или мембраной, и венцом фолликулярных клеток, число которых достигает 3-4 тыс. Он подхватывается бахромками маточной трубы (яйцевода) и продвигается по ней. Здесь и заканчивается созревание половой клетки. При этом в результате второго деления образуется ооцит 2-го порядка (яйцеклетка), который утрачивает центриоли и тем самым способность к делению. В ядре яйцеклетки человека содержится 23 хромосомы; одна из них является половой Х-хромосомой.
Свой резерв питательных веществ яйцеклетка человека обычно расходует в течение 12-24 ч после овуляции, а затем погибает, если не будет оплодотворена.
Оплодотворение происходит в ампулярной части яйцевода. Оптимальные условия для взаимодействия сперматозоидов с яйцеклеткой обычно создаются в течение 12 ч после овуляции. При осеменении многочисленные спермии приближаются к яйцеклетке и вступают в контакт с ее оболочкой. Яйцеклетка начинает совершать вращательные движения вокруг своей оси со скоростью 4 вращения в минуту. Эти движения обусловлены биением жгутиков сперматозоидов и продолжаются около 12 ч. В процессе взаимодействия мужской и женской половых клеток в них происходит ряд изменений. Для спермиев характерны явления капацитации и акросомальная реакция. Капацитация представляет собой процесс активации спермиев в маточной трубе под влиянием слизистого секрета железистых клеток. Активизирует секрецию железистых клеток прогестерон. После капацитации следует акросомальная реакция, при которой происходит выделение из сперматозоидов ферментов — гиалуронидазы и трипсина. Гиалуронидаза расщепляет гиалуроновую кислоту, содержащуюся в блестящей зоне. Трипсин расщепляет белки цитолеммы яйцеклетки и клеток лучистого венца. В результате происходят диссоциация клеток лучистого венца и растворение блестящей зоны.
В яйцеклетке цитолемма в области прикрепления спермия образует приподнимающий бугорок, куда входит один сперматозоид, и возникает плотная оболочка — оболочка оплодотворения, препятствующая вхождению других спермиев и явлению полиспермии. Ядра женской и мужской половых клеток превращаются в пронуклеусы, сближаются, наступает стадия синкариона. Возникает зигота, и к концу 1-х суток после оплодотворения начинается дробление.
Пол ребенка зависит от половых хромосом отца. В связи с большей чувствительностью эмбрионов мужского пола к повреждающему действию различных факторов число новорожденных мальчиков меньше, чем девочек: на 100 мальчиков рождаются 105 девочек.
Движение оплодотворенной яйцеклетки обеспечивается перистальтическими сокращениями мускулатуры трубы и мерцанием ресничек эпителия. Питание зародыша осуществляется за счет небольших запасов желтка в яйцеклетке и, возможно, содержимого маточной трубы.
Транспорт зародыша к матке происходит в иммуносупрессивной среде, в образовании которой важную роль играют сперматозоиды, бластоцистная жидкость, а2-маточный протеин (начинает продуцироваться железистым эпителием эндометрия в ближайшие дни после овуляции) и фактор ранней беременности (ФРБ), впервые описанный H. Morton в 1974 г. ФРБ продуцируется яйцеклеткой через 46-48 ч после оплодотворения и является одним из первых показателей наступившей беременности и наиболее ранним иммуносупрессивным агентом, предотвращающим отторжение бластоцисты. Факторы иммунологической защиты:
- а2-протеин эндометриальных желез;
- фактор ранней беременности яйцеклетки;
- иммуноблокирующие белки синцитиотрофобласта;
- ХГ и плацентарный лактоген (ПЛ);
- ликопротеиды фибриноида плаценты;
- протеолитические свойства трофобласта.
Дробление зародыша человека начинается к концу 1-х суток и продолжается в течение 3-4 суток после оплодотворения (по мере продвижения зародыша к матке). Дробление зиготы человека — полное, неравномерное, асинхронное. В течение 1-х суток оно происходит медленно. Первое деление завершается через 30 ч; при этом борозда дробления проходит по меридиану и образуется два бластомера. За стадией двух бластомеров следует стадия четырех бластомеров. Через 40 ч образуются четыре клетки (рис. 14).
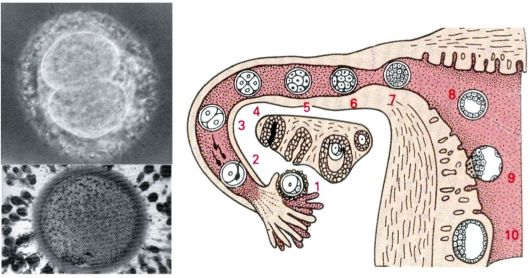
Рис. 14. Стадии развития оплодотворенной яйцеклетки
С первых же делений формируются два вида бластомеров: «темные» и «светлые». «Светлые» бластомеры дробятся быстрее и располагаются одним слоем вокруг «темных», которые оказываются в середине зародыша. Из поверхностных «светлых» бластомеров в дальнейшем возникает трофобласт, связывающий зародыш с материнским организмом и обеспечивающий его питание. Внутренние «темные» бластомеры формируют эмбриобласт — из него образуются тело зародыша и все остальные внезародышевые органы, кроме трофобласта. К моменту попадания бластоцисты в матку она увеличивается в размерах благодаря росту числа бластомеров и объема жидкости вследствие усиленного всасывания трофобластом секрета маточных желез и активной выработки жидкости самим трофобластом.
В трофобласте увеличивается количество лизосом, в которых накапливаются ферменты, обеспечивающие лизис тканей матки и тем самым способствующие внедрению зародыша в толщу слизистой оболочки матки, т.е. нидации. Имплантация (нидация) начинается с 7-х суток после оплодотворения и продолжается около 40 ч (рис. 15). При этом бластоциста оказывается полностью окруженной тканью эндометрия — децидуальной оболочкой.
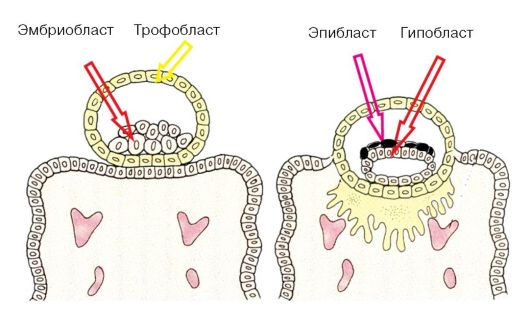
Рис. 15. Нидация бластоцисты
Слой трофобласта вскоре дифференцируется в наружный слой — синцитиотрофобласт, постоянно пополняющийся ядрами и цитоплазмой за счет лежащего под ним внутреннего слоя цитотрофобласта (слой Лангханса), так как деление ядер наблюдается только в цитотрофобласте. Третье производное трофобласта не имеет способности к размножению и представляет собой мононуклеарный тип клеток, которые изначально были обозначены как «Х-клетки» и известны также как «промежуточный трофобласт». Это основной тип клеток, составляющих плацентарную площадку и с клетками децидуальной оболочки внедряющихся в материнские спиральные артерии, а также формирующих основную массу клеток плацентарных перегородок. Х-клетки являются основным источником человеческого плацентарного лактогена (HPL — human placental lactogen) и большого количества основного протеина беременности (MBP — major basic protein)
В течение первых 2 нед трофобласт потребляет продукты распада материнских тканей (гистиотрофный тип питания). Затем синцитиотрофобласт, разрастаясь в виде ворсинок и продуцируя протеолитические ферменты, внедряется в матку, разрушает материнские децидуальные сосуды, тем самым позволяя крови матери изливаться в неравномерные лакуны — являющиеся будущим «межворсинчатым пространством». Таким образом, трофобласт вступает в непосредственный контакт с кровью материнских сосудов и зародыш начинает получать питание непосредственно из материнской крови (гематотрофный тип питания). Полноценное кровообращение у плода устанавливается примерно на 5-й неделе после оплодотворения.
После завершения имплантации в развитии эмбриона начинается очень ответственный период органогенеза и плацентации. С 20-21-х суток происходит обособление тела зародыша от внезародышевых органов и окончательное формирование осевых зачатков. Органогенез завершается к 12-16-й неделе внутриутробной жизни.
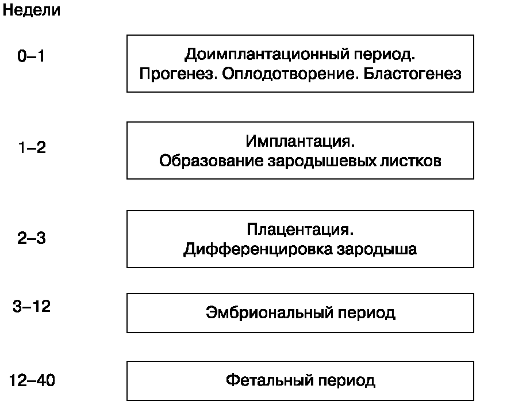
Рис. 16. Периоды антенатального развития
Эмбриональная масса дифференцируется, формируются зародышевые листки: 1) эктодерма; 2) мезодерма; 3) эндодерма. Они тоже дифференцируются (рис. 17).
Рис. 17. Дифференцировка зародышевых листков
Из эктодермы образуется нервная трубка. Замыкание нервной трубки начинается в шейном отделе, затем распространяется кзади и в краниальном направлении, где формируются мозговые пузыри. Примерно на 25-е сутки нервная трубка полностью замыкается, и с внешней средой сообщаются только два не замкнувшихся отверстия на переднем и заднем концах — передний и задний невропоры. Еще через 5-6 суток оба невропора зарастают. При смыкании боковых стенок нервных валиков и образовании нервной трубки появляется так называемый нервный гребень. Клетки нервного гребня способны к миграциям. В туловище мигрирующие клетки образуют парасимпатические и симпатические ганглии и мозговое вещество надпочечников. Часть клеток остается в области нервного гребня, они сегментируются и дают начало спинномозговым узлам.
Дифференцировка мезодермы начинается с 20-х суток эмбриогенеза.
Клетки мезодермы устремляются к внутренней поверхности полости бластоцисты и дифференцируются в соединительную ткань хориона и ворсин. Место, где эти клетки покидают эмбрион, становится пупочным канатиком, в который прорастают аллантоисные сосуды будущей плаценты.
Изменения в самом зародыше выражаются в том, что дорсальные участки мезодермальных листков разделяются на плотные сегменты, лежащие по сторонам от хорды, — сомиты. Процесс образования сегментов, или сомитов, начинается в головной части зародыша и распространяется в каудальном направлении. И если на 22-е сутки развития у эмбриона имеется 7 пар сегментов, то на 35-е сутки — 44 пары. В процессе дифференцировки мезодермы возникает нефрогенный зачаток и эмбриональный зачаток соединительной ткани — мезенхима. В образовании мезенхимы частично принимают участие экто- и эндодермальные клетки.
Эндодерма формирует полость — первичную кишку, будущую пищеварительную трубку, которая развивается через стадию формирования желточного мешка. Выделение кишечной эндодермы начинается с момента появления туловищной складки, которая, углубляясь, отделяет зародышевую эндодерму — первичную кишку — от внезародышевой эндодермы — желточного мешка. В начале 4-й недели на переднем конце зародыша образуется эктодермальное впячивание — ротовая ямка. Углубляясь, ямка доходит до переднего конца кишки и после прорыва разделяющей их мембраны превращается в ротовое отверстие будущего ребенка.
Желточный мешок и пищеварительная трубка некоторое время остаются связанными между собой через омфаломезентериальный проток (желточный стебелек), заканчивающийся в потенциальном дивертикуле Меккеля. Желточный стебелек, как и желточный мешок, в последующем атрофируется.
Таким образом, желточный мешок, образованный внезародышевой эндодермой и внезародышевой мезодермой, принимает активное участие в питании и дыхании эмбриона человека очень недолго. Основная роль желточного мешка — кроветворная. В качестве кроветворного органа он функционирует до 7-8-й недели, а затем подвергается обратному развитию. В стенке желточного мешка формируются первичные половые клетки — гонобласты, мигрирующие из него с кровью в зачатки половых желез.
В задней части зародыша в состав образующейся кишки входит и тот участок эндодермы, из которого возникает энтодермальный вырост аллантоиса.
Аллантоис представляет собой небольшой пальцевидный отросток эндодермы, врастающий в амниотическую ножку. У человека аллантоис не очень развит, но его значение в обеспечении питания и дыхания зародыша всеже велико, так как по нему к хориону растут сосуды, конечные разветвления которых залегают в строме ворсин. На 2-м месяце эмбриогенеза аллантоис редуцируется.
На рис. 18 показано, как выглядит эмбрион в 4-5 нед.
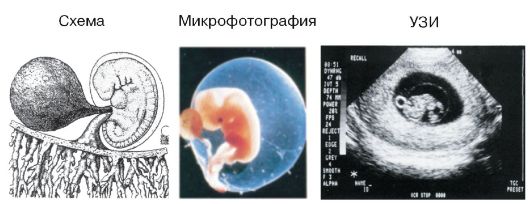
Рис. 18. Эмбрион в 4-5 нед
В периоды органогенеза (рис. 19) и плацентации в результате патогенного действия факторов внешней среды у эмбриона и плода в первую очередь поражаются те органы и системы, которые находятся в это время в процессе дифференцировки. У различных закладок органов зародыша критические периоды не совпадают по времени друг с другом. Поэтому действие повреждающего фактора обычно вызывает уродства различных органов и систем. Наиболее чувствительная фаза развития — первые 3-6 нед онтогенеза (второй критический период развития).
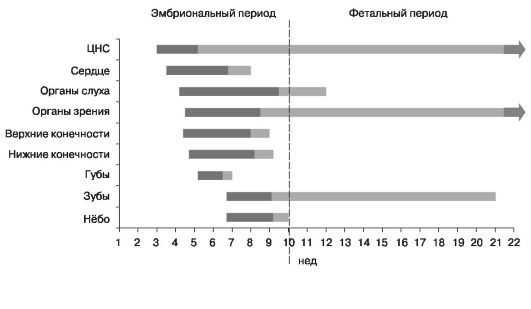
Рис. 19. Периоды органогенеза
ВНУТРИУТРОБНЫЙ РОСТ ПЛОДА
Динамика роста плода в матке обеспечивается взаимодействием генетического потенциала каждого индивидуального плода и внутриматочной средой, связанной в первую очередь с функцией плаценты и гомеостазом матери. Динамика роста плода при физиологической беременности соответствует гестационному возрасту (табл. 1).
Таблица 1. Динамика роста плода
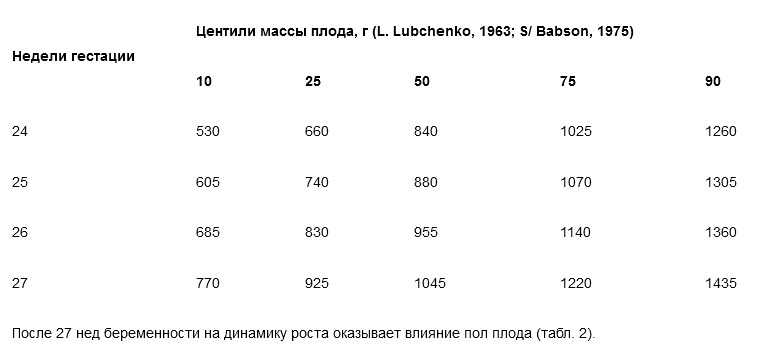
Таблица 2а. Динамика роста плода в зависимости от пола (мальчики)
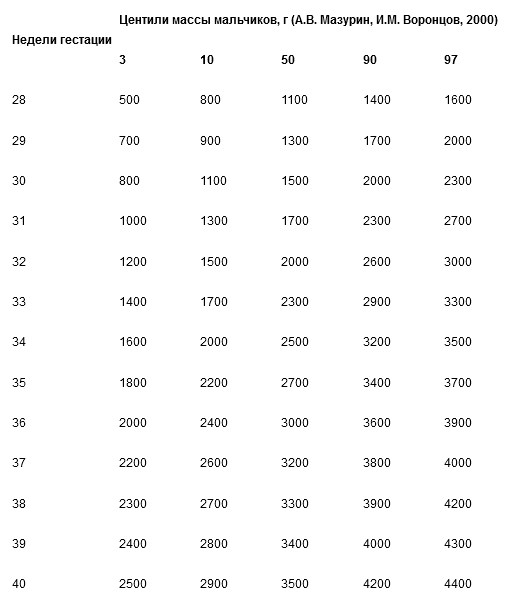
Таблица 2б. Динамика роста плода в зависимости от пола (девочки)
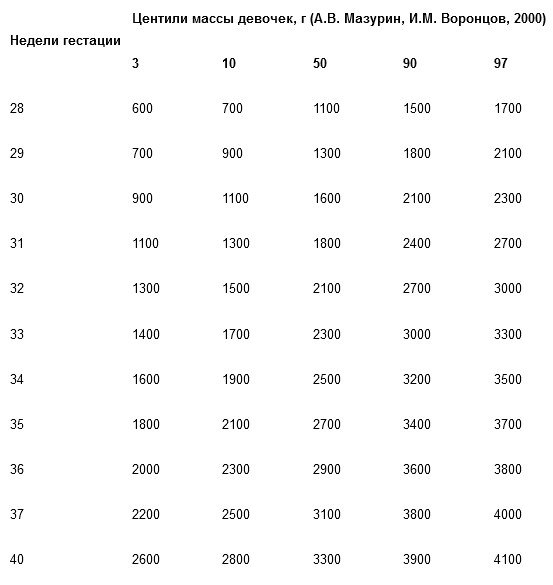
Несоответствие размеров плода фактическому сроку беременности определяется понятием «задержка внутриутробного развития» (ЗВУР) плода. Международным критерием ЗВУР является масса тела и/или рост плода, меньшие, чем нормальные для данного гестационного возраста (10-й центиль и ниже). Синдром ЗВУР — одно из клинических проявлений плацентарной недостаточности.
Плацента — внезародышевый орган, за счет которого устанавливается связь зародыша с организмом матери. Плацента человека относится к типу дискоидальных гемохориальных ворсинчатых плацент. Формирование плаценты начинается на 3-й неделе, когда во вторичные (эпителиомезенхимные) ворсины, начинают врастать сосуды, образуя третичные ворсины, и заканчивается в 14-16 нед беременности.
В плаценте различают зародышевую, или плодную, часть и материнскую, или маточную.
Плодная часть представлена ветвистым хорионом и приросшей к нему амниотической оболочкой, а материнская — видоизмененной базальной частью эндометрия.
Зародышевая, или плодная, часть плаценты к концу 3-го месяца представлена ветвящейся хориальной пластинкой, состоящей из волокнистой (коллагеновой) соединительной ткани, покрытой цито- и синцитиотрофобластом. Ветвящиеся ворсины хориона (стволовые, или якорные, ворсины) хорошо развиты лишь со стороны, обращенной к миометрию. Здесь они проходят через всю толщу плаценты и своими вершинами погружаются в базальную часть разрушенного эндометрия.
Структурно-функциональной единицей сформированной плаценты является котиледон, образованный стволовой ворсиной и ее вторичными и третичными разветвлениями. Общее количество котиледонов в плаценте достигает 200.
Материнская часть плаценты представлена базальной пластинкой и соединительнотканными септами, отделяющими котиледоны друг от друга, а также лакунами, заполненными материнской кровью.
На поверхности базальной пластинки, обращенной к хориальным ворсинам, находится аморфная субстанция — фибриноид Рора. Трофобластические клетки базальной пластинки вместе с фибриноидом играют существенную роль в обеспечении иммунологического гомеостаза в системе мать-плод.
Кровь в лакунах непрерывно обновляется. Она поступает из маточных артерий, входящих сюда из мышечной оболочки матки. Эти артерии идут по плацентарным перегородкам и открываются в лакуны. Материнская кровь оттекает от плаценты по венам, берущим начало от лакун.
Кровь матери и кровь плода циркулирует по самостоятельным сосудистым системам и не смешивается между собой. Гемохориальный барьер, разделяющий оба кровотока, состоит из эндотелия сосудов плода, окружающей сосуды соединительной ткани, эпителия хориальных ворсин (цитотрофобласт, синцитиотрофобласт), а кроме того, из фибриноида, который местами покрывает ворсины снаружи.
Плацента выполняет трофическую, экскреторную (для плода), эндокринную (вырабатывает ХГ, прогестерон, ПЛ, эстрогены и др.), защитную (включая иммунологическую защиту) функции.
Значение ХГ
- Стимулирует продукцию прогестерона желтым телом.
- Участвует в иммунологической защите — угнетает материнские лимфоциты.
- Стимулирует лейдиговые клетки плодов мужского пола и продукцию тестостерона.
- Определяет развитие мужских половых органов.
- Является ранним маркером беременности.
- Является критерием оценки эффективности лечения трофобластической опухоли, а также индуктором овуляции вследствие биологического сходства с ЛГ
Свойства ПЛ
- Участвует в иммунологической защите — угнетает материнские лимфоциты.
- Стимулирует липолиз и повышает концентрацию свободных жирных кислот.
- Ингибирует глюконеогенез матери.
- Увеличивает уровень инсулина в плазме.
- Стимулирует синтез белков и аминокислот вследствие инсулиногенного эффекта.
- Концентрация ПЛ зависит от массы плаценты.
Амниотическая оболочка. Она бессосудистая и образует самую внутреннюю стенку плодовместилища. Основная его функция — выработка околоплодных вод, обеспечивающих среду для развивающегося организма и предохраняющих его от механического повреждения. Эпителий амниона, обращенный в его полость, выделяет околоплодные воды, а также принимает участие в обратном всасывании их. При этом в эпителии амниона, покрывающем плацентарный диск, имеет место преимущественно секреция, а в эпителии внеплацентарного амниона — преимущественно резорбция околоплодных вод. Амниотическая жидкость создает необходимую для развития зародыша водную среду, поддерживая до конца беременности необходимый состав и концентрацию солей в околоплодной жидкости. Амнион выполняет также защитную функцию, предупреждая попадание в плод вредоносных агентов.
Амнион рыхло связан с хорионом, в котором располагаются сосуды плода. Его прикрепление к хориону происходит примерно на 12-й неделе беременности; до этого между амнионом и хорионом существует пространство, заполненное жидкостью. К тому же, амнион часто смещается при беременности и способен даже отслоиться задолго до родов. Он также порой формирует тяжи, которые при соприкосновении с плодом могут стать причиной пренатальных ампутаций и других уродств. Так как амнион связан с пуповиной и плотно к ней прикреплен, то остатки тяжей чаще всего обнаруживаются в месте прикрепления пуповины.
Пупочный канатик
Пупочный канатик образуется в основном из мезенхимы, находящейся в амниотической ножке и желточном стебельке. В формировании канатика принимают участие также аллантоис и растущие по нему сосуды. С поверхности все эти образования окружены амниотической оболочкой. Желточный стебелек и аллантоис быстро редуцируются, и в пупочном канатике новорожденного находят лишь их остатки.
Сформированный пупочный канатик — упругое соединительнотканное образование, в котором проходят две пупочные артерии и пупочная вена. Он образован типичной студенистой (слизистой) тканью, в которой содержится огромное количество гиалуроновой кислоты. Именно эта ткань, получившая название вартонова студня, обеспечивает тургор и упругость канатика. Она предохраняет пупочные сосуды от сжатия, обусловливая тем самым непрерывное снабжение эмбриона питательными веществами, кислородом.
В норме пуповина прикреплена на диске плаценты (центральное прикрепление), в 7% наблюдается краевое прикрепление (battledore), а в 1% — на плодных оболочках (оболочечное прикрепление). Аномальные прикрепления больше характерны для многоплодной беременности. Оболочечное прикрепление плаценты не связано с аномалиями плода, но может быть опасно из-за повышенной частоты сосудистых тромбозов и из-за возможности кровотечения из разрывающихся во время родов сосудов.
Длина пуповины во многом определяется двигательной активностью плода. Так, короткая пуповина нередко свидетельствует о его неподвижности вследствие нейромышечной патологии или амниотических сращений. Напротив, длинная пуповина порой является результатом повышенной двигательной активности плода.
Единственная артерия пуповины встречается более чем в 1% случаев, чаще при многоплодной беременности. Около половины таких новорожденных имеют врожденные аномалии, некоторые из которых следует активно диагностировать, и другие перинатальные проблемы. Единственная артерия пуповины, однако, может быть и у совершенно нормального новорожденного; тогда эта находка лишь сигнализирует о необходимости настороженности в отношении наличия патологии у данного новорожденного.
Несмотря на то, что организм матери и плода генетически чужеродны по составу белков, иммунологического конфликта обычно не происходит. Это обеспечивается рядом факторов; из них особенно важны следующие:
- 1 — синтезируемые синцитиотрофобластом белки, тормозящие иммунный ответ материнского организма;
- 2 — ХГ и ПЛ, находящиеся в высокий концентрации на поверхности синцитиотрофобласта, принимающие участие в угнетении материнских лимфоцитов;
- 3 — иммуномаскирующее действие гликопротеинов фибриноида плацеты, заряженного, как и лимфоциты омывающей крови, отрицательно;
- 4 — протеолитические свойства трофобласта, также способствующие инактивации чужеродных белков;
- 5 — амниотические воды с антителами, блокирующими антигены А и В (содержащиеся в крови беременной) и не допускающими их в кровь плода в случае несовместимой беременности.
В процессе формирования системы мать-плод существует ряд критических периодов, наиболее значимых для установления взаимодействия между двумя системами и для создания оптимальных условий развития плода.
В онтогенезе человека можно выделить несколько критических периодов развития: в прогенезе, эмбриогенезе и постнатальной жизни. К ним относятся:
- 1) развитие половых клеток — овогенез и сперматогенез;
- 2) оплодотворение;
- 3) имплантация (7-8-е сутки эмбриогенеза);
- 4) развитие осевых зачатков органов и формирование плаценты (3-8-я неделя развития);
- 5) стадия усиленного роста головного мозга (15-20-я неделя);
- 6) формирование основных функциональных систем организма и дифференцировка полового аппарата (20-24-я неделя);
- 7) рождение;
- 8) период новорожденности (до 1 года);
- 9) половое созревание (11-16 лет).
