Химико-токсикологическое значение и анализ хлорорганических пестицидов
- 11.2.1. Гексахлорциклогексан (ГХЦГ)
- 11.2.2. Гептахлор
- 11.2.3. Токсикологическое значение других хлорорганических пестицидов
В группу хлорорганических пестицидов входят перхлорированные углеводороды, которые широко применяются, в основном, как инсектициды. Производные хлорфенок- сиуксусной кислоты используются как средства для борьбы с сорными растениями. Особенностью хлорсодержащих ядохимикатов является их способность сохраняться в почве, воде и растениях длительное время. Например, ДДТ может сохраняться в почве 8-12 лет после обработки растений. Некоторые хлорорганические пестициды обнаруживаются в тканях животных за много километров от места применения за счет переноса их воздушными потоками. Все они медленно разрушаются в окружающей среде, поэтому вымываются водой из почвы и могут попадать в водоемы.
В организм человека хлорорганические соединения попадают через ЖКТ вместе с пищевыми продуктами, через легкие при вдыхании пыли. Некоторые пестициды этой труппы могут всасываться через неповрежденную кожу. Большинство хлорсодержащих пестицидов обладает кумулятивными свойствами, поэтому при длительном контакте с ними могут наблюдаться хронические отравления Предварительный анализ объекта на группу хлорорганических пестицидов
Специальных тестов для этих целей не разработано, предложено использовать метод тонкослойной хроматографии и реакцию отщепления хлора. Этим методам можно придать судебно-химическое значение при отрицательном результате.
Объект анализа массой 10 г (содержимое желудка, образцы веществ, изъятых с места происшествия) экстрагируют дважды петролейным эфиром, используя роторный смеситель. Эфирные экстракты промывают последовательно водой очищенной, раствором гидроксида натрия и еще раз водой очищенной. Слой петролейного эфира фильтруют через безводный сульфат натрия.
Анализ с помощью хроматографии в тонком слое сорбента. Часть полученного экстракта наносят на хроматографическую пластинку с тонким слоем силикагеля, подсушивают и хроматографируют. В качестве подвижной системы используют циклогексан. Затем пластинку вынимают, высушивают и обрабатывают раствором перманганата калия, опрыскивают 2-аминоэтанолом и нагревают 20 мин при 100°С. Охлажденную пластинку обрабатывают раствором нитрата серебра и облучают УФ-лампой (254 нм) в течение 10-15 мин. При наличии в объекте хлорсодержащих пестицидов образуются пятна коричневого или черного цвета.
Реакция отщепления хлора. Часть извлечения из объекта в специальном приборе испаряют досуха, добавляют к остатку концентрированную серную кислоту, дихромат калия и сульфат серебра в качестве катализатора. Смесь нагревают, происходит разрушение хлорсодержащего соединения, и выделяется свободный хлор, который улавливают в раствор йодида кадмия в присутствии крахмала — образуется синее окрашивание за счет вытеснения йода хлором.
Cdl2 + Cl2 → CdCI2 +I2
При обнаружении пятен на пластинке и получении положительной реакции отщепления хлора проводят основное исследование на отдельные хлорсодержащие пестициды.
11.2.1 Гексахлорциклогексан (ГХЦГ)
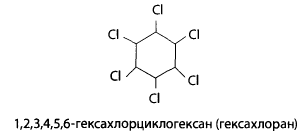
Гексахлоран имеет несколько пространственных изомеров, из них у-изомер проявляет инсектицидные свойства и выпускается по названием линдан.
ГХЦГ — вещество темно-серого или светло-серого цвета, малорастворимое в воде, при повышенной температуре возгоняется с частичным разложением. Применяется ГХЦГ в виде порошков (дустов), эмульсий, дымовых шашек. Он используется для борьбы с вредителями зерновых культур, садов, лесных насаждений, паразитами животных.
Токсическое действие ГХЦГ на человека проявляется в виде гиперемии кожи, отечности, раздражении конъюнктивы глаз. ГХЦГ длительно задерживается в организме (в жировой ткани), медленно выводится через почки, ЖКТ, переходит в молоко кормящей матери. При приеме внутрь ГХЦГ вызывает тошноту, при всасывании в кровь поражается ЦНС, наблюдаются клонические и тонические судороги. Летальная доза составляет 200 мг/кг.
Метаболизм гексахлорана в организме проходит по пути дехлорирования, гидрокси- лирования и образования глюкуронидов во второй фазе метаболизма.
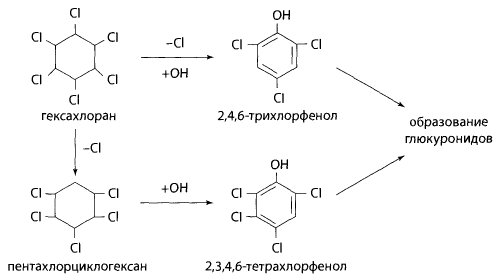
Объекты исследования: желудок с содержимым, печень, почки, кровь, моча.
Для изолирования из желудка с содержимым, печени или почек 100 г объекта измельчают, помещают в круглодонную колбу, смешивают с водой до кашицеобразной массы. Далее проводят перегонку с водяным паром. Собирают 300 мл дистиллята. В ходе перегонки на внутренней стенке холодильника может появиться серовато-белый налет, а в дистилляте белые частицы ГХЦГ. После отгонки холодильник промывают эфиром. Эфирный раствор присоединяют к дистилляту. Дистиллят переносят в делительную воронку и три раза экстрагируют диэтиловым эфиром по 100 мл. Эфирные вытяжки объединяют, промывают водой в делительной воронке. Затем эфир отгоняют до небольшого объема, переносят в выпарительную чашку и осторожно упаривают до сиропообразной массы. Эту массу используют для обнаружения ГХЦГ следующими испытаниями.
Реакция дехлорирования с последующим нитрованием. Часть остатка из чашки помещают в колбу с обратным холодильником, добавляют двукратный объем 10% спиртового раствора гидроксида калия и нагревают в течение часа на водяной бане. При кипячении со спиртовой щелочью ГХЦГ отщепляет 3 и более атомов хлора.
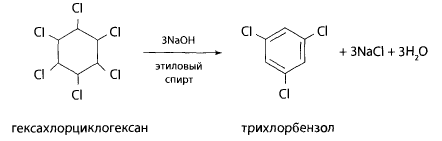
Затем упаривают эту смесь до 1/3 объема, подкисляют азотной кислотой и прибавляют раствор нитрата серебра. При этом выпадает белый осадок хлорида серебра.
NaCI + AgNО3 → AgCI ↓ + NaNО3
Полученный осадок отфильтровывают, фильтрат упаривают до небольшого объема, добавляют к нему 0,1 г нитрата натрия и 2 мл концентрированной серной кислоты. Смесь нагревают на песчаной бане в течение 10 мин при температуре 125-130°С. После охлаждения смесь экстрагируют в делительной воронке диэтиловым эфиром. Эфир осторожно выпаривают. Остаток растворяют в 0,5 мл ацетона и добавляют 2 мл 10% спиртового раствора гидроксида калия — появляется красно-фиолетовая или розовая окраска. Предел обнаружения — 4 мг ГХЦГ в 100 г объекта.
При дехлорировании ГХЦГ образуется бензол или хлорбензол, которые при взаимодействии с серной кислотой и нитратом натрия превращаются в п-нитро- или м-динитропроизводные, Нитропроизводные с ацетоном и гидроксидом калия образуют окрашенные соединения состава:
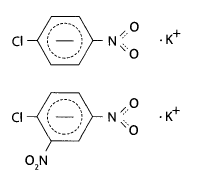
Реакция с янтарной кислотой и сульфатом железа(Ш). К части сухого остатка из чашки добавляют несколько кристалликов янтарной или фталевой кислоты. Отверстие пробирки закрывают фильтровальной бумагой, смоченной 0,1% раствором сульфата железа(Ш). Пробирку погружают в глицериновую баню, нагретую до 200°С, и температуру бани постепенно повышают до 230°С. При наличии ГХЦГ в пробе на бумаге появляется синее пятно.
Можно предположить, что в результате реакции ГХЦГ с янтарной (фталевой) кислотой образуются летучие фенольные соединения, которые дают с сульфатом железа(ПГ) синее окрашивание. Предел обнаружения составляет 30 мг ГХЦГ в пробе.
Для изолирования ГХЦГ из крови в пробирку с притертой пробкой вносят 2 мл цельной крови, 10 мл диэтилового эфира, смесь взбалтывают 15 мин и сливают эфирную вытяжку. Экстрагирование повторяют еще 2 раза с 10 мл эфира. Эфирные вытяжки сливают вместе, добавляют к ним 5 г безводного сульфата натрия и взбалтывают в течение 10 мин. Затем эфирную вытяжку отделяют, осторожно упаривают до небольшого остатка (около 1 мл).
Для изолирования ГХЦГ из мочи 20 мл мочи экстрагируют трижды эфиром по 20 мл. Далее экстракты обрабатывают безводным сульфатом натрия и после упаривания оставшуюся эфирную вытяжку используют для обнаружения и количественного определения ГХЦГ.
Обнаружение ГХЦГ в извлечениях из крови и мочи проводят с помощью тонкослойной хроматографии и описанных выше реакций.
Обнаружение ГХЦГ методом ТСХ. На линию старта хроматографической пластинки со слоем силикагеля наносят несколько капель эфирной вытяжки. Рядом наносят каплю «стандарта». Пятна подсушивают и хроматографируют, используя в качестве подвижной фазы н-гексан. После окончания хроматографирования пластинку подсушивают и обрабатывают водно-ацетоновым аммиачным раствором нитрата серебра, а затем облучают УФ-лучами в течение 15-20 мин. ГХЦГ проявляется в виде серо-черных пятен
Для количественного определения ГХЦГ рекомендованы методы ГЖХ, фотоколориметрии и аргентометрии.
При газожидкостной хроматографии используют электронозахватный детектор (ДЭЗ). Определение с помощью детекторов такого типа основано на измерении электропроводности между двумя электродами. В ДЭЗ ионы образуются под воздействием радиоактивного излучения. Его источником могут быть 3Н, 63Ni, 90Sr и др. Детектор состоит из ионизационной камеры с источником радиоактивного излучения и блока питания (2 электрода с определенной разницей потенциалов). Когда в детектор поступает соединение, способное захватывать электроны, происходит изменение электропроводности между электродами. Свойством захватывать электроны обладают молекулы химических соединений, в состав которых входят атомы галогенов, фосфора, серы, азота, кислорода. Обнаружение хлорсодержащих пестицидов проводят по времени удерживания, а количественное определение — по высоте или площади пика.
Фотоколориметрический метод. Он используется чаще всего для определения ГХЦГ в крови и моче. Метод основан на дехлорировании ГХЦГ до бензола или хлорбензола, переведении их в нитропроизводные и получении окрашенных соединений с гидроксидом калия в присутствии ацетона. Дехлорирование ГХЦГ в остатке после испарения эфира проводят с помощью цинковой пыли в присутствии 2 мл ледяной уксусной кислоты.
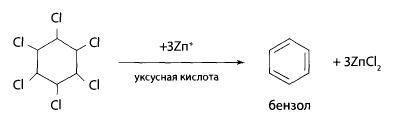
К полученному раствору добавляют 1 мл нитрующей смеси (10% раствор нитрата аммония в концентрированной серной кислоте) и нагревают в течение часа на асбестовой сетке. После охлаждения смесь экстрагируют эфиром, эфир испаряют и к сухому остатку добавляют ацетон и 1 мл 40% раствора гидроксида натрия.
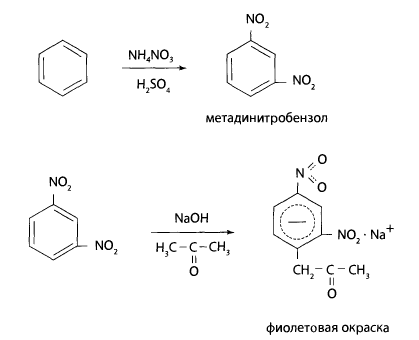
Через 20 мин измеряют оптическую плотность окрашенного в фиолетовый цвет раствора с помощью фотоколориметра в кювете с толщиной поглощающего слоя 20 мм с зеленым светофильтром.
Определение ГХЦГ аргентометрическим методом проводят по методике, описанной ранее при определении алкилгалогенидов (см. раздел 9.4.6).
11.2.2 Гептахлор
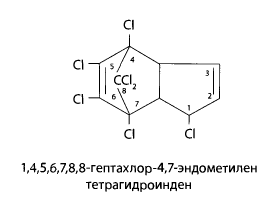
Гептахлор — это белое кристаллическое вещество со слабым камфорным запахом, нерастворим в воде, растворяется в органических растворителях. Промышленностью гептахлор выпускается в виде 25% концентрата эмульсии и применяется в качестве инсектицида.
При попадании в организм через кожу проявляется резорбтивное действие гептахлора. При вдыхании пыли отмечаются головные боли, тошнота, диспепсические явления. ПДК в воздухе рабочей зоны составляет 0,01 мг/м3. Остаточные количества в пищевых продуктах не допускаются. При попадании в желудок гептахлор вызывает тяжелые поражения паренхиматозных тканей и ЦНС.
В организме гептахлор окисляется до эпоксигептахлора, который отличается более высокой токсичностью, чем сам гептахлор. Гептахлор и эпоксигептахлор накапливаются в тканях организма и оказывают токсическое действие. В почве продукты метаболизма гептахлора сохраняются в течение нескольких лет.
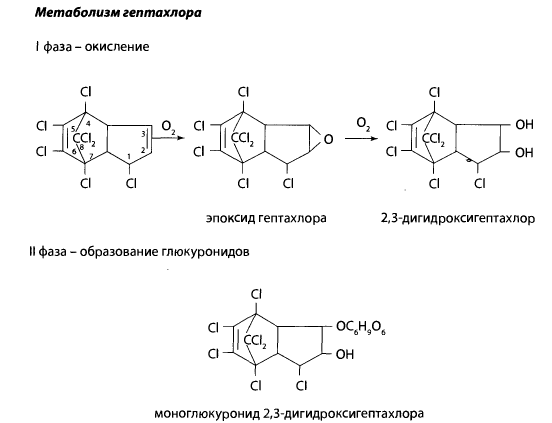
Объектами исследования являются кровь, моча, при смертельном отравлении — желудок с содержимым, печень.
Для изолирования гептахлора лучшими экстрагентами являются диэтиловый эфир, бензол, гексан.
Извлечение гептахлора из цельной крови проводят 3 раза по 10 мл, из 20 мл мочи 3 раза по 20 мл экстрагента. Для изолирования из паренхиматозных органов 100 г объекта настаивают трехкратно в течение 30 мин с диэтиловым эфиром или гексаном по 100, 50 и 50 мл. Вытяжки в каждом случае объединяют, обрабатывают безводным сульфатом натрия или взбалтывают с насыщенным раствором сульфата натрия в 20% растворе серной кислоты с целью очистки, упаривают до минимального объема и далее используют для качественного и количественного определения.
Для обнаружения гептахлора используют следующие реакции.
Реакция гептахлора с диэтиламином. Часть извлечения выпаривают досуха. Остаток растворяют в дихлорэтане, затем по стенке пробирки добавляют 5-7 капель смеси диэтиламина и 0,1 М раствора гидроксида калия в метаноле (1:2). Смесь взбалтывают — появляется зеленая, быстро исчезающая окраска.
Реакция с диэтаноламином проводится, как и предыдущая. В качестве реактива используется смесь диэтаноламина и 0,1 М раствора гидроксида калия в метаноле (1:2). При наличии гептахлора появляется фиолетовое окрашивание.
Реакция с анилином и пиридином. Часть извлечения испаряют досуха, остаток растворяют в бензоле, добавляют 5 капель анилина и 2 капли 0,1 М раствора гидроксида калия в метаноле. Смесь нагревают на водяной бане 15 с и прибавляют 1 мл пиридина и снова помещают в водяную баню на 10 с. Смесь перемешивают. Через 1-3 мин появляется темно-зеленое окрашивание.
Реакция с раствором гидроксида калия. К части извлечения прибавляют 1 мл 0,1 М раствора гидроксида калия в метаноле и взбалтывают. Пробирку помещают на 30 с в водяную баню, затем прибавляют 1 мл бензола. Постепенно развивается розовое или пурпурное окрашивание.
Количественное определение. Для количественного определения используют метод ГЖХ с электронно-захватным детектором. Определение ведут по высоте или площади пика в присутствии внутреннего стандарта.
11.2.3 Токсикологическое значение других хлорорганических пестицидов
В настоящее время число хлорорганических пестицидов насчитывает несколько десятков. Все они имеют определенное токсикологическое значение и вносят вклад в «токсическую ситуацию» в мире. Поэтому все импортируемые и производимые пищевые продукты в нашей стране подвергаются анализу на содержание хлорорганических соединений.
ДДТ — 4,4′-дихлордифенилтрихлорметилметан. Это белый кристаллический порошок, малорастворим в воде, растворим в органических растворителях. Токсическое воздействие ДДТ выражается в быстрой усталости, головных болях, нарушениях сердечной деятельности, тошноте, рвоте. Отмечаются снижение в крови содержания эритроцитов и повышение содержания лейкоцитов. На кожу и слизистую оболочку глаз оказывает раздражающее действие.
Полихлоркамфен — твердое, воскообразное вещество коричневого цвета, практически нерастворимое в воде, растворимое в большинстве органических растворителей. Токсическое действие выражается подобно предыдущему препарату. Так как полихлоркамфен накапливается в фосфолипидах спинного и головного мозга, его действие более выражено на ЦНС. При попадании в организм больной ощущает сначала дискомфорт, потом действие проявляется бессистемно: может быть нарушена ориентация в пространстве, появиться нарушение памяти и т.д.
Полихлорпинен — это вязкое бесцветное вещество, практически нерастворимое в воде, хорошо растворимо в органических растворителях. Токсическое действие проявляется как раздражение кожи, отечность, изъязвления, при попадании в глаза развивается серозно-гнойный конъюнктивит. При всасывании в кровь больной теряет сознание с тонико-клоническими судорогами, может развиться отек легких. При вскрытии отмечается полнокровие внутренних органов, отек мозга.
Хлорфеноксиуксусные кислоты. Чаще всего применяют производные 2,4-Д (2,4-дихлорфенокеиуксусной кислоты), реже производные 2,4,5-Т (2,4,5-трихлорфенок- сиуксусной кислоты). Токсическое действие 2,4-Д и 2,4,5-Т на организм теплокровных животных и человека сходно по характеру. Они действуют на центральную и периферическую нервные системы, эндокринные железы. При отравлении наблюдаются повышенная саливация, раздражение слизистых оболочек глаз, дыхательных путей, диспепсические явления, судороги.
Химико-токсикологический анализ перечисленных хлорорганических соединений проводится по схемам, как указано для ГХЦГ и гептахлора, с использованием хроматографии в тонком слое сорбента, ГЖХ, для некоторых веществ — реакций окрашивания, ГХ-МС (после дериватизации), УФ-спектрофотометрии, ВЭЖХ и др.
