Химико-токсикологическое значение и анализ фосфорсодержащих пестицидов
- 11.3.1. Характеристика некоторых фосфорсодержащих пестицидов
- 11.3.2. Методы изолирования и обнаружения фосфорсодержащих пестицидов
- 11.3.3. Методы количественного определения фосфорорганических пестицидов
11.3.1 Характеристика некоторых фосфорсодержащих пестицидов
Пестициды из группы фосфорсодержащих органических соединений применяют в сельском хозяйстве в качестве инсектицидов, акарицидов, гербицидов, дефолиантов, десикантов и др. Широкое применение фосфорсодержащих органических пестицидов обусловлено тем, что многие из них, обладая высокой активностью, сравнительно быстро разлагаются в организме животных и в окружающей среде. Они не натапливаются в больших количествах в тканях животных и человека и не вызывают хронических отравлений. Однако при поступлении в организм фосфорсодержащих органических пестицидов наблюдаются тяжелые отравления.
Токсическое действие фосфорсодержащих органических пестицидов заключается в их угнетающем влиянии на ферментативные системы, прежде всего холинэстеразу. Путем фосфорилирования холинэстеразы блокируется разложение ацетилхолина, а это приводит к нарушению ряда физиологических процессов. Однако одним действием на холинэстеразу нельзя объяснить всего спектра токсического действия фосфорсодержащих пестицидов. Это подтверждается тем, что, исключив действие некоторых пестицидов на холинэстеразу, наблюдают токсическое действие этих препаратов на организм.
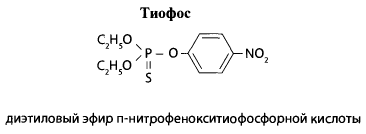
Тиофос представляет собой маслянистую жидкость со слабым запахом чеснока, при температуре 6,1°С затвердевает. Тиофос малорастворим в воде, но хорошо растворяется в органических растворителях. Промышленностью выпускается в виде концентрата эмульсии 30%, из которого готовят 0,03-0,05% водные разведения и используют как инсектицид.
При легкой форме отравления тиофосом наблюдается общая слабость, головокружение, вялая реакция зрачков. При отравлении средней тяжести — головокружение, беспокойство, рвота, понос, маскообразное лицо, дрожание рук, головы, понижение сухожильных рефлексов. При тяжелых формах возникают клонико-тонические судороги, кома с глубокой потерей сознания, отек легких.
В организме у тиофоса отщепляется сера, и образуется более ядовитое соединение — параоксон (летальный синтез).
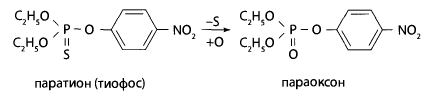
При вскрытии трупов обычно наблюдают отек легких, головного мозга, полнокровие внутренних органов.
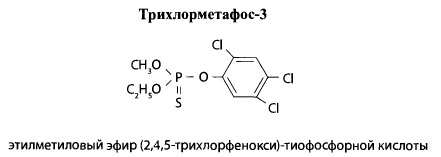
Трихлорметафос-3 представляет собой бесцветную или маслянистую желтоватую жидкость со слабым неприятным запахом. Вещество малорастворимо в воде, хорошо растворимо в большинстве органических растворителей. Препарат выпускают в виде 50% концентрата-эмульсии. Применяют после разведения минеральным маслом в качестве контактного инсектицида и акарицида в борьбе с комнатными мухами, их личинками, клопами, вредителями сахарной свеклы, виноградников и других культур.
Токсичность трихлорметафоса-3 значительно ниже, чем тиофоса. Токсическое действие проявляется в виде раздражения кожи и слизистой оболочки глаз, нарушении обменных процессов, понижении кровяного давления, снижении активности холинэстеразы.
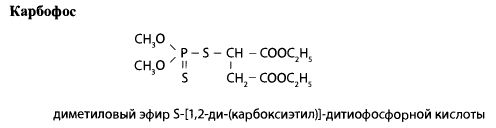
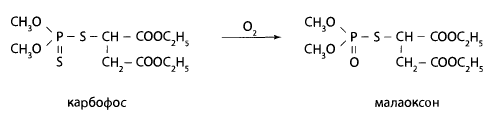
Карбофос — это бесцветная маслянистая жидкость с характерным неприятным запахом, мало растворяется в воде и предельных углеводородах. Растворяется в большинстве органических растворителей. Карбофос выпускается в виде 30-60% концентрата- эмульсии, которая после разведения применяется в качестве контактного инсектицида и акарицида в борьбе с тлями, клещами на плодовых и полевых культурах.
Токсическое действие карбофоса по сравнению с тиофосом менее выражено и развивается медленнее. Основные симптомы отравления: слюнотечение, рвота, понос, одышка, цианоз, клонические судороги.
В организме карбофос подвергается окислению с образованием малаоксона, который обладает выраженной антихолинэстеразной активностью.
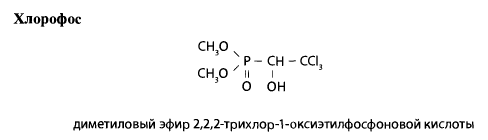
Хлорофос — это белый кристаллический порошок, растворим в воде, бензоле, хлороформе и других органических растворителях. Он малорастворим в предельных углеводородах. Хлорофос выпускается в виде порошка, содержащего 80% основного вещества. В виде 0,1-0,3% водного раствора применяется как контактный и кишечный инсектицид для обработки садов, виноградников, зерновых, бахчевых и других культур. В быту применяются 0,3% растворы для борьбы с мухами, обработки жилых помещений.
Токсическое воздействие на человека ниже по сравнению с тиофосом и проявляется в раздражающем действии на кожу и слизистые оболочки глаз, понижении активности холинэстеразы в крови. При хронических отравлениях наблюдаются нарушения функции печени и сердечно-сосудистой системы.
В организме продуктом разложения хлорофоса является дихлофос (ДДВФ — диметиловый эфир 2,2-дихлорвинилфосфорной кислоты), который обладает более выраженным холинэстеразным эффектом.
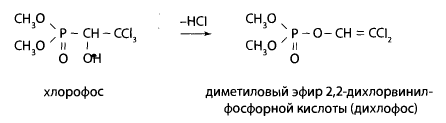
При гидролизе ДДВФ образуется диметилфосфорная кислота и дихлорвиниловый алкоголь, который окисляется в дихлоруксусный альдегид.
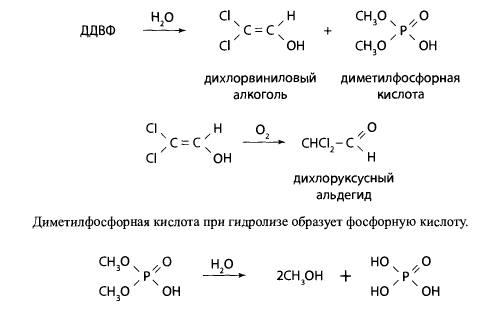
11.3.2 Методы изолирования и обнаружения фосфорсодержащих пестицидов
Из биологических объектов тиофос, трихлорметафос-3, карбофос извлекают органическими растворителями. Для очистки полученных извлечений используют методы: вымораживание липидов при низких температурах, реэкстракцию, иногда рекомендуется колоночная хроматография.
Карбофос, трихлорметафос-3, тиофос. К 100 г измельченного биологического материала добавляют воду до кашицы, 100 мл хлороформа (или бензола) и смесь оставляют на 4 ч при периодическом перемешивании. Затем органический растворитель сливают и настаивают объект с растворителем еще 2 раза (по 50 мл) в течение 2 ч при взбалтывании. Экстракты объединяют, фильтруют и выпаривают досуха. Остаток растворяют в 10 мл хлороформа и исследуют.
Для извлечения трихлорметафоса-3 используют также ацетон, хлороформ или их смесь.
Хлорофос. 100 г измельченного биологического материала заливают 150 мл воды очищенной, подкисляют серной кислотой до рН=2-2,5 и оставляют на 2 ч. Затем извлечение процеживают через марлю. К объекту еще 2 раза добавляют воду очищенную (каждый раз по 75 мл) и настаивают по часу. Полученные извлечения объединяют, центрифугируют и экстрагируют 30 мл хлороформа 4 раза. Хлороформные экстракты объединяют, выпаривают до сухого остатка, который растворяют в 5 мл воды очищенной, раствор фильтруют и анализируют.
Предварительное исследование на фосфорорганические пестициды
Холинэстеразная проба. В основе реакции — способность фосфорсодержащих органических соединений снижать активность ацетилхолинэстеразы. Она является общей для фосфорорганических ядохимикатов.
Ацетилхолин (гидроксид (2-ацетоксиэтил) триметиламмония) в присутствии ацетилхолинэстеразы способен разлагаться с образованием уксусной кислоты. Этот процесс можно зафиксировать, если к смеси добавить индикатор бромфеноловый синий.
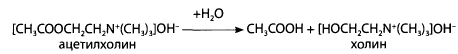
При появлении в растворе уксусной кислоты окраска индикатора меняется от синей до желтой. Если в растворе присутствует фосфорорганическое соединение, являющееся ингибитором ацетилхолинэстеразы, то разложение ацетилхолина до уксусной кислоты не происходит и окраска бромтимолового синего не меняется.
Для проведения испытания в фарфоровую чашку вносят индикатор, каплю исследуемого раствора (извлечения из объекта) и каплю раствора холинэстеразы (или плазмы крови, содержащей этот фермент). Через 10 мин добавляют каплю раствора ацетилхолина. Если окраска раствора меняется на желтую, делают вывод о необнаружении в объекте фосфорорганических ядохимикатов.
Пробе придается судебно-химическое значение при отрицательном результате из-за ее не- специфичности, так как некоторые другие соединения (например, севин, эзерин) могут также подавлять активность ацетилхолинэстеразы, хотя и не содержат в своей молекуле фосфор.
Обнаружение фосфора. В тигель вносят 0,2-0,3 г смеси из 2 частей безводного карбоната натрия и 5 частей пероксида натрия. К полученной смеси добавляют несколько капель полученного извлечения из объекта. Тигель осторожно нагревают до выпаривания жидкости. Затем усиливают нагревание до расплавления смеси. После охлаждения остаток переносят в фарфоровую чашку, добавляют немного карбоната натрия и 10 мл воды, растирают, фильтруют. В полученном растворе могут быть фосфаты, сульфаты, галогениды, арсенаты. Обнаружению фосфора мешают арсенаты. Чтобы их удалить, добавляют хлороводородную кислоту до рН=0,5 и пропускают сероводород. При наличии арсенатов выпадает осадок сульфида мышьяка. Осадок отфильтровывают и в фильтрате обнаруживают фосфат-ионы.
В пробирку вносят 3-5 капель фильтрата (свободного от арсенатов), добавляют 5 капель молибдата аммония и 10% азотную кислоту. При наличии фосфатов появляется желтая окраска. К полученному раствору добавляют 3-5 капель насыщенного водного раствора гидрохлорида бензидина и 10% раствор аммиака до щелочной реакции (по лакмусу). При наличии фосфат-ионов появляется синяя окраска.
При получении положительных результатов предварительных реакций проводят исследование на индивидуальные вещества из группы фосфорсодержащих пестицидов.
Обнаружение тиофоса
Реакция с о-анизидином. К 1 мл хлороформного раствора остатка прибавляют 0,5 мл раствора о-анизидина и 2 мл раствора пербората натрия (NaB03-4H20). Через 5-30 мин появляется окрашивание от желтого до красноватого цвета в зависимости от количеств тиофоса.
Метод ТСХ. На хроматографическую пластинку со слоем силикагеля, закрепленного крахмалом, наносят 2 капли хлороформного раствора остатка. Рядом наносят хлороформный раствор «стандарта». Пластинку помещают в систему растворителей н-гексан — хлороформ (1:2). После хроматографирования пластинку подсушивают и опрыскивают смесью растворов бромфенолового синего и нитрата серебра. Затем пластинку вносят в сушильный шкаф и выдерживают при температуре 60°С в течение 20 мин. После охлаждения пластинку обрабатывают раствором лимонной кислоты. Тиофос и «стандарт» проявляются в виде красных пятен на желтом фоне.
Реакция щелочного гидролиза. К сухому остатку прибавляют 4-5 мл пероксида водорода и нагревают на водяной бане до обесцвечивания жидкости. После охлаждения вносят в раствор 2 мл 20% раствора гидроксида натрия и нагревают на водяной бане 20 мин. Появляется желтое окрашивание.
Обнаружение трихлормет афоса-3
На хроматографическую пластинку с нанесенным слоем силикагеля, закрепленного крахмалом, наносят 3 капли хлороформного извлечения и параллельно раствор «стандарта». Пластинку помещают в систему растворителей н-гексан — ацетон (2:1). После хроматографирования и высушивания пластинки на воздухе ее обрабатывают щелочным раствором о-толидина и облучают УФ-светом в течение 3-5 мин. Трихлорметафос-3 и «стандарт» проявляются в виде желтых пятен.
Обнаружение карбофоса
Реакция с диазотированной сульфаниловой кислотой. Несколько миллилитров хлороформного раствора остатка выпаривают досуха. К сухому остатку прибавляют 2 мл воды очищенной, 1 мл раствора диазотированной сульфаниловой кислоты и 0,5 мл 5% раствора гидроксида натрия — появляется вишнево-красное окрашивание.
Реакция с реактивом Марки. Несколько миллилитров хлороформной вытяжки выпаривают досуха. К остатку добавляют 5-10 капель реактива Марки — появляется оранжевая окраска, переходящая в желто-коричневую.
Реакция с сульфатом меди(П). К сухому остатку после испарения экстракта из объекта прибавляют 1 мл 10% спиртового раствора гидроксида натрия и нагревают на кипящей водяной бане 10 мин. После охлаждения pH раствора доводят до 4-5 с помощью 25% серной кислоты, прибавляют 1 мл хлороформа и 2 капли 10% раствора сульфата меди(П). При наличии карбофоса слой хлороформа окрашивается в зеленовато-желтый цвет.
Микрокристаллоскопические реакции. Для проведения этих реакций спиртовый раствор остатка, содержащего карбофос, помещают в углубление на предметном стекле и к нему добавляют один из нижеперечисленных реактивов, закрывают покровным стеклом и помещают во влажную камеру. Карбофос с хлоридом ртути(П) образует желтоватые кристаллы в форме зведочек; с йодидом висмута — темно-красные кристаллы в форме игл; с хлористым йодом — бурые кристаллы, которые исчезают через некоторое время.
Метод ТСХ. На хроматографическую пластинку со слоем силикагеля, закрепленного гипсом, наносят несколько капель раствора остатка. Параллельно наносят раствор «стандарта». Пластинку помещают в систему растворителей н-гексан — ацетон (2:1). После хроматографирования пластинку опрыскивают бромтимоловым синим и нитратом серебра. Затем пластинку нагревают в термостате 20 мин при 60°С. После охлаждения пластинку опрыскивают 10% раствором уксусной кислоты — появляются пятна лилового цвета при наличии карбофоса.
Обнаружение хлорофоса
Реакция с пиридином (реакция Фудживара). В пробирку вносят 1 мл исследуемого раствора, 1 мл пиридина и 1 мл 50% раствора гидроксида натрия. Смесь нагревают на кипящей водяной бане — появляется красное или розовое окрашивание. Предел обнаружения составляет 10 мкг хлорофоса в пробе. Реакция неспецифична.
Реакция с о-толидином. В пробирку вносят водный раствор исследуемого вещества,
1 мл о-толидина в ацетоне, 1 мл смеси пероксида водорода и гидроксида натрия — постепенно развивается желтое или оранжевое окрашивание. Такой же результат получается в присутствии метафоса и тиофоса.
Реакция с 2,4-динитрофенилгидразинам. В пробирку вносят 1-10 капель исследуемого раствора и 2 капли 1 М раствора гидроксида натрия. Через 20 мин добавляют 1 каплю 0,1% раствора 2,4-динитрофенилгидразина в 4 М растворе хлороводородной кислоты. Смесь нагревают на водяной бане 30 мин. После охлаждения прибавляют 1 каплю 4 M раствора гидроксида натрия и 0,5 мл этилового спирта. Появляется синее или синефиолетовое окрашивание.
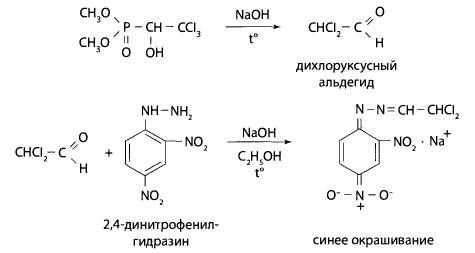
Эта реакция положительна при наличии хлорофоса и его основного метаболита — дихлоруксусного альдегида.
Реакция с ацетоном. В пробирку помещают 0,1-0,5 мл исследуемого раствора в этиловом спирте и прибавляют 1 мл ацетона и 0,5 мл 0,5 М спиртового раствора гидроксида натрия. Через 5-15 мин появляется розовая окраска, переходящая в оранжевую.
Реакция образования изонитрила. В пробирку вносят раствор исследуемого вещества в спирте, добавляют 2 мл 10% спиртового раствора гидроксида натрия и 1 каплю анилина. При нагревании ощущается характерный запах изонитрила. Реакция неспецифична.
Реакция с о-анизидином. Проводится так же, как и с тиофосом. Появляется желтое или красноватое окрашивание.
Метод ТСХ. Анализ проводят в присутствии «стандарта» на пластинке с тонким слоем силикагеля с использованием системы растворителей ацетон — гексан (1:1). После хроматографирования пластинку высушивают, обрабатывают смесью 2% раствора резорцина в 10% растворе карбоната калия, затем пластинку выдерживают 10 мин в сушильном шкафу при 100°С. Хлорофос проявляется в виде пятна оранжевого цвета.
11.3.3 Методы количественного определения фосфорорганических пестицидов
Фотоколориметрический метод. Он основан на минерализации ФОС с помощью серной и азотной кислот. Определенный объем извлечения из объекта помещают в колбу Кьельдаля, добавляют 3 мл концентрированной серной, 10 мл концентрированной азотной кислот. Смесь нагревают до просветления жидкости и появления белых паров. Минерализат охлаждают и доводят до определенного объема водой очищенной. К части раствора прибавляют молибдат аммония и бензидин. Регистрируют величину оптической плотности окрашенного раствора. Расчет содержания фосфорорганического соединения ведут по калибровочному графику.
Порядок выполнения реакций приведен ниже
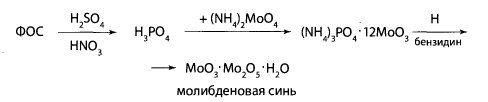
Метод газожидкостной хроматографии. Анализ проводится по высоте или площади пика. Используются термоионный, пламенно-фотометрический или электроннозахватный детекторы.
