ГЛОМЕРУЛОНЕФРИТЫ
В группе заболеваний почек и мочевыводящих путей гломерулонефриты занимают 3-4 место, уступая в распространенности только пиелонефриту и мочекаменной болезни. В настоящее время, в связи с активной антибактериальной терапией стрептококковой инфекции, снизилась частота острого гломерулонефрита, который сейчас встречается в основном только в педиатрической практике. В это же время, по данным нефрологического центра С-Петербурга, число зарегистрированных больных хроническим гломерулонефритом нарастает быстрыми темпами. Указывается на связь роста нефрологической патологии с изменениями окружающей среды, в частности, с повышением радиационного фона.
Лишь острые нефриты, сравнительно редкие в настоящее время, заканчиваются (и то не больше, чем в половине случаев) выздоровлением; хронический нефрит, особенно подострый, неуклонно прогрессирует по направлению к хронической почечной недостаточности, сопровождаясь нередко отеками (нефротический синдром) и тяжелой гипертонией, приводящими к инвалидизации еще до развития ХПН. Заболевают чаще (и болеют тяжелее) молодые, трудоспособные мужчины. Необходимо отметить, что, хотя и существуют методы, позволяющие замещать нефункционирующие почки (так называемая заместительная почечная терапия) — диализ и трансплантация, но в России они доступны далеко не всем (потребность удовлетворяется примерно на 120), очень дороги и имеют свои сложности — привязанность к аппаратам, необходимость постоянной иммуносупрессии и др. Во многих случаях в дальнейшем пациенты остаются инвалидами.
Гломерулонефриты – группа иммунных заболеваний почек, характеризующихся первичным поражением клубочков и последующим вовлечением в патологический процесс интерстиция с тенденцией к прогрессированию, переходом в нефросклероз и развитием синдрома хронической почечной недостаточности. Впервые заболевание описано английским врачом Р. Брайтом в 1827, и длительное время все нефриты назывались «болезнью Брайта», в начале 20-го века появилась первая классификация Ф.Фольгарта и Т. Фара, разделившая гломерулонефриты по течению заболевания. Однако только с 1951 г., когда была разработана техника биопсии почек, начался активный этап изучения этой патологии.
Этиология более чем в половине случаев этиология хронических гломерулонефритов остается неизвестной. В отношении острого гломерунефрита установлен возбудитель – стрептококки группы А штаммов 1,3,4,12 и 49. Наиболее велика роль штамма 12. Кроме того, в качестве этиологических факторов рассматриваются стафилококки, энтерококк, диплококки, бледная трепонема, цитомегаловирус, вирусы простого герпеса, гепатита В, Эпштейн-Бар, шистосома, малярийный плазмодий, токсоплазмы, лекарственные препараты, вакцины, яды.
Патогенез
В настоящее время в развитии и прогрессировании хронического гломерулонефрита придают значение трем основным механизмам иммунным, гемодинамическим и метаболическим. Однако в развитии гломерулонефрита наибольшее значение имеет первый из этих факторов. Только в 50-60 гг. появились сообщения об обнаружении иммунных комплексов в клубочке и периферической крови. Развивая эту концепцию, в дальнейшем была разработана теория об иммунокомплексном гломерулонефрите. Однако в 1981 г. J. Hamburger высказал предположение о том, что «иммунокомплексный» и «антительный» механизмы развития хронического гломерулонефрита не могут объяснить разнообразие клинических, морфологических и иммунологических проявлений хронического гломерулонефрита. Это привело к тому, что вопрос о патогенезе гломерулонефритов остается открытым. В соответствии с данными литературы, механизм развития гломерулярной патологии, прежде всего, должен рассматриваться как следствие генетической неполноценности Т-клеточного звена иммунитета, что в конечном итоге приводит к нарушению процессов репарации отдельных частей нефрона с дальнейшим изменением их антигенной структуры и образованием иммунных комплексов. Последние локализуются на пораженных участках базальной мембраны с последующим их фагоцитозом подоцитами, нейтрофилами, мезангиальными клетками и макрофагами. При разрушении некоторых из этих клеток выделяются лизосомальные ферменты, в результате чего базальная мембрана повреждается еще больше. К этому предрасполагает низкое содержание Т-лимфоцитов, что делает процесс необратимым.
Иммунные механизмы развития хронического гломерулонефрита (по Рябову С.И. 2000)

Иммунные механизмы развития острого пролиферативного гломерулонефрита (по Рябову С.И. 2000 г).
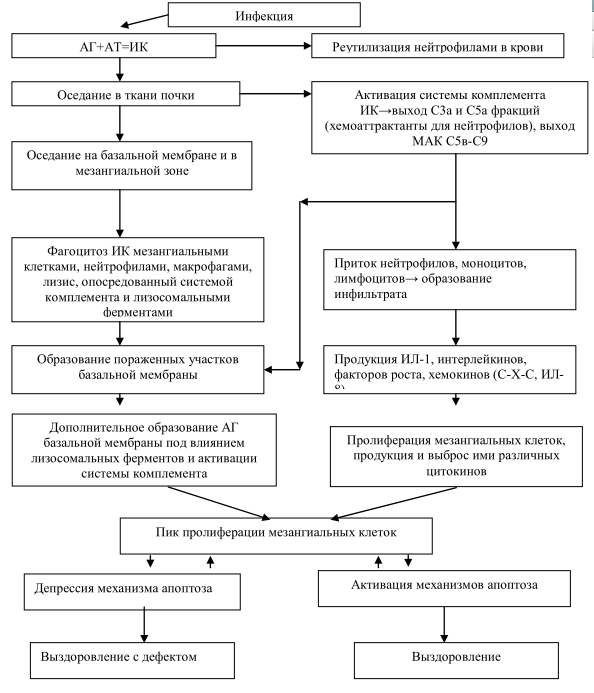
Примечание: АГ – антиген, АТ – антитело, ИК – иммунный комплекс Патогенез острого гломерулонефрита заключается в том, что при развитии стрептококковой инфекции и попадании экзогенного антигена в организм, антителообразующие клетки в увеличенном количестве начинают продуцировать антитела для связывания с антигеном и формирования иммунного комплекса. Часть этих комплексов реутилизируется непосредственно клетками гранулоцитарного ряда в периферическом русле, оставшаяся часть попадает в ткань клубочка и откладывается там. Далее наблюдается активация системы комплемента, что в свою очередь привлекает в зону клубочка нейтрофилы. Нейтрофилы при фагоцитозе иммунных комплексов в зоне базальной мембраны выбрасывают лизосомальные ферменты, тем самым повреждая эти участки мембраны. Помимо нейтрофилов в гломерулярную зону приходит большое количество моноцитов. Моноциты появляются в ткани раньше других клеток, образуют моноцитаный инфильтрат, который участвует в продукции ИЛ-1бета, последний запускает пролиферацию мезангиальных клеток, вследствие чего развивается состояние патологической пролиферации гломерулярных клеток. В дальнейшем большое внимание уделяется механизму апоптоза. На высоте пролиферации гломерулярных клеток, а также нейтрофилов, моноцитов и пришедших Т-лимфоцитов активный апоптоз быстро восстанавливает и очищает структуру клубочка.
Классификация
По нозологическому принципу: первичный (идиопатический) гломерулонефрит (ГН) – 85%, этиология неизвестна; вторичный – 15% (при системных заболеваниях, заболеваниях печени, лекарственный и др.).
По течению:
- острый (потенциально с исходом в выздоровление);
- подострый (с бурным, часто злокачественным течением и развитием ОПН);
- хронический (с прогрессирующим течением и исходом в ХПН).
По морфологическому принципу:
- Пролиферативные
- Диффузный пролиферативный эндокапилярный (острый инфекционный) Экстракапилярный (диффузный с полулуниями, быстропрогрессирующий)
- Мембранозно-пролиферативный
- Мезангиально-пролиферативный (Ig нефропатия, болезнь Берже)
- С минимальными изменениями
- Мембранозный
- Фокально-сегментарный гломерулосклероз
- Склерозирующий (фибропластический)
По активности: ремиссия; активная стадия (увеличение в 5-10 раз гематурии, протеинурии, нарастание АД и отеков, появление нефротического синдрома или острой почечной недостаточности).
Морфологическая картина.
Основным критерием диагностики гломерулонефритов является морфологическая картина, так она индивидуальна для каждого типа ГН.
Острый гломерулонефрит

Быстропрогрессирующий гломерулонефрит
Мембранозный гломерулонефрит

Острый гломерулонефрит – морфология характеризуется поражением 80-100% клубочков с резкой пролиферацией мезангиальных клеток. В начальной (острой) стадии клубочки обычно увеличены в размерах, отмечается увеличение клеточности. Выявляется усиленная пролиферация эндотелиальных клеток капилляров, а также мезангиальных клеток. Мезангий инфильтрирован нейтрофилами и моноцитами. В острейшей стадии может определяться геморрагический экссудат. После экссудативной фазы развивается экссудативно-пролиферативная, а затем и пролиферативная. Просвет капилляров при этом сужается. Пролиферативные и экссудативные проявления обычно начинают разрешаться через 1-2 мес. от начала заболевания, хотя полное морфологическое восстановление затягивается на несколько месяцев.
При электронно-микроскопическом исследовании наиболее типичным является выявление «горбов» на эпителиальной стороне базальной мембраны капилляров клубочка. Они соответствуют отложению иммунных комплексов, обычно эти изменения выявляются в течение первых 6 нед. заболевания. В целом, морфологическая картина при остром процессе оценивается как эндокапилярный диффузный пролиферативный гломерулонефрит, при котором прослеживается несколько стадий — экссудативная, экссудативно-пролиферативная, полиферативная и, наконец, стадия остаточных явлений, которые могут сохраняться несколько лет.
Быстропрогрессирующий гломерулонефрит – это экстракапиллярный диффузный гломерулонефрит, при этом полулуния выявляются не менее чем в 50-60% клубочков. Полулуния располагаются вне клубочка, занимая часть пространства боуменовой капсулы. По клеточному составу полулуния состоят из пролиферирующих клеток капсулы, моноцитов и лимфоцитов. Полулуния сдавливают капиллярные петли и начальную часть проксимального отдела петли Генле. По мере прогрессирования заболевания доля фибрина в полулуниях возрастает, что, в конечном счете, приводит к запустеванию клубочка, в результате появляются некрозы петель и дефекты в стенках капилляра. В конечной стадии это приводит к появлению пролиферации мезангиальных клеток и инфильтратов, расположенных перигломерулярно и в интерстиции.
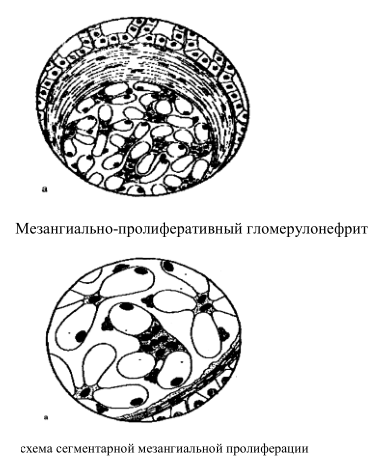
Мезангиально-пролиферативный гломерулонефрит – при световой микроскопии выделяют диффузный и очаговый мезангиально-пролиферативный гломерулонефрит. В первом случае выявляется диффузная пролиферация мезангиальных клеток и увеличение мезангиального матрикса. Базальная мембрана остается тонкой. Одновременно почти у половины больных выявляется глобальный и сегментарный склероз почти трети клубочков, что приводит к нефронному запустеванию. При прогрессировании болезни этот процесс нарастает. Одновременно выявляется пролиферация клеток капсулы Боумена. Почти у всех больных отмечается сращение петель клубочка с капсулой и ее утолщение. Нарастание указанных изменений сопровождается прогрессированием клинических симптомов, в частности, повышением АД, а затем и снижением почечных функций, что свидетельствует о появлении глобального гиалиноза клубочков. Наряду с этим наблюдается сначала очаговая, а затем и более распространенная дистрофия, субатрофия и атрофия проксимальных канальцев. Иммунофлюоресцентная микроскопия позволяет выявить два варианта – иммунопозитивный и иммунонегативный. В первом случае выявляется отложение различных иммуноглобулинов (прежде всего G,A,M), во втором – никаких отложений обнаружить не удается. Электронная микроскопия позволяет подтвердить диагноз при обнаружении мезангиальных клеток и мезангиального матрикса. Очаговый мезангиально-пролиферативный гломерулонефрит характеризуется очаговой и сегментарной пролиферацией мезангиальных клеток.
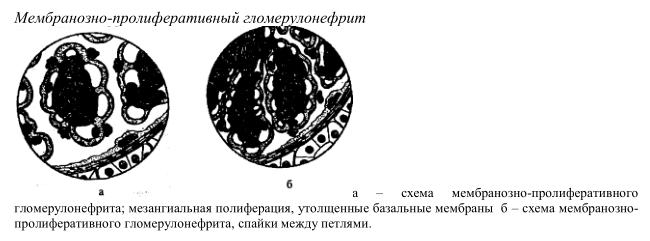
Мембранозно – пролиферативный гломерулонефрит. Для больных этой группы характерны поражения клубочков с изменением мезангиального матрикса, отложением фибрина, комплемента и иммуноглобулинов в мезангии, и вторичное изменение базальной мембраны. При отложении депозитов субэндотелиально выделяют I тип болезни. В случае отложения депозитов внутри базальной мембраны выделяют II тип болезни (болезнь плотных депозитов). Наконец, если число депозитов велико, и они соприкасаются с субэндотелиальными депозитами, принято выделять III тип. Плотная пластинка базальной мембраны при этом расслаивается и разрушается. При световой микроскопии диффузная пролиферация мезангиальных клеток сопровождается увеличением мезангиального матрикса. У большинства больных выявляется раздвоение и утолщение капиллярных петель клубочков, обнаруживается понефронное запустевание, а также интерстициальный склероз. У части больных выявляется значительное увеличение мезангиального матрикса в центре долек, что приводит к увеличению объема мезангиальной области. Капиллярные петли клубочков, располагаясь по периферии этих разрастаний, оказываются сдавленными.
Мембранозный гломерулонефрит. Для этой формы гломерулонефрита основным признаком является изменение базальной мембраны, а также наличие субэпителиальных депозитов, соответствующих отложению иммуноглобулинов. При световой микроскопии основным характерным проявлением является изменение базальной мембраны, практически во всех клубочках. В зависимости от выраженности этих изменений различают 4 стадии. Для 1 стадии характерно некоторое уплотнение с редко встречающимися утолщениями базальных мембран. Изредка выявляются единичные субэпителиальные депозиты. Для 2 стадии субэпителиальные депозиты располагаются более часто, напоминая картину «зубцов гребенки». 3 стадии по выраженности изменений со стороны базальной мембраны является как бы промежуточной между 2-й и 4-й стадиями, так как имеет черты одной и другой. 4 стадия характеризуется резким изменением базальной мембраны, отдельные участки ее утолщаются, сменяясь местами с истончением. Выступающие на эпителиальной стороне шипики («зубцы гребенки») как бы сливаются между собой. Базальная мембрана при этом может резко утолщаться, вызывая склероз клубочков.
Гломерулонефрит с минимальными изменениями. Изменения со стороны клубочков незначительные. При световой микроскопии различают пять возможных вариантов изменений отсутствие каких-либо изменений со стороны клубочков, хотя может отмечаться повышение содержания белковых и липидных капель; выявляется очаговое запустевание клубочков; минимальное расширение мезангиального матрикса без изменений числа клеток в клубочке; очаговые изменения канальцев, которые могут быть даже атрофированы; минимальная гиперклеточность мезангиума, при этом число мезангиальных клеток не должно превышать 3 на одну мезангиальную область. При электронной микроскопии выявляется «исчезновение» ножковых отростков подоцитов. Ножковые отростки подоцитов выглядят набухшими, в результате происходит закрытие щелевидных пространств.
Фокально-сегментарный гломерулосклероз. Световая микроскопия выявляет отложения гиалиновых масс с развитием склероза юкстагломерулярной зоны. При этом изменения могут выявляться не во всех клубочках и сегментарно, так как в процесс вовлекаются не все капилляры клубочков. В результате отмечается сегментарный гиалиноз одной или нескольких долек клубочка. В более поздних стадиях процесса гиалиновые массы заменяются в связи с прогрессирование склеротических изменений. В результате клубочки запустевают. Электронная микроскопия выявляет исчезновение ножковых отростков подоцитов, что связано с их набуханием и сокращением. В результате щелевидные пространства закрываются. Подоциты обычно увеличены в размерах, содержат много органелл.
Клиническая картина
Клинические проявления включают три основных синдрома мочевой, отечный и гипертензионный. Нередко заболевание начинается с острого нефритического синдрома. Изменения со стороны мочи наиболее типичны и выявляются стабильно. У подавляющего большинства больных эти изменения характеризуются преходящей (чаще стабильной) протеинурией, эритроцитурией, цилиндрурией. Важно указать на необходимость определения протеинурии не только в разовых порциях мочи, но и в суточной, так как этот показатель лучше отражает величину потери белка. Острый нефритический синдром о.начало — олигурия + изменения в моче + повышение АД + отеки + +транзиторная азотемия При некоторых формах гломерулонефрита (или в определенных стадиях его течения) развивается нефротический синдром, который в этом случае называется первичным, в отличие от вторичного, развивающегося при некоторых инфекциях, тромбозе почечных сосудов, воздействии некоторых лекарств. Составляющие нефротического синдрома массивная протеинурия (3,0 гсут), гипоальбуминемия (30 гл), отеки, гиперлипидемия. Наиболее частые причины вторичного нефротического синдрома диабетическая нефропатия, амилоидоз, ВИЧ-инфекция, злокачественные опухоли (лимфопролиферативные, молочных желез, легких, желудка и толстой кишки), лекарственные препараты (золото, пеницилламин, НПВП).
Патогенез нефротических отеков:
1) гипотеза «недополнения» массивная протеинурия→гипоальбуминемия→уменьшение внутрикапиллярного онкотического давления→переход жидкости в интерстициальное пространство→снижение ОЦК→Активация РААС
2) гипотенза «переполнения» нарушение экскреции натрия.
В настоящее время установлена значимость вариантов течения процесса для исходов заболевания. Три типа течения редкие обострения (не чаще 1 раза в 8 лет), умеренно частые (каждые 4-7 лет), частые обострения (1 раз в 1-3 года) или непрерывное рецидивирование (неполное исчезновение признаков обострения под влиянием терапии на 1-2 года или постоянное их сохранение на протяжении всего известного периода болезни). Критериями обострения для больных с изолированным мочевым синдромом являются увеличение протеинурии и эритроцитурии в 8-10 раз в разовых анализах мочи, тогда как суточная потеря белка увеличивается не менее чем на 1 г. Для больных с экстраренальными проявлениями болезни критериями обострения являются появление нефротического синдрома, резкое и стойкое повышение артериального давления; нарастание протеинурии и эритроцитурии в разовых анализах мочи более чем в 10 раз. Признаками прекращения обострения является исчезновение нефротического синдрома, нормализация или снижение до обычных цифр артериального давления, возвращение к обычным величинам протеинурии и эритроцитурии. В настоящее время различают полную и неполную ремиссии. О полной ремиссии можно говорить в случае регрессии нефротического синдрома и снижении суточной протеинурии до 0,3 г, тогда как эритроцитурия уменьшается в 8-10 раз (в разовых порциях мочи). В диагнозе должна быть указана морфологическая форма гломерулонефрита, клинические проявления на момент обследования, тип течения (оценивается по совокупности за несколько последних лет) и функциональное состояние почек.
Примерная формулировка диагноза:
Мезангиально-пролиферативный гломерулонефрит с изолированным мочевым синдромом иммунопозитивный с отложением иммуноглобулинов G, I тип течения, в стадии обострения, без нарушения функции почек.
Осложнения хронического гломерулонефрита: острая почечная недостаточность, хроническая почечная недостаточность, энцефалопатия (эклампсия) – возможна у пациентов с острым гломерулонефритом.
Отдельные варианты гломерулонефритов
Острый гломерунефрит
Острый диффузно-пролиферативный гломерулонефрит – заболевание, возникающее после инфекции (чаще всего, кокковой природы), приводящее к иммуновоспалительному поражению клубочков, характеризующееся пролиферативно- экссудативными проявлениями. Большинство исследователей выявили более частное развитие заболевания в климатических зонах с повышенной влажностью воздуха. Острый гломерулонефрит – заболевание, характерное для лиц молодого возраста. В этиологии ведущую роль играют стрептококки группы А штаммов 1,3,4,12 и 49. Особенно велика роль штамма 12. Ревматизм вызывается другими штаммами стрептококков. В результате острый гломерулонефрит с поражением суставов практически никогда не сочетается. Инкубационный период составляет 1-3 недели. Можно выделить 3 основных варианта болезни гломерунефрит, проявляющийся только изменениями мочи; форма, когда отмечается сочетание всех трех основных симптомов (развернутая форма болезни) – мочевой синдром, отеки и гипертония; случаи, когда сразу диагностируется нефротический синдром. Боли в поясничной области выявляются у 50-70% всех больных. Кроме того, больные отмечают снижение работоспособности, головную боль, связанную с повышением АД, дизурию, жажду, снижение суточного диуреза. При объективном обследовании больных с заболеваниями почек, прежде всего, обращается внимание на наличие отеков. Они локализуются чаще на лице, чаще под глазами и более выражены по утрам, кроме того, есть отеки в поясничной области и на ногах. Повышение АД в настоящее время выявляется только у 53% больных. При этом надо отметить, что у подавляющего числа больных гипертензия выражена умеренно. Стадия развернутой клинической картины характеризуется наличием всех или нескольких симптомов. Изменения мочи являются обязательными. Моносимптомная форма заболевания характеризуется более спокойным течением и благоприятным прогнозом. Длительность существования отдельных симптомов варьирует. Первоначально исчезают общие жалобы на слабость, разбитость, головную боль. Из объективных признаков, прежде всего, ликвидируются отеки, которые сохраняются менее 2 нед. у 13 заболевших. Значительно дольше обнаруживается повышенное АД. Дольше всего обнаруживаются изменения в моче. Обычно допускается наличие патологических изменений в моче в течение года со дня заболевания. На прогноз при остром гломерулонефрите влияют следующие факторы возраст больного, сроки госпитализации, длительность существования и выраженность экстраренальных симптомов, осложнения со стороны сердечно-сосудистой системы, наличие эклампсии, анурия, морфологический вариант гломерулонефрита. Полное выздоровление наступает в 40-90% случаев (чаще у детей), кроме того, возможно выздоровление с «дефектом» (сохраняющаяся несколько месяцев преходящая умеренная протеинурия или эритроцитурия). Летальные исходы в настоящее время встречаются редко.
Экстракапиллярный диффузный пролиферативный гломерулонефрит (злокачественный, быстропрогрессирующий, диффузный серповидный, подострый) Клиническая картина достаточно яркая. В большинстве случаев заболевание начинается остро с острого нефритического синдрома. Приблизительно у половины больных выявляется олигоурия. Бурно и рано развивается нефротический синдром появляются отеки, которые быстро прогрессируют. Прибавка массы тела уже в первую неделю заболевания составляет 6-10 кг. Часто уже через 1-2 нед. от начала заболевания обнаруживается асцит, несколько позднее может присоединиться выпот в плевральной полости иили перикарде. С первых дней болезни у большинства больных повышается АД, иногда гипертония приобретает злокачественное течение. Течение заболевания неблагоприятное. У большинства больных быстро прогрессируют симптомы почечной недостаточности. У лиц с преимущественным преобладанием АГ 50% уровень выживаемости равен 1,7 мес, а при нефротическом синдроме 10 мес.
Мезангиально-пролиферативный гломерулонефрит. Чаще заболевают мужчины. В большинстве случаев заболевание протекает малосимптомно. Обострения процесса встречаются относительно редко. Клиническая картина достаточно скудна. Наиболее характерным является умеренно выраженная АГ и мочевой синдром. При болезни Берже, как варианте мезангиально-пролиферативного гломерулонефрита, наиболее выраженным симптомом является макрогематурия у детей.
Мембранозно-пролиферативный гломерулонефрит. Чаще выявляется в молодом возрасте и у женщин. Клиническая картина неоднородна. Больные отмечают преходящую макрогематурию, которая у 15 больных является первым признаком заболевания. Более половины пациентов указывают на отеки, ноющие боли в поясничной области, дизурию, АГ у примерно 44% больных. Прогноз обычно неблагоприятный и ХПН развивается в первые 5 лет течения болезни.
Мембранозный гломерулонефрит. Среди заболевших преобладают мужчины, в основном зрелого возраста. Клиническая картина характеризуется медленным постепенным началом и частым развитием самопроизвольных ремиссий. Первым клиническим проявлением обычно бывают отеки. Кроме того, часто – преходящая протеинурия. У 13 больных первым признаком болезни бывает АГ. Заболевание характеризуется относительно медленным течением. Через 5 лет умирает чуть больше 10% больных. У отдельных пациентов возможны спонтанные ремиссии продолжительностью 5 лет.
Гломерулонефрит с минимальными изменениями (липоидный некроз). Иногда заболевание называют «болезнью малых отростков подоцитов». Заболевание развивается у детей, связано с вакцинацией и банальными респираторными заболеваниями. Клиническая картина сводится к наличию типичного нефротического синдрома, который развивается остро и протекает бурно. Иногда самопроизвольно без всякого лечения отеки исчезают самопроизвольно. Иногда бывает преходящее повышение АД. Выживаемость при лечении антибиотиками и стероидами высокая.
Фокально-сегментарный гломерулосклероз. Встречается редко, у лиц молодого возраста, мужского пола. Клиническая картина достаточно выражена и определяется обычно двумя синдромами – нефротическим и гипертензионным (высокие цифры АД, систолическое АД может превышать 200 мм.рт.ст.). Обычно характерно быстро прогрессирущее течение, приводящее к развитию ПН. Характерно, что пересадка почки при данной форме гломерулонефрита часто сопровождается развитием заболевания в трансплантате.
Методы обследования: диагностика мочевого синдрома в общем анализе мочи протеинурия, гематурия (микро и макро «цвета мясных помоев»), цилиндрурия, иногда лейкоцитурия.
Диагностика нефротического синдрома – суточная потеря белка более 3 гсутки, гипопротеинемия (общий белок менее 60 гл, альбумин менее 40 гл), гиперлипидемия и гиперхолестеринемия. Оценка функционального состояния почек (выявление ХПН) — проба Зимницкого при ухудшении функции уменьшение относительной плотности мочи (1012), проба Реберга — снижение клубочковой фильтрации (менее 80 млмин), креатинин, мочевина крови нормальные или увеличенные, электролиты крови тенденция к снижению Na, Ca, увеличению K, P, Mg; КОС — развитие метаболического ацидоза (гломерулярного и канальцевого). Инструментальные методы обследования: внутривенная урография – исключение врожденной и урологической патологии; ультразвуковое исследование – исключение полостных и объемных образований; ренография – общая оценка функционального состояния почек; пункционная биопсия с использованием световой микроскопии (гемотоксилин-эозин, ШИКPAS, серебрение по Джонсу и другие — Masson, конго-рот и т.д.), электронной микроскопией (позволяет точно определить расположение депозитов, обнаружить мелкие депозиты, выявить повреждение структуры мембран, клеток), иммунофлюоресцентным исследованием (используют обработанные флюоресценном АТ к Ig, компонентам С, альбумину, фибрину, каппа и лямбда-легким цепям Ig. При наличии соответствующих АГ – свечение, которое м.б. линейное, гранулярное). Биопсия – основной метод морфологической диагностики гломерулонефрита.
Дифференциальный диагноз при проведении дифференциального диагноза необходимо учитывать мочевой, отечный, гипертензионный синдром. Дифференциальный диагноз поводится с другими заболеваниями почек (тубулоинтерстициальные заболевания почек, туберкулез, гипернефрома, вторичные нефропатии, вторичные гломерулопатии), при наличии нефротического синдрома – с амилоидозом, тромбозом почечных вен, артериальная гипертензия – с гипертонической болезнью и вазоренальной артериальной гипертензией.
Лечение больного с хроническим гломерулонефритом Режим – ограничение только в период обострения процесса или развития хронической почечной недостаточности. Диета – ограничение белка при развитии ХПН (диета 7, 7а и 7б). При синдроме артериальной гипертензии – ограничение соли и воды, при гиперкалиемии — досаливание пищи.
Терапия патогенетическая, симптоматическая и заместительная.
Патогенетическая: глюкокортикоиды – постоянная терапия пероральный прием преднизолона 1-2 мгкгсутки не менее 2 мес., с последующим постепенным снижением дозы до 10-20 мгсутки в течение 2 и более мес.; альтернативный прием удвоенной дозы через 1 день; пульс-терапия 0,5-1,0 г метилпреднизолона в течение 20-40 мин через 1 день (суммарно 3-4 г) Цитостатики — как правило, используют алкилирующие соединения — циклофосфамид (в дозе 1,5—2 мгкг в день) и хлорбутин (в дозе 0,1—0,2 мгкг в день); антиметаболит азатиоприн менее эффективен, хотя и менее токсичен. Снижение числа лейкоцитов происходит в течение нескольких дней или недель. В этот период важно проверять число лейкоцитов в периферической крови каждые 2—3 дня, с тем, чтобы при их снижении до нижнего допустимого уровня доза препарата могла быть снижена или отменена.
Самыми серьезными побочными эффектами алкилирующих цитостатиков являются супрессия костного мозга, развитие инфекций и недостаточность гонад. Другие осложнения гепатит, алопеция, геморрагический цистит, желудочно-кишечные расстройства и повышенный риск развития опухолей. Селективный иммунодепрессант циклоспорин А (ЦсА) подавляет активность Т хелперов (CD 4), продукцию интерлейкина 2, цитотоксических Т клеток. Селективный иммунодепрессант Такролимус. Селективный иммунодепрессант микофенолат мофетил – ингибитор инозинмонофосфата дегидрогеназы, ингибирует пролиферацию Т и В лимфоцитов. Начальная доза ЦсА для взрослых в нефрологической клинике составляет 3—5 мгкг, для детей — 6 мгкг в день. В дальнейшем доза зависит от переносимости, наличия побочных эффектов и концентрации в сыворотке крови, которую следует регулярно проверять. ЦсА показан в первую очередь больным с минимальными изменениями и фокально- сегментарном гломерулосклерозе при частом рецидивировании нефротического синдрома или стероидорезистентном нефротическом склерозе, при развитии осложнений стероидной и цитостатической терапии. Наиболее серьезными осложнениями лечения ЦсА являются артериальная гипертензия и нефротоксичность.
При назначении иммуносупрессивной терапии надо руководствоваться следующими положениями.
- • При высокой активности гломерулонефрита всегда показана иммуносупрессивная терапия.
- • Впервые возникший нефротический синдром, особенно без гематурии и гипертонии — всегда показание для лечения глококортикомдами.
- • При быстропрогрессирующих формах нефрита (с быстрым нарастанием уровня креатинина) обязательно назначение иммунодепрессантов — большие дозы глюкокортикоидов и цитостатиков внутрь и/или в виде “пульсов”.
Плазмаферез – элиминация циркулирующих иммунных комплексов. Антикоагулянты (преимущественно, гепарин), антиагреганты (преимущественно дипиридамол). Симптоматическая нефропротекторы иАПФ, антагонисты АРА II, антагонисты кальция, бета-блокаторы диуретики (тиазидовые и петлевые), статины (при развитии нефротического синдрома). Заместительная гемодиализ, перитонеальный диализ, трансплантация почек. Прогноз и исходы прогноз заболевания зависит от морфологического варианта гломерулонефрита, частоты обострений, развития хронической почечной недостаточности. Пациенты находятся на дипансерном учете в одном из нефрологических центров города с контролем лабораторных и функциональных показателей, при необходимости — госпитализации. Первичная профилактика заключается в своевременном лечении стрептококковой инфекции для предотвращения развития острого гломерулонефрита, в случае хронического гломерулонефрита – профилактика раннего развития осложнений (в частности, хронической почечной недостаточности).
