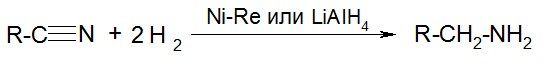Функциональными производными карбоновых кислот
называются соединения следующей структуры:

РЕАКЦИИ АЦИЛИРОВАНИЯ

Легкость ухода Х уменьшается с уменьшением устойчивости аниона Х- в ряду:
Cl- > R-COO- > HO- > RO- > NH2—
Более трудно уходящая группа замещает более легко уходящую.
Галогенангидриды
1. Получение
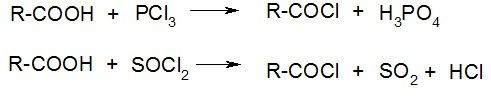
2. Реакции ацилирования
Галогенангидриды – самые активные ацилирующие агенты:
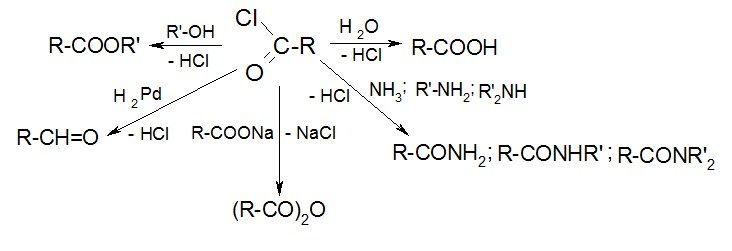
Ангидриды — продукты отщепления воды от двух молекул кислоты
1. Получение
а) промышленный способ получения уксусного ангидрида: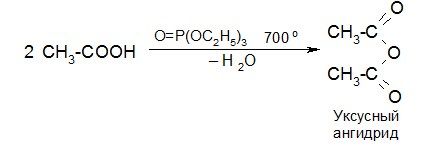
б) универсальный способ, в том числе для получения смешанных ангидридов: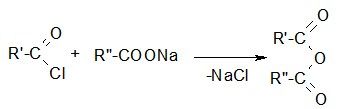
Циклические ангидриды – янтарный, глутаровый, фталевый – получаются при нагревании соответ-ствующих дикарбоновых кислот
2. Реакции ацилирования
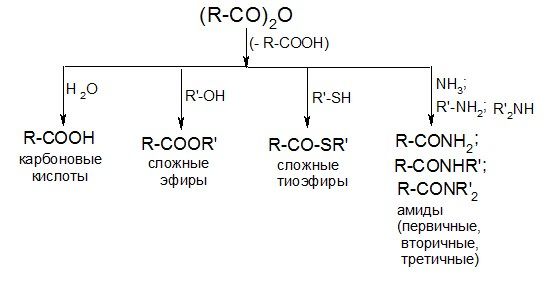
Сложные эфиры
1. Получение:
а) Реакция этерификации
б) Реакция солей карбоновых кислот с галогеналкилами:
![]()
1. Реакции ацилирования
а) гидролиз
Кислотный гидролиз – реакция, обратная этерификации
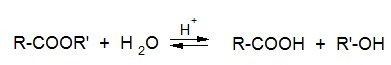
Щелочной гидролиз (омыление):

б) переэтерификация
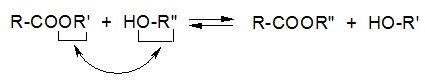
Реакция обратима, катализируется кислотами и основаниями, идет по тем же механизмам, что этерификация и гидролиз. Смещение равновесия в ту или другую сторону регулируется количественным соотношением спиртов R’-OH и R»-OH.
в) сложноэфирная конденсация Кляйзена:
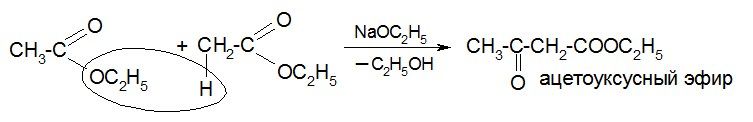
3. Взаимодействие с магнийорганическими соединениями
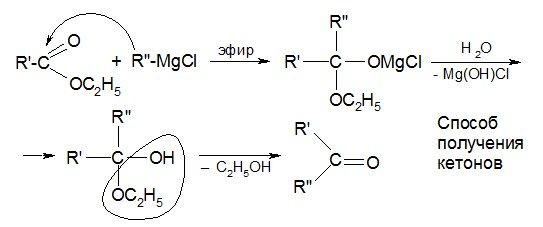
4. Восстановление
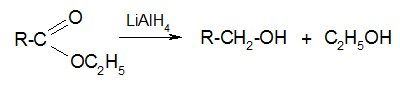
МАЛОНОВЫЙ ЭФИР — применение в органическом синтезе
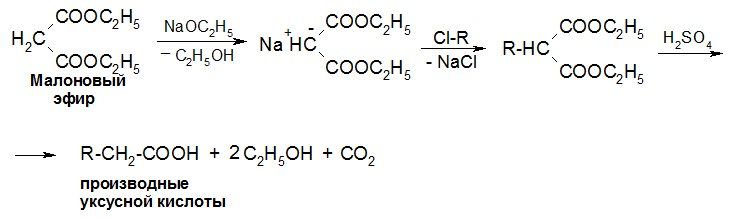
Амиды
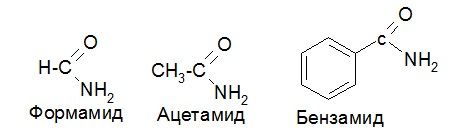
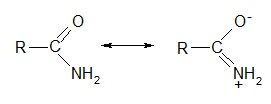
СТРОЕНИЕ АМИДОВ
1. Получение амидов
а) см. реакции ацилирования карбоновых кислот, ангидридов и галогенангидридов с аммиаком и аминами. Например, метод Шоттена-Баумана:
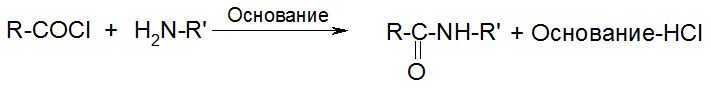
б) аммонолиз сложных эфиров:
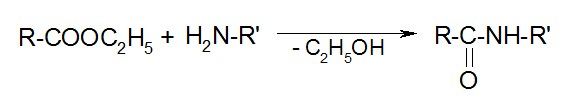
2. Химические свойства амидов
а) кислотно-основные свойства
Амиды – слабые основания и слабые кислоты, не образуют устойчивых солей.
б) гидролиз:
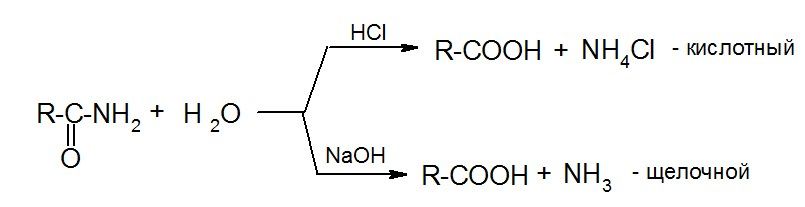
в) ацилирование:
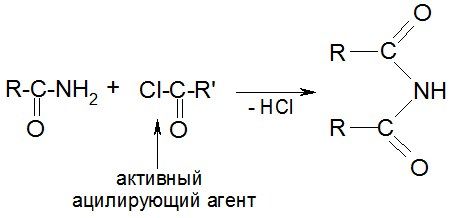
г) расщепление под действием гипогалогенитов (перегруппировка Гофмана):
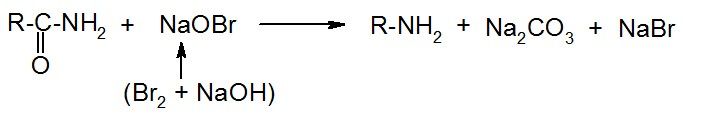
Нитрилы (цианиды)
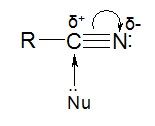
1. Получение нитрилов
а) нуклеофильное замещение галогенов на цианид:
![]()
б) присоединение HCN к кратным связям:
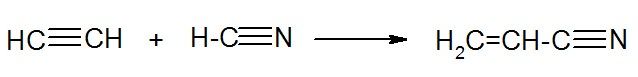
в) дегидратация амидов:
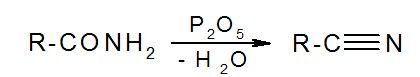
2. Химические свойства нитрилов
а) гидратация и гидролиз:
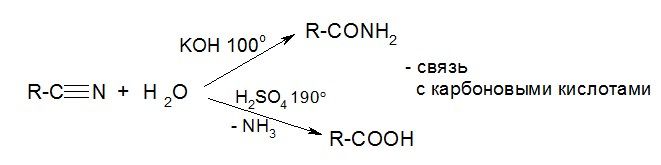
б) восстановление (гидрирование):