ФЛАВОНОИДЫ
Фармакогнозия. Карпук В.В. – 2011
Лекарственные растения, содержащие флавоноиды
Флавоноиды — большая группа природных кислородсодержащих гетероциклических соединений, в основе строения которых лежит дифенилпропановый скелет С6 -С3 -С6:

Свое название эти вещества получили от латинского слова flavus — желтый, так как первые выделенные флавоноиды имели желтую окраску. Это же название им дал в 1895г. химик С. Косанецкий, стоявший у истоков изучения данных веществ.
Химическая структура и классификация Большинство флавоноидов относят к производным хромана (бензо-гамма-пирона) и хромана (бензо-гамма-пирана). Их группируют исходя из:
- — степени гидроксилирования и окисленности (СН2) 3 -фрагмента;
- — положения бокового фенильного радикала;
- — величины гетероцикла.
Флавоноиды подразделяют на следующие группы:
- — эуфлавоноиды с боковым фенильным радикалом у С2;
- — изофлавоноиды с фенильным радикалом у С3;
- — бифлавоноиды;
- — неофлавоноиды.

В растениях большинство флавоноидов присутствует в форме гликозидов, кроме катехинов и лейкоантоцианидинов. В углеводной части могут быть как моносахариды — Д-глюкоза, Д-галактоза, L-рамноза и др., так и некоторые специфические дисахариды—рутиноза, т.е. рамноза + глюкоза, софороза (две молекулы глюкозы). Сахара могут присоединяться к агликону в 3, 7, 3- и 4- и других положениях.
Основную группу флавоноидов составляют О-гликозиды; реже встречаются С-гликозиды, где углеводные компоненты связаны с агликоном через С 6 или С 8 . Известны также ацилированные гликозиды, содержащие ацильные остатки в агликоновой или углеродной части молекулы, которые могут отдавать бензойная, уксусная, протокатеховая, кофейная и другие кислоты. О-гликозидывзависимости от числа остатков сахара, положения и порядка их присоединения делятся на монозиды, биозиды, триозиды и дигликозиды. В дигликозидах, как правило, моносахара присоединяются в двух разных положенииях флавоноидного ядра. Для флавоноидов характерно также гидроксилирование. Присоединение ОН-групп возможно почти во всех положениях. У некоторых флавоноидов гидроксилы еще метилированы, т. е. имеют метоксигруппы.
Биосинтез флавоноидов изучен достаточно хорошо. Установлено, что он происходит по смешанному типу: кольца А и С образуются по ацетатному пути, а кольцо В через шикимовую кислоту. Шикимовая кислота при участии АТФ претерпевает ряд превращений и становится префеновой кислотой, которая является ключевым промежуточным продуктом в биосинтезе не только флавоноидов, но и кумаринов, аминокислот ароматического ряда, ряда фенольных соединений, один из таких продуктов — п-кумаровая кислота. Из нее затем образуется халкон, считающийся предшественником всех других флавоноидов.
1. К эуфлавоноидам относятся производные:
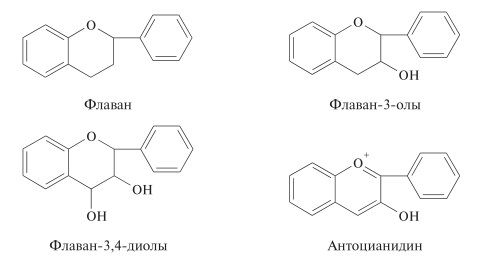
- — флавана (2-фенилхромана): флаваны, катехины (флаван-3-олы), лейкоантоцианидины (флаван-3, 4-диолы), антоцианидины (например, цианидин, пеларгонидин, дельфинидин);
- — флавона (2-фенилхромона): флавоны (например, апигенин, лютеолин), флавонолы (кемпферол, кверцетин, мирицетин, а также гликозиды — кверцетрин (кверцетин-3-рамнозид), рутин (кверцетин-3-глюко-рамнозид), гиперозид (кверцетин-3-галактозид), авикулярин (кверцетин-3-арабинозид), флаваноны (нарингенин), флаванонолы (таксифолин);

— флавоноидов с раскрытым пироновым кольцом: халконы, дигидрохалконы, изохалконы;
— флавоноидов с пятичленным фуроновым кольцом: ауроны (например, сульфуретин).

К изофлавоноидам относятся соединения с фенильным радикалом в положении С 3: изофлаван, изофлавон, изофлавонон.
Неофлавоноиды: 4-бензохроман (неофлаван), 4-бензокумарин.
Бифлавоноиды: димеры из субъединиц флавонов, флаванонов и др., связанных С-С-связью: например, 5, 7, 8’-биапигенин (аментофлавон).
Физико-химические свойства
Большинство флавоноидов — твердые кристаллические вещества, без запаха, бесцветные или желто-коричневые, с определенной температурой плавления. Чистые флавоноиды отличаются по цвету: в желтый цвет окрашены флавоны, флавонолы, халконы, ауроны; бесцветны катехины, лейкоантоцианидины, флаваны, флаваноны, изофлавоны, а антоцианидинам присущи яркие оттенки синего или красного цвета, в зависимости от рН среды. В кислой среде они имеют красный цвет (соли катионов), в щелочной — синий (соли анионов). Флавоноиды флуоресцируют в УФ-свете, при этом на хроматограммах флавоны, флавонол-3-гликозиды, флаваноны, халконы обнаруживаются в виде коричневых пятен, флавонолы и их 7-гликозиды — в виде желтых или желто-зеленых пятен.
Флавоноидные гликозиды оптически активны. Преобладающие О-гликозиды при действии разбавленных минеральных кислот и ферментов легко отщепляют углеводный остаток. С-гликозиды при действии концентрированных кислот (СН3СООН, НСl, H2SO4) даже при длительном нагревании расщепляются с трудом. Катехины и лейкоантоцианидины гликозидных форм не образуют. Они легко окисляются под действием света и гидроксидов щелочных металлов. Остальные флавоноиды более устойчивы к окислению. Флавоноиды в кислой среде в присутствии Mg 2+ или Zn 2+ могут восстанавливаться атомом водорода.
Флавоноиды взаимодействуют со щелочами с образованием фенолятов, имеющих желтый цвет; при нагревании плотность их окраски усиливается до оранжевой и коричневой. Благодаря карбонильным и фенольным оксигруппам флавоноиды способны образовывать комплексы с солями металлов различной степени устойчивости. Свободная ОН-группа в седьмом положении способствует реакции диазотирования.
Агликоны флавоноидов не растворимы в воде, но хорошо растворимы в метиловом и этиловом спиртах, органических растворителях (диэтиловом эфире, ацетоне, бензоле) и растворах гидроксидов щелочных металлов. Гликозиды флавоноидов, содержащие более трех сахарных остатков, растворимы в воде, водно-спиртовых смесях, спиртах (при нагревании), этилацетате и не растворимы в органических растворителях (петролейном и диэтиловом эфирах, дихлорэтане, четыреххлористом углероде).
Выделение флавоноидов из ЛРС
Не существует универсального метод авыделения флавоноидов из ЛРС. Учитываются свойства выделяемых веществ, сопутствующие вещества, особенности ЛРС. Обычно проводят экстракцию флавоноидов из ЛРС одним из подходящих растворителей: этанолом, метанолом, горячей водой или водно-спиртовой смесью. Как правило, в качестве экстрагента флавоноидов из ЛРС используют этиловый или метиловый спирт либо их смеси с водой. Для лучшей экстракции спиртовые растворы с ЛРС нагревают. Полученные спиртовые извлечения затем выпаривают до водного остатка, разбавляют горячей водой и из водной фазы удаляют балластные липофильные вещества (смолы, жирные масла, хлорофилл), используя делительную воронку и прибавление дихлорэтана или четыреххлористого углерода. После очистки агликоны флавоноидов извлекают этиловым эфиром, монозиды — этилацетатом, биозиды и триозиды — н-бутанолом, насыщенным водой, либо другими органическими растворителями. Вытяжку флавоноидов разделяют на компоненты, используя колоночную хроматографию и сорбенты—силикагель, полиамид, оксид алюминия, целлюлозу (бумагу) и др. Элюирование флавоноидных веществ с колонки (или бумаги) в форме агликонов проводят смесью хлороформа с метанолом (или этанолом) с возрастающей концентрацией спирта, а в форме гликозидов — водно-спиртовыми смесями, начиная от воды с увеличением доли спирта. Идентификацию флавоноидов проводят по совокупности их физико-химических свойств и на основании сравнения с данными таблицы.
Качественные реакции на флавоноидные соединения
- Цианидиновая проба, проводимая с помощью концентрированной хлористо-водородной кислоты и стружки металлического магния. Выделяющийся водород действует на молекулу флавоноидов с образованием оксониевого соединения, имеющего окраску от оранжевой (флавоны) до красно-фиолетовой (флавонолы, флаваноны, флаванонолы). Халконы, ауроны и изофлавоны не дают окрашивания в цианидиновой реакции, но при добавлении концентрированной НСl без Mg дают красное окрашивание за счет образования оксониевых солей. Следует помнить также, что изменение условий реакции путем замены Mg на Zn приводит к изменению окраски на желто-бурую, при этом положительную реакцию дают флавонолы и флаван-3-О-гликозиды, а флаваноны не дают положительной реакции. Важно отметить также, что окрашенные соединения в этой реакции можно фотоколориметрировать, т. е. получить приблизительную количественную оценку содержания отдельных флавоноидов.
- При добавлении к спиртовому извлечению флавоноидов нескольких капель раствора гидроксида натрия или калия наблюдается желтое окрашивание — его дают флавоны, флавонолы, флаваноны, оранжево-красное и пурпурное — ауроны, халконы, синее — антоцианы.
- При добавлении к спиртовому извлечению флавоноидов 2—3 капель 2% спиртового раствора хлорида алюминия (или циркония) наблюдается реакция комплексообразования и появление желтого окрашивания с яркой зеленой флуоресценцией в УФ-лучах. Эта реакция очень наглядна при изучении пятен флавоноидов на хроматограммах в УФ-свете.
- Для выявления флавоноидов часто используют борно-лимонную реакцию (или реакцию Вильсона — Таубека): 5-оксифлавоны и 5-оксифлавонолы с борной кислотой в присутствии лимонной кислоты дают желтую окраску с красноватой флуоресценцией в УФ-свете. Замена лимонной кислоты на щавелевую ведет к изменению цвета флуоресценции пятен флавоноидов с красноватого на желтый или зеленый.
- Флавоноиды с ацетатом свинца (средним и оснóвным) образуют желтые хлопья в растворе, выпадающие в осадок.
- Флавоноиды со свободной оксигруппой у С 7 легко образуют азокрасители с диазотированной сульфокислотой и другими производными ароматических аминов.
- Флавоноиды, как и все фенольные соединения, взаимодействуют с ионами Fe 3+ с образованием комплексов, окрашенных главным образом в сине-черный и зелено-черный цвета. Реакция малоспецифична.
- С треххлористой сурьмой флавоноиды (5-оксифлавоны и 5-оксифлавонолы) взаимодействуют с образованием комплексных соединений, окрашенных в желто-оранжевый (флавоны) или красно-фиолетовый (халконы) цвет.
- При хроматографическом разделении суммы флавоноидов из ЛРС на бумаге (или в тонком слое сорбента) смесью бутанол, уксусная кислота и вода (4: 1: 5) под УФ-лучами выявляются (без обработки хроматограмм проявляющими реактивами) желтые, буро-желтые или коричневые пятна. А после проявления хроматограмм спиртовым раствором гидроксида натрия или калия—оранжевое или красное свечение (после проявления в парах аммиака — оранжево-коричневое свечение).
Количественное определение содержания флавоноидов в ЛРС
Для этого используют различные химические и физико-химические методы:
- — УФ-спектрофотометрию и флуориметрию — методы, основанные на способности флавоноидов поглощать свет в УФ-области спектра и флуоресцировать;
- — хроматоспектрометрию — более совершенный метод количественного определения содержания флавоноидов в сочетании с хроматографией, позволяющий проводить очистку и разделение на отдельные компоненты;
- — фотоколориметрию — метод, основанный на цветных реакциях, в частности реакциях комплексообразования с солями различных металлов—алюминия, циркония, хрома, сурьмы; на реакции восстановления атомарным водородом в кислой среде в присутствии металлического магния или цинка, а также на реакции с борно-лимонным реактивом.
Распространение и локализация в растениях
Флавоноиды содержатся в микроорганизмах, грибах, водорослях, во мхах и других высших растениях, особенно в видах семейств Бобовые (Fabaceae), Гречишные (Polygonaceae), Сельдерейные (Apiaceae), Астровые (Asteraceae), Рутовые (Rutaceae), Березовые (Betulaceae), Розовые (Rosaceae). В растениях флавоноиды накапливаются в различных частях: бутонах (софора японская), цветках (бессмертник песчаный, василек синий), траве (горец птичий, череда, сушеница топяная), плодах (боярышник, арония черноплодная), корнях (стальник пашенный, шлемник байкальский). Содержание флавоноидов в ЛР колеблется в широких пределах—от0, 5—1% (василек синий) до 30% (бутоны софоры японской).
В надземных частях растений более 85% суммы флавоноидов локализуется в клетках эпидермы и только 15 % — в остальных тканях. Около 40 % растительных флавоноидов приходится на группу производных флавонола, около 20 % — производные флавона, почти 10 % — катехины, антоцианидины, флаваноны, ауроны, халконы. Некоторые группы флавоноидов встречаются в растениях редко и в небольших количествах.
В живых тканях растений флавоноиды обычно находятся в форме гликозидов (преимущественно О-гликозидов). Флавоноидные гликозиды накапливаются в основном в вакуолях, но некоторые обнаруживаются в хромо- и хлоропластах. Гликозильные группы обычно присутствуют в положениях С3 -, С5 -, С7 -, С3’-, C4’-, C5’-молекул флавоноидов. Из углеводов во флавоноидных гликозидах часто присутствуют глюкоза, рамноза, арабиноза, галактоза, ксилоза. В зависимости от количества сахаристых остатков (1, 2, 3) различают монозиды, биозиды, триозиды.
Флавоноиды, находящиеся в свободном состоянии (агликоны), как правило, обнаруживаются в специальных образованиях — смоляных ходах, эфиромасличных канальцах, вместилищах, железках, а также в омертвевших деревянистых тканях, где они, вероятно, высвобождаются из гликозидов под действием ферментов-гидролаз.
Влияние различных факторов на накопление флавоноидов
На накопление флавоноидов в растениях оказывают влияние следующие факторы:
- возраст и фаза развития растения. Как правило, в молодых растениях флавоноидов больше, в старых — меньше. Максимальное их содержание наблюдается в цветках, листьях и травах в период бутонизации и цветения, в фазе плодоношения количество этих веществ становится меньше. В плодах и семенах наибольшее количество флавоноидов отмечается в стадии молочной зрелости — полного созревания семян, в корнях — в период увядания надземной части растения осенью;
- освещенность: содержание флавоноидов увеличивается с ростом освещенности, а степень их гидроксилирования (число ОН-групп) — с увеличением высоты над уровнем моря;
- температура: содержание антоцианов увеличивается при понижении температуры (например, листья щавеля осенью краснеют); наоборот, содержание других групп флавоноидов увеличивается с ростом температуры.
Значение флавоноидов в жизни растений
Биологическая роль флавоноидов для растений изучена недостаточно. На основании имеющихся данных можно утверждать, что флавоноиды принимают участие:
- — в различных окислительно-восстановительных процессах в клетках растений;
- — защите аскорбиновой кислоты и других биомолекул от окисления, т.е. являются антиоксидантами;
- — защите растений от неблагоприятных воздействий УФ-лучей и низких температур;
- — инициации симбиоза с азотфиксирующими бактериями и микоризными грибами, в выработке и проявлениях фитоиммунитета;
- — процессе двойного оплодотворения у высших растений;
- — проявлении разнообразной окраски цветков и плодов, что привлекает внимание насекомых и тем самым способствует опылению и оплодотворению растений.
Медико-фармакологическое действие флавоноидов и их терапевтическое применение
Использование флавоноидов в медицине обусловлено широким диапазоном их биологического действия, повсеместным распространением и почти полным отсутствием токсичности. Флавоноиды имеют следующие свойства:
- 1) P-витаминную активность, в частности, способность уменьшать проницаемость стенок капилляров и хрупкость сосудов. Практическое значение имеют рутин и кверцетин (получаемые из софоры японской), катехины чая, флавоноиды из плодов цитрусовых, аронии черноплодной, шиповника. Известно, что P-витаминное действие усиливается при одновременном приеме с витамином С (синергизм действия);
- 2) антисклеротическую активность: флавоноиды могут снижать концентрацию холестерина и—липопротеидов в крови эффективнее, чем известные противосклеротические ЛС Полиспонин и Цетамифен;
- 3) спазмолитическую активность: выраженным спазмолитическим эффектом обладают ЛС на основе лютеолина и кверцетина; спазмолитическое действие присуще также кемпферолу, рутину, изорамнетину и другим флавоноидам. Наибольшую активность проявляют агликоны;
- 4) противовоспалительую, противоязвенную, ранозаживляющую активность: суммарные ЛС флавоноидов солодки — Флакарбин и Ликвиритон, календулы лекарственной — Калефлон — индивидуальные флавоноиды—рутин, кверцетин;
- 5) желчегонную активность, выявленную у катехинов чая, флавоноидов мяты перечной, цветков бессмертника, плодов шиповника, цветков пижмы, которые служат сырьем для получения ЛС Холосаса, Фламина, Флакумина соответственно. Известны и другие желчегонные препараты флавоноидов: Танацехол (из пижмы), Конвафлавин (из ландыша майского);
- 6) гипоазотемическую активность, т. е. способность понижать в крови уровень азотистых веществ, что характерно для агликонов флавоноидов леспедеции головчатой (Леспенифрил) и леспедеции двухцветной (Леспефлан) и используется при лечении почечной недостаточности;
- 7) сердечно-сосудистую активность, т.е. оказывают влияние на работу сердца и сосудов, увеличивают амплитуду сердечных сокращений, восстанавливают работу сердечной мышцы при утомлении и отравлении хлороформом, нормализуют ритм, в особенности рутин, кверцетин, мирицетин, мирицитрин, лейкоантоцианидины;
- 8) сосудорасширяющее действие, в том числе и на коронарные сосуды сердца: Флакразид (сумма полифенолов из цветков боярышника), а также отдельные флавоноиды — кверцетин, кемпферол, гиперозид;
- 9) кардиотоническое действие: настойка плодов боярышника, Кардиовален;
- 10) седативное действие: настойка пустырника и др.;
- 11) гипотензивное действие: настойка пустырника, настой сушеницы топяной;
- 12) мочегонное действие: флавоноиды хвоща полевого, горца птичьего, шлемника байкальского;
- 13) противовирусную и антимикробную активность: флавоноиды из ивы остролистной, лютеолин-7-гликозид и др.;
- 14) эстрогенное действие: флавоноиды Бобовых увеличивают скорость созревания яйцеклетки, способствуют рецепции сперматозоидов при оплодотворении, помогают при лечении бесплодия;
- 15) радиопротекторное и противоопухолевое действие: катехины чая, флавоноиды цитрусовых — антоцианидины, кверцетин, рутин.
Заготовка и хранение ЛРС, содержащее флавоноиды в надземной части, заготавливают в фазу бутонизации (начала цветения), в подземной — в конце вегетации. Собранное сырье быстро сушат, так как флавоноидные гликозиды быстро гидролизуются, а агликоны окисляются. Сушат сырье в тени в сушилках (при температуре 50—60С, но не выше 90С). Медленная сушка, особенно на солнце, ведет к разрушению флавоноидов. Хранят сырье в упакованном виде без доступа прямых солнечных лучей.
