ЭНДОКРИННАЯ ПАТОЛОГИЯ И БЕРЕМЕННОСТЬ
Клинические лекции по акушерству (учебное пособие)
- Сахарный диабет и беременность
- Классификация сахарного диабета
- Причины вторичного сахарного диабета
- Течение сахарного диабета при беременности
- Родоразрешение при сахарном диабете
- Диабетическая нефропатия
- Заболевания щитовидной железы и беременность
- Функциональные изменения щитовидной железы при беременности
- Взаимодействие тиреоидной системы матери и плода
- Струма (зоб)
- Гипертиреоз
- Клиническая картина диффузного токсического зоба
- Гипотиреоз
- Тиреоидная патология и невынашивание беременности
- Заболевания щитовидной железы в послеродовом периоде
САХАРНЫЙ ДИАБЕТ И БЕРЕМЕННОСТЬ
Сахарный диабет — заболевание, характеризующееся недостаточностью инсулина в организме: абсолютной, когда поджелудочная железа вырабатывает малое количество гормона, или относительной, когда ткани больного человека невосприимчивы к инсулину, хотя секреторная функция поджелудочной железы не нарушена.
Болезнь встречается у 0,5% от общего количества рожающих женщин, причем число беременных с диабетом ежегодно увеличивается в связи с аналогичной тенденцией в популяции.
Лечение инсулином позволило подавляющему большинству пациенток иметь детей, однако перинатальная смертность остается достаточно высокой (около 15-20%). Она при рациональной тактике лечения и ведения беременных может быть значительно сокращена — до 2-3%, если в качестве причины смерти плода и новорожденных останутся только несовместимые с жизнью пороки развития. Эти аномалии развития органов и систем зависят от степени декомпенсации сахарного диабета в период зачатия и на ранних стадиях беременности.
Классификация сахарного диабета
Диабет I типа (ИЗСД) — аутоиммунное заболевание, при котором происходит разрушение β-клеток поджелудочной железы. Развивается у детей и подростков, характеризуется абсолютной инсулиновой недостаточностью, лабильностью течения, склонностью к кетоацидозу, появлением ангиопатий, наличием аутоантител к собственным антигенам β-клеток поджелудочной железы. Риск развития диабета у потомства при заболевании матери 2-3%, отца — 6,1%, обоих родителей — 20%.
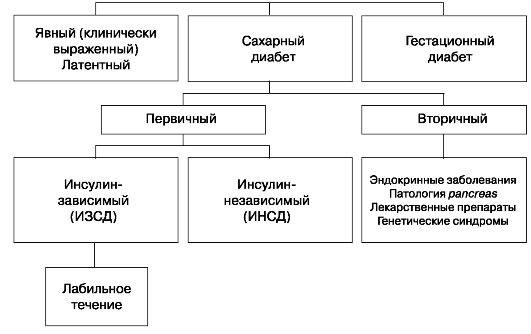
Диабет II типа (ИНСД) — возникает у людей старше 30 лет, часто на фоне ожирения, ему свойственна относительная инсулиновая недостаточность: снижена чувствительность тканей к эндогенному инсулину, инсулинорезистентность. При этой форме сахарного диабета при позднем начале и нерезко выраженных метаболических нарушениях функциональное состояние репродуктивной системы не нарушается. Риск развития диабета у потомства очень велик — аутосомно-доминантный тип наследования.
Причины вторичного сахарного диабета
- Патология поджелудочной железы: хронический панкреатит, карцинома, гемохроматоз, резекция железы.
- Эндокринные заболевания: синдром Кушинга, акромегалия, феохромоцитома, гипертиреоз, глюкагонома.
- Лекарственные препараты: кортикостероиды, АКТГ, тиазидовые диуретики, диазоксид, оральные контрацептивы.
Особенности инсулинозависимого сахарного диабета и инсулиннезависимого сахарного диабета отражены в табл. 26.
Таблица 26. Особенности ИЗСД и ИНСД
| Клинические и лабораторные данные | ИЗСД | ИНСД |
| Частота | 10-20% больных диабетом | 80-90% больных диабетом |
| Начало | Быстрое | Постепенное |
| Возраст начала болезни | Обычно до 25 лет | Обычно после 35 лет |
| Симптоматика | Выраженная | Часто отсутствует |
| Инсулинозависимость | Есть | Нет |
| Наследственность | Проявляется не всегда | Обычно имеется |
| Поражение в-клеток pancreas | Есть | Нет |
| Ожирение | Отсутствует | Более чем у 60% |
| Развитие диабетических микроангиопатий | Через несколько лет | Могут присутствовать к установлению диагноза |
| Конкордантность у близнецов | 50% | 95% |
| Инсулиновые рецепторы | Нормальные | Нарушение функции |
| Уровень инсулина в плазме | Снижен | Повышен или нормальный |
| Склонность к кетоацидозу | Есть | Нет |
| Реакция на инсулин | Имеется | Инсулинорезистентность |
| Реакция на пероральные сахароснижающие препараты | Отсутствует или слабая | Положительная |
Диабет беременных (гестационный) — это транзиторное нарушение толерантности к глюкозе, впервые выявляемое во время беременности. Встречается у 4% беременных (чаще у тучных женщин) при наличии диабета у родственников и при отягощенном акушерском анамнезе (само-произвольный выкидыш, мертворождение, многоводие, рождение в анамнезе крупных детей). Гестационному диабету присуща относительная инсулиновая недостаточность. Выявляется чаще в 27-32 нед беременности, исчезает через 2-12 нед после родов. Патогенез диабета беременных сходен с патогенезом сахарного диабета II типа. Различие состоит в том, что основными факторами, определяющими инсулинорезистентность, являются свойственные беременности гормональные и метаболические изменения.
Если у женщины имел место гестационный диабет, то в течение 10-20 лет после родов развивается диабет как хроническое заболевание, чаще трансформируясь в диабет II типа (риск в 306 раз выше, чем в популяции).
Инсулин — анаболический гормон, способствующий утилизации глюкозы и биосинтезу гликогена, липидов, белков. При недостатке инсулина нарушается утилизация глюкозы, увеличивается глюконеогенез, результатом чего становится гипергликемия — основной признак сахарного диабета.
Для плода глюкоза необходима в качестве основного источника энергии, поэтому действие основных гормонов беременности (плацентарного лактогена, эстрогенов, прогестерона, а также кортикостероидов) контринсулярное. Нормальная беременность характеризуется понижением толерантности к глюкозе, чувствительности к инсулину, усиленным распадом инсулина и увеличением уровня свободных жирных кислот. Физиологические изменения углеводного обмена при беременности расцениваются как сходные с изменениями при сахарном диабете, поэтому беременность рассматривается как диабетогенный фактор.
Различают диабет явный (клинически выраженный) и латентный (нарушение толерантности к глюкозе).
Предрасположенность к сахарному диабету
- Оба родителя больны сахарным диабетом или имеется наследственная предрасположенность.
- Один из однояйцовых близнецов — диабетик.
- Женщины, родившие ранее живых или мертвых детей с массой более 4500.
- Женщины, родившие ранее мертвого ребенка с гиперплазией островкового аппарата поджелудочной железы.
- Женщины с ожирением.
- Женщины с привычным невынашиванием.
- Беременные с многоводием.
- При глюкозурии.
Жалобы больных сахарным диабетом
- Сухость во рту.
- Жажда (полидипсия).
- Потребление увеличенного количества жидкости (более 2 л).
- Полиурия.
- Повышенный или пониженный аппетит.
- Слабость.
- Похудание.
- Зуд кожи, особенно в области ануса, половых органов.
- Нарушение сна.
- Склонность к гнойничковым заболеваниям кожи.
В моче здорового человека сахара нет. Однако у беременных может определяться глюкозурия, связанная с изменением фильтрационной функции почек, а не с нарушением углеводного обмена (глюкозурия беременных). Для уверенности в том, что это не признак гестационного диабета, следует установить, каково содержание глюкозы в крови натощак. При нормально функционирующих почках глюкозурия появляется только в том случае, когда уровень сахара в крови выше 8,88-9,99 ммоль/л.
Для суждения о динамике гликемии в течение суток определяют гликемический профиль: исследуют содержание глюкозы в крови каждые 3 ч в течение суток. Нормальными показателями считаются колебания 5,5-8,3 ммоль/л, у беременных рекомендуется поддерживать уровень 3,5-7 ммоль/л. Глюкозурический профиль — определение сахара в трехчасовых порциях мочи в течение суток — показан для коррекции доз инсулина.
Сахарный диабет протекает с микроангиопатиями — генерализованным дегенеративным поражением мелких сосудов (капилляров, артериол и венул) — и с сосудистой патологией органов: глаз, почек, кожи, мышц, нервной системы, желудочно-кишечного тракта. После 30-40 лет присоединяется диабетическая макроангиопатия (ранний атеросклероз), поражающая сосуды среднего и крупного калибра. Особенно опасна диабетическая ретинопатия, сопровождающаяся прогрессирующим падением остроты зрения, кровоизлиянием в сетчатку и стекловидное тело и угрожающая слепотой. Ретинопатия отмечается у 30-90% больных.
Диабетическая нефропатия проявляется узелковым интракапиллярным гломерулосклерозом у 10-90% больных, синдром характеризуется ретинопатией, артериальной гипертензией, протеинурией, отеками, гиперазотемией.
Опасные осложнения беременности — коматозные состояния. Возможны кетонемическая и гипогликемическая комы (табл. 27).
Кетонемической (диабетической) коме предшествует прекоматозное состояние. Причинами его возникновения могут быть нарушение диеты (потребление слишком большого количества углеводистой пищи), недостаток инсулина, инфекция, интоксикация. Прекоматозное состояние характеризуется усилением жажды, потерей аппетита, слабостью, утомляемостью, тошнотой, рвотой, сонливостью, появлением запаха ацетона изо рта, обезвоживанием, потерей электролитов. Развиваются сердечнососудистая, почечная недостаточность, потеря сознания — кома. Кома сопровождается обезвоживанием, олигурией, снижением тургора кожи и упругости глазных яблок, сухожильных рефлексов, адинамией, тахикардией, снижением АД, шумным дыханием Куссмауля, потерей сознания, коллапсом. Лабораторные исследования выявляют гипергликемию и гиперкетонемию, много сахара и ацетона в моче, появляются метаболический ацидоз, азотемия, гипокалиемия и гипонатриемия. Кетонемическая кома развивается медленно, постепенно.
Гипогликемические состояния и гипогликемическая кома могут возникать при передозировке инсулина или недостаточном приеме углеводов при введении обычной дозы инсулина. Больные при гипогликемии беспокойны, жалуются на страх смерти, слабость, голод, потливость, познабливание, онемение кончика языка, тремор, бледность, тахикардию. Позже присоединяются дискоординация движений, смазанность речи, афазия, возбуждение, судороги, помутнение сознания и кома.
Гипергликемические состояния во время беременности возникают реже, чем до нее, а гипогликемические — значительно чаще.
Различают три степени тяжести сахарного диабета:
- Легкая степень — гипергликемия натощак <7,7 ммоль/л; нет признаков кетоза; нормализация уровня сахара диетой.
- Средняя степень — гипергликемия натощак <12, 7 ммоль/л;нет признаков кетоза; инсулинотерапия в дозах не >60 ЕД.
- Тяжелая степень — гипергликемия натощак >12,7 ммоль/л; выраженный кетоацидоз; микроангиопатии; инсулинотерапия в дозе >60 ЕД/сут.
Таблица 27. Дифференциальная диагностика ком
| Признаки | Диабетическая кома | Гипогликемическая кома |
| Скорость нарастания темпов | Постепенно, в течение нескольких дней, реже — часов | Быстро, при длительном лечении инсулином — в течении нескольких часов |
| Запах ацетона изо рта | Резкий | Отсутствует |
| Дыхание | Шумное, Куссмауля | Нормальное |
| Кожа | Сухая, тургор понижен | Влажная, тургор нормальный |
| Тонус глазных яблок | Понижен | Нормальный |
| Мышечный тонус | Снижен | Нормальный |
| Сухожильные рефлексы | Снижены или отсутствуют | Нормальные |
| Пульс | Частый | Частый, нормальный |
| АД | Снижено | Нормальное |
| Сахар в моче | В большом количестве | Отсутствует |
| Ацетон в моче | В большом количестве | Отсутствует |
| Сахар в крови | >19, 4 ммоль/л | <2,2 ммоль/л Нормальные |
| Кетоновые тела в крови | Повышены | |
| Лейкоциты крови | Увеличены | Нормальные |
| Щелочной резерв крови | Снижен | Нормальный |
Течение сахарного диабета при беременности
- I триместр: улучшение течения болезни, снижение уровня глюкозы в крови, гипогликемия. Госпитализация для компенсации сахарного диабета, решение вопроса о пролонгировании беременности.
- II триместр: рост гипергликемии, увеличение дозы инсулина (контринсулярные гормоны плаценты). Госпитализация в 20-24 нед для коррекции гипогликемии.
- III триместр: с 32 нед гипогликемии, декомпенсация сахарного диабета. Госпитализация в 32 нед для компенсации диабета и решения вопроса о сроках и методах родоразрешения.
Госпитализация осуществялется:
- в начале беременности для компенсации диабета;
- в 20-24 нед для коррекции гипергликемии;
- в 32 нед для компенсации диабета и решения вопроса о сроках и методах родоразрешения.
Противопоказания к беременности при сахарном диабете
- Диабетические микроангиопатии.
- Инсулинорезистентные и лабильные формы диабета с наклонностью к кетоацидозу.
- Заболевание диабетом обоих супругов.
- Сочетание диабета и резус-сенсибилизации.
- Сочетание диабета и активного туберкулеза.
- Наличие в анамнезе повторных мертворождений или детей с пороками развития.
Осложнения беременности при сахарном диабете
- Невынашивание беременности — 15-31%.
- Сочетанные гестозы — 30-70%.
- Многоводие — 20-60%.
- Крупный плод — 24-27%.
- СЗРП — 20%.
- Пороки развития плода — 10-12%.
- Плацентраная недостаточность.
- Внутриутробная гибель плода (36-38 нед).
- Пиелонефрит — до 30%.
Родоразрешение при ИЗСД производится в 37 нед, до 36 нед — по витальным показаниям со стороны матери или плода.
Родоразрешение при сахарном диабете
Осложнения родов:
- аномалия родовой деятельности;
- гипоксия плода;
- клинически узкий таз;
- дистоция плечиков;
- родовой травматизм плода;
- декомпенсация диабета;
- нарастание тяжести гестоза.
Показания к кесареву сечению:
- прогрессирование ангиопатий;
- лабильное течение со склонностью к кетоацидозу;
- тяжелый гестоз;
- гипоксия плода;
- нарастающее многоводие;
- тазовое предлежание плода;
- крупный и гигантский плод.
Послеродовые осложнения
- Гнойно-септические осложнения.
- Инфекция мочевых путей.
- Гипогалактия.
- Декомпенсация сахарного диабета.
Глюкоза проходит через плаценту, а инсулин — нет. Гипергликемия у больной женщины способствует переходу глюкозы от матери к плоду и вызывает гиперплазию β-клеток островкового аппарата поджелудочной железы плода, гиперинсулинемию, макросомию и органомегалию.
Осложнения у плода:
- макросомия;
- гипогликемии у 30-60% новорожденных (гиперинсулинизм);
- диабетическая фетопатия: отечность, цианоз, кушингоидная внешность (лунообразное лицо, гипертрихоз, кожные петехии, избыточное отложение жира), незрелость;
- гипотрофия — при ИЗСД в 20% случаев (васкулопатии, гестоз);
- ВПР (в 2-4 раза чаще);
- синдром дыхательной недостаточности (гиперинсулинемия ингибирует синтез сурфактанта);
- СЗРП.
Факторами риска возникновения пороков развития плода являются плохой контроль диабета до зачатия, длительность болезни свыше 10 лет и диабетическая микроангиопатия. Гипергликемия нарушает органогенез уже на самых ранних этапах беременности. Особенно высок риск повреждений мозговой трубки, чаще встречаются пороки сердца, желудочно-кишечного тракта, мочевыделительной системы.
Перинатальная смертность:
- при ИЗСД — 150%0;
- при ИНСД — 24%;
- при гестационном сахарном диабете — 45%.
Согласно классификации P. White, процент вероятности (р) рождения жизнеспособного ребенка зависит от длительности и осложнений сахарного диабета (табл. 28):
Таблица 28. Вероятность рождения жизнеспособного ребенка у больной сахарным диабетом (классификация P. White)
| Класс | Клинические признаки |
| Класс А (р=100) | Нарушение толерантности к глюкозе и отсутствие осложнений |
| Класс В (р=67) | Длительность сахарного диабета менее 10 лет, сахарный диабет возник в возрасте старше 20 лет, сосудистых осложнений нет |
| Класс С (р=48) | Длительность сахарного диабета от 10 до 19 лет, сахарный диабет возник в возрасте 10-19 лет, сосудистых осложнений нет |
| Класс D (р=32) | Длительность сахарного диабета более 20 лет, сахарный диабет возник в возрасте до 10 лет, ретинопатия или кальцификация сосудов ног |
| Класс Е (р=13) | Кальцификация сосудов таза |
| Класс F (р=3) | Диабетическая нефропатия |
Диабетическая нефропатия
Из данных табл. 28 следует: шансы на рождение здорового ребенка у больных классов D, E, F очень невелики, беременность противопоказана.
Неблагоприятный прогностический признак для плода и новорожденного — длительное (2 нед и более) повышение минимального уровня сахара крови выше 10 ммоль/л или максимального его уровня выше 14 ммоль/л.
Новорожденный нуждается в интенсивной терапии, направленной на борьбу с гипогликемией, дыхательной недостаточностью, гипокальцимией, гипомагнимией, последствиями родового травматизма.
Тактика ведения женщин, страдающих сахарным диабетом, до и во время беременности заключается в достижении полной компенсации диабета в период, предшествующий беременности и на всем протяжении гестации.
Показатели достаточной компенсации ИЗСД: гликемия в течение суток колеблется от 4,4 до 8,3 ммоль/л; отсутствуют эпизоды гипогликемии. Критерием компенсации диабета является не только уровень глюкозы в крови (это очень лабильный показатель), но и уровень гликированного (гликозилированного) гемоглобина HbA1c; у здоровых и при компенсированном диабете уровень составляет 3-6%; при декомпенсированном диабете его количество увеличивается до 10% и более. Гликированный гемоглобин позволяет оценить средний уровень гликемии на протяжении предшествующих 1,5-2 мес.
Показатели компенсации ИНСД — нормальный уровень гликемии натощак, колебания гликемии в течение суток от 3,85 до 8,25 ммоль/л, отсутствие глюкозурии, гликированный гемоглобин <6%.
Диета беременных, больных сахарным диабетом: уменьшенное количество углеводов (200-250 г), жиров (60-70 г) и нормальное или даже увеличенное количество белков (1-2 г/кг); содержание калорий — 2000-2200. Прием пищи должен совпадать по времени с началом действия инсулина.
Пероральные антидиабетические средства противопоказаны беременным: они переходят через плаценту и оказывают тератогенное действие. При диабете II типа беременным без ожирения назначают инсулин. 1 таблетка манинила соответствует 6-8 ЕД простого инсулина. Инсулин рекомендуется назначать при гликемии больше 5,5 ммоль/л натощак и 7 ммоль/л после еды при условии соблюдения диеты.
Расчет суточной дозы инсулина: 6-8 ЕД инсулина вводят на каждые 2,7 ммоль/л глюкозы крови, превышающие физиологическую норму (5,5 ммоль/л) + 4-8 ЕД инсулина при глюкозурии >1,1% во всех порциях мочи, исследованной за сутки. Начальной фазой лечения для пациенток, нуждающихся в инсулинотерапии, является режим трех инъекций (смесь короткого и длинного инсулина утром, простой до ужина и длинный перед сном). Желательно использовать только человеческий инсулин.
В последнее время для лечения беременных с ИЗСД применяется базис-болюсная интенсивная инсулинотерапия, имитирующая работу здоровой поджелудочной железы, с применением инсулина короткого действия перед каждым приемом пищи (обычно три раза в день) и пролонгированного инсулина при моделировании базальной секреции (однократная инъекция перед сном). У женщин с ИНСД обосновано применение изолированно болюсной инсулинотерапии, состоящей из трехкратного введения инсулина короткого действия только перед приемом пищи. При гестационном диабете базальная секреция инсулина часто бывает сохранена, поэтому лечение может ограничиться назначением инсулина короткого действия, вводимого перед приемом пищи. В случае гипергликемии натощак необходимо назначение базис-болюсной инсулинотерапии. В родах и при операции кесарева сечения — дробные дозы простого инсулина под контролем гликемии.
В табл. 29 приведена характеристика действия препаратов инсулина.
Таблица 29. Характеристика действия препаратов инсулина

ЗАБОЛЕВАНИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ И БЕРЕМЕННОСТЬ
Заболевания щитовидной железы (табл. 30) — самая частая эндокринная патология. Их отличает практически десятикратно большая распространенность среди женщин, манифестация в молодом, репродуктивном возрасте и развитие тяжелых осложнений при отсутствии квалифицированной медицинской помощи.
Таблица 30. Распространенность тиреоидной патологии в общей популяции, проживающей в условиях легкого и умеренного йодного дефицита
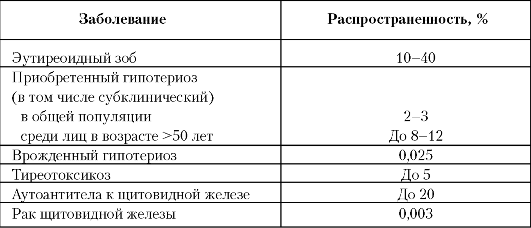
Роль гормонов щитовидной железы при беременности чрезвычайно велика. Гормоны имеют большое значение для развития плода, роста и дифференциации тканей, влияя на все виды обмена веществ.
Нарушения функции щитовидной железы при беременности повышают риск невынашивания беременности; мертворождений; задержки роста плода; ВПР.
Влияние тиреоидного статуса матери на развитие нервной системы плода, в частности головного мозга, обусловливает необходимость изучения физиологии щитовидной железы и критической оценки механизмов регуляции ее функции.
Наиболее частыми тиреоидными заболеваниями, сочетающимися с беременностью, являются увеличение щитовидной железы (струма), гипофункция (гипотиреоз), гиперфункция (гипертиреоз), воспаление (тиреоидит) и рак щитовидной железы, при этом патология щитовидной железы может предсуществовать или впервые возникать во время беременности.
Функциональные изменения щитовидной железы при беременности
Щитовидная железа в нормальных условиях — единственный источник тироксина (Т4), тогда как около 80% трийодтиронина (Т3) образуется не в щитовидной железе, а путем дейодирования Т4 в периферических тканях — мышцах, печени, почках и т.д. Плацента — дополнительное место превращения свободного (free) Т4 (FT4) в свободный Т3 (FT3).
Гормональная активность трийодтиронина приблизительно в 20 раз выше, чем тироксина. При физиологической концентрации гормонов ядерные рецепторы более чем на 90% связаны с Т3, тогда как Т4 присутствует в комплексе с рецепторами в очень небольшом количестве, что оправдывает мнение о Т4 как о прогормоне и о Т3 как об истинном тиреоидном гормоне.
Гормоны щитовидной железы в крови связаны с белками: Т4 на 60% связан с тиреоидсвязывающим глобулином, на 30% — с преальбумином, на 10% — с альбумином; T3 связан с тиреоидсвязывающим глобулином и альбумином. В связанной форме циркулирует 99,97% Т4 и 99,9% Т3, незначительные количества Т4 и Т3 находятся в свободном виде, однако именно они обладают непосредственной биологической активностью и определяют статус щитовидной железы путем отрицательной обратной связи с гипофизом. При повышении уровня гормонов щитовидной железы снижается секреция ТТГ гипофиза, при снижении их уровня секреция ТТГ возрастает.
Умеренное увеличение щитовидной железы наблюдается у 30% беременных, при этом концентрация ТТГ не изменяется. Можно заключить, что при беременности наблюдается зобогенный эффект вне зависимости от материнской концентрации ТТГ. Однако, несмотря на часто возникающую при беременности гипертрофию щитовидной железы, тахикардию, признаки увеличения основного обмена, функция щитовидной железы на протяжении беременности в целом остается нормальной.
К физиологическим изменениям функционирования щитовидной железы во время беременности (рис. 104) относятся следующие.
- Увеличение продукции тиреоидсвязывающего глобулина в печени:
- повышение уровня общих фракций тиреоидных гормонов;
- увеличение общего содержания тиреоидных гормонов в организме беременной.
- Гиперстимуляция щитовидной железы ХГ:
- физиологическое снижение уровня ТТГ в первой половине беременности;
- повышение продукции тиреоидных гормонов.
- Усиление экскреции йода с мочой и трансплацентарного переноса йода.
- Дейодирование тиреоидных гормонов в плаценте.
Концентрация тиреоидсвязывающего глобулина при гиперэстрогенемии возрастает в 2-3 раза вследствие увеличения его синтеза в печени и снижения метаболического клиренса. Это приводит к повышению уровня общего тироксина (Т4) для поддержания нормальной концентрации свободного тироксина (FT4). Увеличение содержания в сыворотке T4 начинается в I триместре и сопровождается подобным, хотя и менее выраженным, повышением уровня общего трийодтиронина (Т3). Фракция тироксина, связанного с тиреоидсвязывающим глобулином, продолжает прогрессивно увеличиваться на протяжении беременности. В регионах с недостаточным поступлением йода дополнительный синтез тироксина может нарушаться, что приводит к относительной гипотироксинемии у 1/3 беременных женщин, преимущественной секреции трийодтиронина, повышению концентрации ТТГ, увеличению размера щитовидной железы.
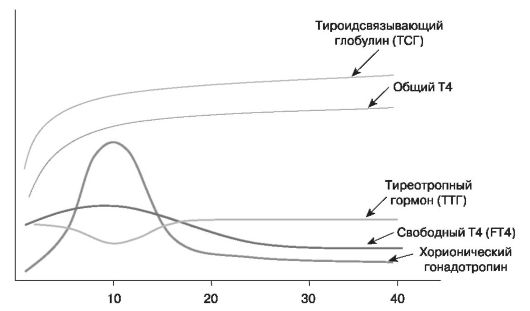
Рис. 104. Изменение функции щитовидной железы при беременности
Исследование свободных фракций гормонов щитовидной железы на протяжении беременности дает следующие результаты: незначительное повышение свободных фракций в I триместре беременности, снижение или неизменная концентрация свободных тиреоидных гормонов во II и III. Регулирование по принципу обратной связи поддерживает уровень FT4 в нормальных физиологических пределах, поэтому его изменения при беременности — самые минимальные, от нормальных или несколько повышенных значений в I триместре до слегка пониженных в III триместре. Исследование уровня FT3 при беременности дает ошибочные результаты, поэтому у беременных проводить его не рекомендуется.
Исследования с применением чувствительных методик указывают на незначительное снижение содержания ТТГ в I триместре, что, по-видимому, связано с действием ХГ, чья активность подобна таковой ТТГ. Обе молекулы имеют одинаковые α-субъединицы и некоторое сходство между специфическими β-субъединицами, что обусловливает слабую тиреоидстимулирующую эффективность ХГ (1/4000 активности ТТГ). Биохимический и клинический гипертиреоз часто наблюдается у больных с пузырным заносом и хорионэпителиомой. По-видимому, молекула ХГ выступает как антагонист ТТГ, конкурирующий с ним за мембранные рецепторы клеток щитовидной железы, что может приводить к некоторому гипертиреозу в I триместре беременности. Напротив, в III триместре при снижении количества FT4 до нижних границ физиологических значений уровень ТТГ остается нормальным, что позволяет при комбинированном определении обоих гормонов правильно оценить функцию щитовидной железы.
Таким образом, при нормальной беременности функция щитовидной железы может изменяться от компенсированного гипертиреоза в I триместре до компенсированного гипотиреоза в III триместре, что следует учитывать при оценке клинических и лабораторных данных.
Скрининг функции щитовидной железы при беременности.
- Для скрининга функции щитовидной железы при беременности необходимо определение двух показателей — FT4 и ТТГ — чувствительными методами.
- Определение концентрации общего Т4 (Т3) и использование низкочувствительных методов определения уровня ТТГ во время беременности неинформативно.
- Уровень ТТГ в первой половине беременности в норме понижен у 20-30% женщин.
- Уровни общих Т4 и Т3 в норме всегда повышены (примерно в 1,5 раза).
- Уровень FT4 в I триместре несколько повышен.
- На поздних сроках беременности в норме часто определяется низконормальный или погранично сниженный уровень FT4 при нормальном уровне ТТГ.
Взаимодействие тиреоидной системы матери и плода
Гипоталамо-гипофизарно-тиреоидная система плода начинает формироваться к концу I триместра беременности. К 10-12 нед определяется ТТГ плода, к 14 нед он достигает концентрации, выявляемой при рождении. К 11-12 нед беременности устанавливается механизм отрицательной обратной связи между ТТГ и FT4. Контроль за функцией щитовидной железы плода осуществляется (рис. 105) при участии трех механизмов: прогрессивного увеличения синтеза тиреотропин рилизинг-гормона (ТРГ) гипоталамуса, увеличения чувствительности тиреоидных клеток к ТТГ и повышения чувствительности гипофиза к ингибирующему действию тиреоидных гормонов. В своем развитии гипоталамо-гипофизарно-тиреоидная система плода проходит несколько этапов — от состояния первичного гипотиреоза (тиреоидного) и третичного (гипоталамического) в середине беременности до состояния легкого третичного гипотиреоза в III триместре и, наконец, до состояния функциональной зрелости перинатального периода.
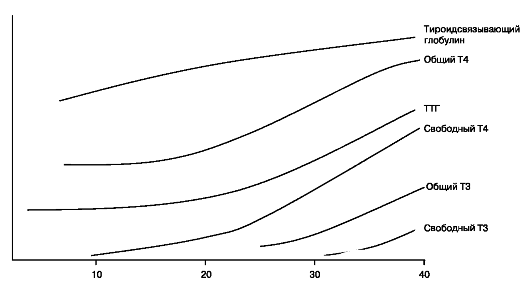
Рис. 105. Функция щитовидной железы плода
Гипоталамо-гипофизарно-тиреоидная система плода развивается автономно, однако плацента выполняет функцию селективного транспорта веществ, определяющих фето-материнские взаимоотношения.
Тироксин проходит через плаценту уже в I триместре и, по-видимому, необходим развивающемуся плоду, пока его собственная щитовидная железа еще не функционирует. ТТГ не проходит через плацентарный барьер в отличие от ТРГ. Следует учитывать, что трансплацентарно транспортируются антитиреоидные антитела, которые могут служить причиной струмы и гипотиреоза плода, и иммуноглобулины, стимулирующие щитовидную железу, с возможным развитием гипертиреоза плода и новорожденного.
Струма (зоб)
Термин «струма» (зоб) в целом означает увеличение объема щитовидной железы вне зависимости от причины (исключение — злокачественные новообразования) и функционального состояния этого органа. Нетоксический зоб классифицируется на эндемический (средняя частота в популяции — 10%), спорадический (или «простой» зоб) и семейный. Наиболее частая причина эндемического зоба – недостаточность йода в определенных регионах (потребление йода менее 20 мкг). В большинстве случаев эндемический зоб бессимптомный, эутиреоидный и, по-видимому, не влияет на репродуктивную функцию. Во время беременности величина струмы обычно возрастает, в тяжелых случаях возможно снижение концентрации тиреоидных гормонов и повышение уровня ТТГ.
Случаи спорадического зоба отмечаются в неэндемических регионах, их частота у женщин в 7-8 раз выше, чем у мужчин. Этиология простого зоба неизвестна, возможно, он — следствие индивидуальной гиперчувствительности к минимальному воздействию зобогенных факторов. У ряда пациентов со спорадическим зобом выявляется биохимический дефект синтеза тиреоидных гормонов, в этом случае струма обычно семейная. Клиническая картина при простой струме различна, в большинстве случаев струма эутиреоидная, однако возможно появление симптомов гипотиреоза или тиреотоксикоза, требующих соответствующей коррекции.
Формирование зоба ранее объясняли повышением чувствительности щитовидной железы к влиянию ТТГ в условиях йодного дефицита, однако препараты йода оказались более эффективны в стабилизации объема щитовидной железы, чем L-тироксин. По современным представлениям, повышение продукции ТТГ или повышение к нему чувствительности тироцитов имеет лишь второстепенное значение в патогенезе йододефицитного зоба. Главная роль в патогенезе принадлежит аутокринным ростовым факторам (АРФ), в частности, инсулиноподобному ростовому фактору 1-го типа (ИРФ-1), эпидермальному ростовому фактору (ЭРФ) и фактору роста фибробластов (ФРФ), которые в условиях снижения содержания йода в щитовидной железе оказывают мощное стимулирующее воздействие на тироциты. Основной физиологический блокатор продукции АРФ — йод, связанный с непредельными жирными кислотами (йодлактоны).
Диффузный эутиреоидный зоб, т.е. увеличение объема щитовидной железы (у женщин в норме меньше 18 мл), без нарушения функции не представляет опасности, однако в дальнейшем йододефицитная патология щитовидной железы может прогрессировать. В зависимости от выраженности йодного дефицита диффузный зоб (этап I) может формироваться у 10-80% всего населения.
Терапия струмы этиотропная, при диффузном эутиреоидном зобе показано назначение йодида калия в дозе около 200 мкг в день, что приводит к уменьшению объема щитовидной железы. Терапия безопасна, отсутствует необходимость в подборе дозы и проведении частых гормональных исследований.
Гипертиреоз
Клинические признаки гипертиреоза сходны с клиническими проявлениями, часто имеющими место у беременных (раздражительность, эмоциональная лабильность, тахикардия, увеличение аппетита), что существенно затрудняет диагностику. Показано: при рвоте беременных часто отмечается умеренное повышение уровня тиреоидных гормонов, однако оно редко сопровождается симптомами гипертиреоза. Существует предположение, что важная роль и в развитии рвоты беременных, и в стимуляции щитовидной железы принадлежит ХГ. При исследованиях больных с пузырным заносом и хорионэпителиомой биохимический гипертиреоз наблюдался при уровне ХГ в сыворотке, превышающем 100 000 ЕД, а клинический гипертиреоз — при концентрациях более 300 000 ЕД. Этот синдром в I триместре беременности называется «гестационным транзиторным тиреотоксикозом».
Частота клинически выраженного гипертиреоза при беременности составляет, по данным различных авторов, 0,04-1,4% (в среднем 0,2%), 95% случаев обусловлены диффузным токсическим зобом (базедовой болезнью).
Базедова болезнь — аутоиммунное заболевание, при котором образуются стимулирующие щитовидную железу антитела. В целом степень выраженности тиреотоксикоза при беременности уменьшается вследствие снижения числа тиреостимулирующих антител, что связано с иммуносупрессией беременности.
Клиническая картина диффузного токсического зоба
1. Легкое течение:
- повышенная нервная возбудимость;
- потливость;
- тахикардия до 100 ударов в минуту;
- похудание с потерей до 15% массы тела.
2. Средняя степень тяжести:
- тахикардия до 120 ударов в минуту;
- похудание с потерей более 20% массы тела;
- гипергидроз;
- выраженный тремор;
- повышение систолического и снижение диастолического давления;
- снижение трудоспособности. 3. Тяжелая степень:
- похудание до 50% (кахексия);
- частота пульса до 140 ударов в минуту, мерцательная аритмия;
- изменения печени;
- снижение функции коры надпочечников;
- нетрудоспособность.
При наличии признаков тиреотоксикоза показана терапия антитиреоидными препаратами или β-адреноблокаторами c мониторингом FT4 и ТТГ (FT4 на верхней границе физиологических значений, ТТГ в пределах нормальных значений) с назначением минимальной эффективной дозы (у них отмечено выраженное побочное действие на плод).
Второй частой причиной гипертиреоза при беременности является латентный тиреоидит, представляющий собой, по-видимому, вариант клинического течения тиреоидита Хашимото. Так, по данным некоторых авторов, его частота в послеродовом периоде составляет 5%, что клинически проявляется симптомами гипертиреоза в течение нескольких недель или месяцев с последующими симптомами гипотиреоза, иногда ошибочно расцениваемыми клиницистами как послеродовая депрессия.
Гипотиреоз
Снижение функции щитовидной железы встречается достаточно часто у женщин детородного возраста, хотя тяжелые случаи гипотиреоза редко сочетаются с беременностью. Распространенность гипотиреоза среди беременных женщин составляет около 2%. При отсутствии заместительной терапии гипотиреоз приводит к увеличению частоты невынашивания беременности, мертворождений и ВПР плода; так, частота невынашивания беременности при гипотиреозе достигает 35-50%.
Этиология гипотериоза
Первичный:
- идиопатический аутоиммунный зоб;
- тиреодит Хашимото;
- состояние после хирургического или радиолечения базедовой болезни;
- внешнее радиоактивное облучение;
- врожденное отсутствие щитовидной железы;
- врожденное нарушение синтеза тироксина;
- выраженный дефицит йода;
- прием антитиреоидных препаратов. Вторичный:
- опухоли гипофиза или гипоталамуса;
- кровоизлияния или инфаркты гипофиза;
- гипоталамическая недостаточность ТРГ;
- гипофизарно-гипоталамические инфильтративные заболевания (саркоидоз, гемохроматоз и др.).
Под субклиническим гипотиреозом понимают изолированное повышение уровня ТТГ при нормальном уровне свободного тироксина (FT4), под манифестным гипотиреозом — сочетание повышения уровня ТТГ и снижения уровня FT4.
Осложнения некомпенсированного гипотиреоза при беременности отражены в табл. 31.
Таблица 31. Осложнения некомпенсированного гипотиреоза при беременности
| Осложнение | Манифестарный гипотериоз, % | Субклинический гипотериоз, % |
| Гипертензия, преэклампсия | 22 | 15 |
| Отслойка плаценты | 5 | 0 |
| СЗРП | 16,6 | 8,7 |
| Внутриутробная гибель | 6,6 | 1,7 |
| Пороки развития | 3,3 | 0 |
| Послеродовое кровотечение | 6,6 | 3,5 |
Гипотиреоз представляет собой клинический синдром с разнообразными этиологическими факторами, возникающий как вследствие заболеваний щитовидной железы (первичный гипотиреоз), так и вследствие заболеваний гипофиза или гипоталамуса со снижением синтеза ТТГ (вторичный гипотиреоз). Случаи вторичного гипотиреоза практически никогда не сочетаются с беременностью. Наиболее частыми причинами клинического гипотиреоза при беременности являются идиопатический аутоиммунный зоб и тиреоидит Хашимото.
При гипотиреозе показана заместительная терапия тиреоидными гормонами, для контроля за лечением рекомендуется мониторинг FT4 и ТТГ каждые 8-10 нед (с 8 нед беременности). Мониторинг необходим для определения адекватной дозы тироксина, так как потребность в Т4 во время беременности возрастает на 50-100%, доза тироксина при этом может достигать 200-300 мкг/сут. С появлением нового поколения чувствительных методик определения ТТГ средняя доза L-тироксина при заместительной терапии уменьшилась до 100-150 мкг/сут, что позволяет поддерживать уровень ТТГ в пределах 1-2 мЕ/л. Пациентам с гипотиреозом после резекции щитовидной железы требуются более высокие дозы Т4, чем, например, при тиреоидите Хашимото, так как в последнем случае синтезируются некоторые количества эндогенного тироксина.
В последние годы в зарубежной литературе большое внимание уделяется транзиторному гипотиреозу, что связано с высокой частотой его распространения — около 5% популяции. Признаками транзиторного субклинического гестационного гипотиреоза являются: повышение ТТГ сыворотки в I триместре при нормальном или сниженном FT4 с последующим возвратом этих показателей к нормальным значениям приблизительно к 17 нед беременности; отсутствие субъективных жалоб; отсутствие заболеваний щитовидной железы в анамнезе; незначительное увеличение щитовидной железы; повышение уровня антител к тиреоидной пероксидазе (АТ-ТПО); нормальная концентрация ХГ сыворотки. Причина транзиторного раннего гестационного гипотиреоза в настоящее время остается неизвестной, возможно, он связан с иммунными изменениями при беременности, влияющими на течение предсуществующего латентного аутоиммунного тиреоидита.
Тиреоидная патология и невынашивание беременности
У 31% женщин с привычным невынашиванием имеются антитиреоидные антитела (антитироглобулиновые и АТ-ТПО), а частота преждевременных родов у женщин с бессимптомными аутоиммунными тиреоидными нарушениями составляет 16%. Возможно, что более высокая частота невынашивания у женщин с тиреоидными аутоиммунными нарушениями — прежде всего следствие активации аутоиммунитета, а не следствие нарушения функции щитовидной железы. Однако у беременных с антитиреоидными антителами часто снижен функциональный тиреоидный резерв, что проявляется развитием субклинического гипотиреоза на протяжении беременности у 42% женщин с аутоиммунными нарушениями, при этом на ранних сроках функция щитовидной железы не нарушена. В этом случае гипотиреоз — следствие снижения способности щитовидной железы адаптироваться к изменениям тиреоидного обмена, связанным с беременностью.
Развитие субклинического гипотиреоза можно прогнозировать по уровню ТТГ и титру АТ-ТПО в I триместре. Эти показатели — маркеры, позволяющие выявить женщин группы высокого риска невынашивания беременности с последующим проведением мониторинга функции щитовидной железы на протяжении беременности и назначением тироксина в индивидуальных случаях.
У женщин с привычным невынашиванием частота обнаружения органоспецифических антитиреоидных антител выше, чем органонеспецифических антител (к фосфолипидам, нуклеотидам и гистонам). Скрининг на наличие тиреоидных антител (антитироглобулиновых и АТ-ТПО) следует проводить в I триместре беременности, так как на протяжении беременности их уровень снижается на 50%.
В последние годы предлагается использовать определение тиреоидсвязывающего глобулина в качестве прогностического фактора исхода беременности при невынашивании. Изменение уровня тиреоидсвязывающего глобулина может быть связано с самопроизвольным прерыванием беременности, так как он косвенно отражает функцию плаценты (синтез эстрогенов). Диагностическая чувствительность определения тиреоидсвязывающего глобулина в группе высокого риска по невынашиванию беременности составляют 80%.
Скрининг гипотиреоза и аутоиммунного тиреоидита
Основной причиной спонтанного гипотиреоза является аутоиммунный тиреоидит. Для постановки диагноза аутоиммунного тиреоидита необходимы следующие признаки.
- Первичный гипотиреоз.
- Наличие антител к ткани щитовидной железы и УЗ-признаки аутоиммунной патологии.
Распространенность носительства АТ-ТПО достигает среди беременных 10-20%. Однако не всякое повышение уровня антител свидетельствует об аутоиммунном тиреоидите и развитии гипотиреоза. Диагностические критерии, при выявлении сочетания которых у беременной женщины целесообразно обсуждение вопроса о превентивной заместительной терапии L-тироксином, следующие.
- Повышение уровня АТ-ТПО.
- Увеличение уровня ТТГ на ранних сроках беременности более 2 мЕ/л.
- Увеличение объема щитовидной железы более 18 мл по данным УЗИ.
При выявлении повышенного уровня АТ-ТПО без других признаков аутоиммунного тиреоидита необходима динамическая оценка функции щитовидной железы во время беременности (в каждом триместре). Специфические клинические симптомы чаще всего отсутствуют и при гипотиреозе, даже манифестном, не говоря уже о субклиническом. Поэтому крупные эндокринологические ассоциации предложили проведение скрининга нарушений функции щитовидной железы у всех женщин на ранних сроках беременности, принимая во внимание высокую распространенность носительства АТ-ТПО и гипотиреоза в популяции, а также в силу следующих причин.
- Гипотиреоз и аутоиммунные тиреопатии достаточно часто встречаются у молодых женщин.
- Субклинический, а зачастую манифестный гипотиреоз не имеет специфических клинических проявлений.
- Повышен риск акушерских осложнений при некомпенсированном гипотиреозе.
- Повышен риск самопроизвольного прерывания беременности у женщин, имеющих высокий уровень АТ-ТПО.
- Повышен риск прогрессирования гипотиреоза во время беременности у женщин-носительниц АТ-ТПО.
- Повышен риск развития послеродовых тиреопатий у женщин-носительниц АТ-ТПО.
Предлагаемый скрининг базируется на определении уровня ТТГ и АТ-ТПО на ранних сроках беременности. Определение ТТГ и АТ-ТПО рекомендуется проводить как можно раньше, в идеале до 12 нед беременности. Если уровень ТТГ превышает 4 мЕ/л независимо от наличия или отсутствия антител, у пациентки с высокой вероятностью имеется гипотиреоз. Этим женщинам показана терапия L-тироксином на протяжении всей беременности. Если уровень ТТГ у носительниц АТ-ТПО составляет менее 2 мЕ/л, назначение L-тироксина не показано, но уровень ТТГ необходимо контролировать в каждом триместре беременности. В отношении женщин, имеющих АТ-ТПО и уровень ТТГ в нормальных пределах, но составляющий 2-4 мЕ/л, необходимо рассматривать вопрос о назначении превентивной терапии L-тироксином.
Тиреоидная патология и гестозы
Возрастание частоты гестозов у женщин с тиреоидными нарушениями не имеет удовлетворительного объяснения. У беременных с гестозом часто отмечается биохимический гипотиреоз, однако в большинстве случаев снижение FT4 со значительным повышением ТТГ позволило предположить наличие истинного гипотиреоза у этих пациенток. Сообщалось о так называемом «гестозоподобном» синдроме (preeclamptic-like syndrome) у беременных с гипотиреозом, поскольку гипотиреоз может клинически проявляться симптомами, сходными с симптомами гестоза. Так, гипотиреоз является установленной причиной обратимой гипертензии у небеременных; нарушение функции щитовидной железы может сочетаться с протеинурией, например у 30% больных аутоиммунным тиреоидитом выявлена протеинурия. Кроме того, протеинурия может приводить к возрастанию экскреции тироксина и тиреоидсвязывающих белков, что усугубляет гипотиреоз. У беременных с диагностированным гипотиреозом лечение «гестозоподобного» синдрома следует начинать с достижения эутиреоидного состояния, что при выраженной протеинурии может потребовать увеличения дозы тироксина, а при отсутствии указаний на патологию щитовидной железы у беременной с тяжелым гестозом показано исследование тиреоидной функции с последующей ее коррекцией.
Имеются данные, указывающие на избирательное снижение Т3 у беременных с гестозом (low T3-syndrome — синдром низкого Т3), при котором ингибируется процесс превращения Т4 в Т3, что биохимически проявляется снижением Т3 и FT3 при нормальных значениях Т4 и FT4, а клинически может проявляться симптомами гипотиреоза, поскольку биологическая активность Т3 гораздо более высока.
Заболевания щитовидной железы в послеродовом периоде
Частота встречаемости послеродового тиреоидита в послеродовом периоде составляет 5%. Как указывалось выше, при беременности течение заболеваний, обусловленных иммунными нарушениями, несколько улучшается вследствие иммуносупрессии беременности, однако в послеродовом периоде имеет место обратный эффект. Послеродовой тиреоидит, по-видимому, проявление этого ребаунд-эффекта. Клиническая картина послеродового тиреоидита характеризуется кратковременным гипертиреозом с последующим транзиторным гипотиреозом и выздоровлением. Однако следует отметить, что у 40% женщин с послеродовым тиреоидитом развивается постоянная тиреоидная недостаточность, а у 1/4 женщин с клиническим выздоровлением после этого заболевания гипотиреоз возникает через 3-4 года. Послеродовый тиреоидит формируется у 50% женщин с наличием антитиреоидных антител; их уровень достигает максимальных значений к 16-20 нед послеродового периода.
Существует взаимосвязь между нарушением функции щитовидной железы и послеродовой депрессией, общая частота которой в течение года после родов составляет 10-20%. Особенно часто депрессивные симптомы отмечаются у женщин с антитиреоидными антителами. У женщин с антитиреоидными антителами и нарушением функции щитовидной железы депрессивный синдром выражен в большей степени, чем у эутиреоидных антителопозитивных женщин. Скрининг на наличие антитиреоидных антител нужно проводить во время беременности с последующим исследованием функции щитовидной железы в послеродовом периоде у антителопозитивных женщин с целью своевременной коррекции тиреоидной дисфункции (заместительная гормонотерапия). Всех больных с послеродовым тиреоидитом необходимо периодически обследовать, поскольку не менее чем у 20-35% из них развивается постоянный гипотиреоз.
Принципы заместительной терапии гипотиреоза во время беременности
Современные концепции лечения многих заболеваний щитовидной железы, встречающихся в репродуктивном возрасте (Базедова болезнь, рак щитовидной железы), подразумевают удаление всей щитовидной железы и далее — заместительную терапию L-тироксином. Основные принципы заместительной терапии гипотиреоза во время беременности сводятся к следующему.
- Компенсированный гипотиреоз не есть противопоказание для планирования беременности.
- Во время беременности происходит увеличение потребности в Т4, требуется увеличение дозы L-тироксина (исходная доза — около 1,6-1,8 мкг/кг, что составляет 100 мкг).
- Сразу после наступления беременности у женщин с компенсированным гипотиреозом дозу L-тироксина увеличивают на 50 мкг.
- Контроль уровня ТТГ и FT4 проводят каждые 8-10 нед.
- Адекватной заместительной терапии соответствует поддержание низконормального (менее 2 мЕ/л) уровня ТТГ и высоконормального уровня FT4.
- При гипотиреозе, впервые выявленном во время беременности, женщине сразу назначается полная заместительная доза L-тироксина (2,3 мкг/кг веса) без ее постепенного увеличения, принятого при лечении гипотиреоза вне беременности.
- Подходы к лечению манифестного и субклинического гипотиреоза во время беременности не отличаются.
- После родов доза L-тироксина снижается до обычной заместительной (1,6-1,8 мкг/кг). Принимается утром за 30 мин до завтрака. Поливитамины, содержащие карбонат кальция, лучше принимать днем или вечером, ибо карбонат кальция существенно снижает биодоступность L-тироксина.
